
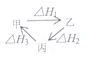
| A£® | ¼×”¢ŅŅ”¢±ūČżĪļÖŹ×Ŗ»ÆČēĶ¼ĖłŹ¾£¬Ōņ”÷H1=”÷H2+”÷H3 | |
| B£® | 1molCOĶźČ«Č¼ÉÕÉś³ÉĪȶØŃõ»ÆĪļ·Å³öČČĮæĪŖ283.0KJ£¬Ōņ2 CO2£Øg£©=2 CO£Øg£©+O2£Øg£©£¬”÷H=+566.0KJ•mol-1 | |
| C£® | ČōN2£Øg£©+3H2£Øg£©?2NH3£Øg£©£¬”÷H=-92.4KJ•mol-1£¬¹ŹŌŚÄ³ČŻĘ÷ÖŠ³äČė1mol N2Óė3molH2³ä·Ö·“Ó¦ŗ󣬷ųöµÄČČĮæĪŖ92.4KJ | |
| D£® | ³£ĪĀĻĀ£¬Ļ”HClŗĶĻ”NaOHČÜŅŗ·“Ӧɜ³É1molH2O·Å³öČČĮæĪŖ57.3 KJ£¬ĘäČČ»Æѧ·½³ĢŹ½ĪŖHCl£Øaq£©+NaOH£Øaq£©=NaCl£Øaq£©+H2O£Øaq£©£¬”÷H=-57.3KJ |
·ÖĪö A£®øł¾ŻøĒĖ¹¶ØĀɽųŠŠ¼ĘĖć£»
B.1molŅ»Ńõ»ÆĢ¼ĶźČ«Č¼ÉÕÉś³É1mol¶žŃõ»ÆĢ¼·Å³ö283kJµÄČČĮ棬Ōņ1mol¶žŃõ»ÆĢ¼·Ö½āÉś³É1molCOĪüŹÕ283kJµÄČČĮ棻
C£®ŗĻ³É°±µÄ·“Ó¦ĪŖæÉÄę·“Ó¦£¬µŖĘųŗĶĒāĘų²»æÉÄÜĶźČ«·“Ó¦£»
D£®Ė®µÄדĢ¬Ņ²ŅŗĢ¬£¬Ó¦øĆÓĆ”°l”±±ķŹ¾£¬²»ÄÜÓĆaq±ķŹ¾£»ĒŅģŹ±äµÄµ„Ī»“ķĪó£®
½ā“š ½ā£ŗA£®øł¾ŻĶ¼Ź¾¼°øĒĖ¹¶ØĀÉæÉµĆ£ŗ”÷H1=-”÷H2-”÷H3£¬¹ŹA“ķĪó£»
B.1molCOĶźČ«Č¼ÉÕÉś³ÉĪȶØŃõ»ÆĪļ·Å³öČČĮæĪŖ283.0KJ£¬Ōņ2mol¶žŃõ»ÆĢ¼·Ö½āÉś³É2molCOŗĶŃõĘųĪüŹÕ566kJµÄČČĮ棬øĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗ2CO2£Øg£©=2 CO£Øg£©+O2£Øg£©£¬”÷H=+566.0kJ•mol-1£¬¹ŹBÕżČ·£»
C£®ČōN2£Øg£©+3H2£Øg£©?2NH3£Øg£©£¬”÷H=-92.4KJ•mol-1£¬ĖµĆ÷Éś³É2mol°±Ęų·Å³ö92.4kJµÄČČĮ棬ÓÉÓŚŗĻ³É°±ĪŖæÉÄę·“Ó¦£¬ŌņŌŚÄ³ČŻĘ÷ÖŠ³äČė1mol N2Óė3molH2³ä·Ö·“Ó¦ŗó£¬Éś³ÉµÄ°±ĘųŠ”ÓŚ2mol£¬ĖłŅŌ·Å³öµÄČČĮæŠ”ÓŚ92.4kJ£¬¹ŹC“ķĪó£»
D£®³£ĪĀĻĀ£¬Ļ”HClŗĶĻ”NaOHČÜŅŗ·“Ӧɜ³É1molH2O·Å³öČČĮæĪŖ57.3 KJ£¬ÕżČ·µÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗHCl£Øaq£©+NaOH£Øaq£©=NaCl£Øaq£©+H2O£Øl£©£¬”÷H=-57.3kJ•mol-1£¬¹ŹD“ķĪó£»
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éĮĖČČ»Æѧ·½³ĢŹ½µÄŹéŠ“”¢øĒĖ¹¶ØĀÉŌŚČČ»Æѧ·½³ĢŹ½ÖŠµÄ¼ĘĖć£¬ĢāÄæÄѶČÖŠµČ£¬Ć÷Č·øĒĖ¹¶ØĀɵÄøÅÄī¼°Ó¦ÓĆ·½·ØĪŖ½ā“š¹Ų¼ü£¬×¢ŅāÕĘĪÕČČ»Æѧ·½³ĢŹ½µÄŹéŠ“ŌŌņ£»CĪŖŅדķµć£¬ŠčŅŖĆ÷Č·æÉÄę·“Ó¦µÄĢŲµć£®


 ĢōÕ½100µ„ŌŖ¼ģ²āŹŌ¾ķĻµĮŠ“š°ø
ĢōÕ½100µ„ŌŖ¼ģ²āŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | X”¢Y¾łÄÜČ¼ÉÕ£¬¶¼ÓŠ“óĮæÅØŃĢ²śÉś | |
| B£® | X¼ČÄÜŹ¹ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ«£¬Ņ²ÄÜŹ¹äåĖ®ĶŹÉ«£¬»¹ÄÜ·¢Éś¼Ó¾Ū·“Ó¦ | |
| C£® | YŹōÓŚ²»±„ŗĶĢž | |
| D£® | YµÄ¶žĀČ“śĪļÓŠČżÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| X | Y | Z | R | |
| Ö÷ŅŖ»ÆŗĻ¼Ū | -4£¬+4 | -4£¬+4 | -2£¬+6 | -1£¬+7 |
| A£® | ·Ē½šŹōŠŌ£ŗZ£¼R£¼Y | |
| B£® | TÓėRæÉŅŌŠĪ³É»ÆŗĻĪļ£ŗTR2 | |
| C£® | XÓėRµÄµ„ÖŹ¾łÄÜŹ¹Ę·ŗģČÜŅŗĶŹÉ«£¬ĒŅĶŹÉ«ŌĄķĻąĶ¬ | |
| D£® | TµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļ·Ö±šÄÜÓėX”¢Y”¢ZµÄ×īøß¼ŪŃõ»ÆĪļ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĶØČė×ćĮæSO2£ŗNa+”¢S2-”¢OH-”¢AlO2- | B£® | ĶØČė×ćĮæCO2£ŗK+”¢Ca2+”¢Cl-”¢NO3- | ||
| C£® | ĶØČė×ćĮæCl2£ŗSO2”¢Ba2+”¢Cl-”¢K+ | D£® | ĶØČė×ćĮæNH3£ŗFe3+”¢Cl-”¢Ba2+”¢Al3+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

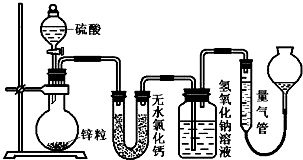
| A£® | Ķ¼¢Ł³£ÓĆÓŚ·ÖĄė·ŠµćĻą²ī½Ļ“óµÄŅŗĢå»ģŗĻĪļ | |
| B£® | Ķ¼¢ŚÓĆÓŚĪüŹÕĪ²ĘųSO2 | |
| C£® | Ķ¼¢ŪÓĆÓŚøÉŌļ”¢ŹÕ¼ÆÉŁĮæNH3 | |
| D£® | ²ÉÓĆĶ¼¢ÜµÄ²Ł×÷Åųö¼īŹ½µĪ¶Ø¹Ü¼ā×ģ“¦µÄĘųÅŻ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ŌŖĖŲXÓŠČżÖÖĶ¬Ī»ĖŲ | |
| B£® | ĘäÖŠŅ»ÖÖĶ¬Ī»ĖŲÖŹĮæŹżĪŖ36 | |
| C£® | ÖŹĮæŹżĪŖ35µÄĶ¬Ī»ĖŲŌ×ÓµÄÖŹĮæ·ÖŹżĪŖ75% | |
| D£® | ŌŖĖŲµ„ÖŹX2µÄĘ½¾łŹ½ĮæĪŖ71 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗžÄĻŹ”³¤É³ŹŠøßČżÉĻѧʌµŚ13“ĪÖܲāĄķæĘ×ŪŗĻ»ÆѧŹŌ¾ķ ĢāŠĶ£ŗŹµŃéĢā
±ł¾§ŹÆ(Na3 AlF6)ÄŃČÜÓŚĖ®£¬¹ć·ŗÓ¦ÓĆÓŚĀĮµÄŅ±Į¶”£¹¤ŅµÉĻÓĆÓ©ŹÆ(CaF2)ĪŖŌĮĻÉś²śNa3 AIF6£ŗ
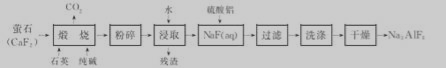
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Na3AIF6ĪŖÖśČܼĮ£¬Ņ±Į¶ĀĮµÄ»Æѧ·½³ĢŹ½ĪŖ ”£
£Ø2£©Š“³öģŃÉÕŹ±×Ü·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ________”£
£Ø3£©ģŃÉÕŗóµÄ¹ĢĢåŌŚ½žČ”Ē°½ųŠŠ·ŪĖéµÄÄæµÄŹĒ____£¬ĪŖ“ļµ½ĻąĶ¬ÄæµÄ£¬³£ĪĀ½žČ”Ź±»¹æɲÉČ”µÄ“ėŹ©ŹĒ____”£
£Ø4£©Š“³öĻņNaFČÜŅŗÖŠ¼ÓČėĮņĖįĀĮČÜŅŗ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ____”£NaFČÜŅŗ³Ź¼īŠŌ£¬ÓĆĄė×Ó·½³ĢŹ½±ķŹ¾ĘäŌŅņ£ŗ £¬Ņņ“ĖŌŚ°“»Æѧ¼ĘĮæ¼ÓČėĮņĖįĀĮČÜŅŗĒ°£¬ŠčĻČÓĆĮņĖį½«NaFČÜŅŗµÄpHĻĀµ÷ÖĮ5×óÓŅ£¬·ńŌņæÉÄܲśÉśø±²śĪļ ”£
£Ø5£©97.5kgŗ¬CaF280%Ó©ŹÆ£ØŌÓÖŹ²»ŗ¬·śŌŖĖŲ£©ĄķĀŪÉĻæÉÉś²śNa3 AIF6 kg£ØÉčÉś²ś¹ż³ĢÖŠµÄĆæŅ»²½ŗ¬·śĪļÖŹ¾łĶźČ«×Ŗ»Æ£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 27gAlÓė×ćĮæÅØĮņĖį»ģŗĻ£¬²śÉśĘųĢå33.6L£Ø±źæö£© | |
| B£® | 1molSiO2ÓėCĶźČ«·“Ó¦£¬Éś³É±ź×¼×“æöĘųĢå44.8L | |
| C£® | µē½ā¾«Į¶CuŹ±£¬Ńō¼«ĆæČܽā12.8gCu£¬Ņõ¼«Īö³ö0.2molCu | |
| D£® | 1mol/LµÄijŅ»ŌŖĖįČÜŅŗ£¬²āµĆpH=3£¬ČÜŅŗÖŠc£ØOH-£©Ņ»¶ØĪŖ1”Į10-11 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com