
 可简化为:
可简化为: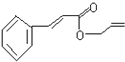 杀虫剂“阿乐丹”的结构表示为:
杀虫剂“阿乐丹”的结构表示为: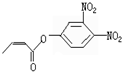 ,它在稀酸作用下能发生水解反应生成两种有机物.下列关于这两种有机物的共同性质叙述不正确的是( )
,它在稀酸作用下能发生水解反应生成两种有机物.下列关于这两种有机物的共同性质叙述不正确的是( )| A. | 遇FeCl3溶液均显紫色 | B. | 均能发生氧化反应 | ||
| C. | 均能与溴水发生反应 | D. | 均能与NaOH溶液发生反应 |
分析 有机物含有酯基,可发生水解反应,含有碳碳双键,可发生加成、氧化和加聚反应,水解产物为CH3CH=CHCOOH,另一种产物为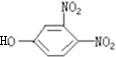 ,含有酚羟基和硝基,酚羟基可发生取代、氧化和显色反应,以此解答该题.
,含有酚羟基和硝基,酚羟基可发生取代、氧化和显色反应,以此解答该题.
解答 解:水解产物为CH3CH=CHCOOH和 ,
,
A.CH3CH=CHCOOH,不含酚羟基,故A错误;
B.CH3CH=CHCOOH含有碳碳双键,可发生氧化反应, 含酚羟基,可被氧化,故B正确;
含酚羟基,可被氧化,故B正确;
C.CH3CH=CHCOOH含有碳碳双键,可与溴水发生加成反应, 含有酚羟基,可与溴水发生取代反应,故C正确;
含有酚羟基,可与溴水发生取代反应,故C正确;
D.CH3CH=CHCOOH含有羧基, 含有酚羟基,都可与氢氧化钠反应,故D正确.
含有酚羟基,都可与氢氧化钠反应,故D正确.
故选A.
点评 本题综合考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握有机物的官能团的性质,为解答该题的关键,难度不大,注意相关基础知识的积累.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 .
. Al(OH)3+3H+(用离子方程式表示).
Al(OH)3+3H+(用离子方程式表示).| X | ||||
| Y | Z | W |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
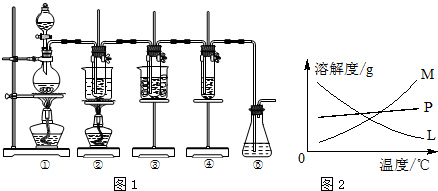
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卤素单质的最外层电子数都是7 | |
| B. | 从上到下,卤素原子的电子层数依次增多,半径依次减小 | |
| C. | 卤素单质与H2化合的容易程度为F2<Cl2<Br2<I2 | |
| D. | 从F到I,原子核对最外层电子的吸引能力依次减弱,原子得电子能力依次减弱,元素的非金属性依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状态下,1L庚烷完全燃烧后,所生成的气态产物的分子数为$\frac{7}{22.4}$NA | |
| B. | 1mol碳正离子CH5+所含的电子数为11NA | |
| C. | 标准状态下,16g甲烷完全燃烧所消耗的氧气的分子数为2NA | |
| D. | 0.5molC3H8分子中含C-H共价键2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
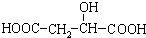 )广泛存在于水果中,尤以苹果、葡萄、西瓜、山
)广泛存在于水果中,尤以苹果、葡萄、西瓜、山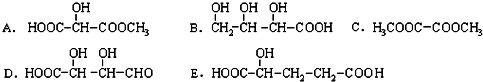
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 甲 | 乙 | 丙 | 丁 | |
| 化合物中各元素原子个数比 | A:C=1:1 | B:A=1:2 | D:E=1:3 | B:E=1:4 |
 ,丁的结构式
,丁的结构式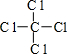
 ,最高价氧化物的水化物化学式为HClO4.
,最高价氧化物的水化物化学式为HClO4.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com