
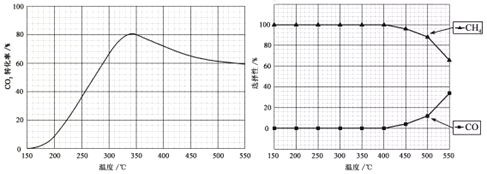
����Ŀ���ڳ�ѹ��Ru/TiO2���£�CO2��H2�������(�����1:4�������ʵ���a mol)���з�Ӧ�����CO2ת���ʡ�CH4��COѡ�������¶ȱ仯����ֱ�����ͼ��ʾ(ѡ����:ת����CO2������CH4��CO�İٷֱ�)��
��ӦI CO2(g)+4H2(g) CH4(g) + 2H2O(g) ��H1
��ӦII CO2(g) + H2(g) CO(g) + H2O(g) ��H2
����˵������ȷ����
A.��H1����
B.�¶ȿ�Ӱ������ѡ����
C.CO2ƽ��ת�������¶���������������
D.�����������䣬��CO2��H2�ij�ʼ����ȸı�Ϊ1:3�������CO2ƽ��ת����
���𰸡�CD
��������
A�������Ŀ������ͼ����֪��350-400�� CH4��ѡ����Ϊ100%��Ҳ����CH4��������ӦI������ͼ��֪�ڴ��¶����������¶ȣ�CO2ת�����½���ƽ�������ƶ������Է�ӦI����H1С���㣬��A��ȷ��
B��ͼ��2������֪��ͼ��仯�������¶����ߵ�400�����ϣ�CH4��COѡ�������¶�Ӱ�죬�����¶����ߣ������ѡ������С��һ����̼��ѡ���������¶ȿ�Ӱ������ѡ���ԣ���B��ȷ��
C����һ�����¶ȷ�Χ�ڣ�ֻ�����˷�ӦI��������H1��0����֪CO2ƽ��ת�������¶����߶����ͣ���C����
D����ͼ��CO2��H2������������1:4ʱ�õ������ߣ���Ҫ����CO2��ƽ��ת���ʣ�Ӧ���H2��ռ�ı�������D����
��ѡCD��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������CuSO4��5H2O��д[Cu(H2O)4]SO4��H2O����ṹʾ��ͼ���£�
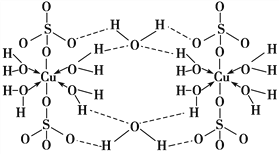
�����йص�����˵����ȷ���ǣ� ��
A. ������ԭ�Ӷ���ȡsp3�ӻ� B. ��ԭ�Ӳ����γ���λ����������ֻ�ѧ��
C. Cu2���ļ۵����Ų�ʽΪ3d84s1 D. �����е�ˮ�ڲ�ͬ�¶��»�ֲ�ʧȥ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ѱ���Ϊ21���͵�����ȼ�ϣ�Ҳ�������������������ȣ��Գ��������ƻ����á���ҵ�ϳ����ü״�������ˮ������ȡ���䷴Ӧ����ʽΪ��2CH3OH(g)![]() CH3OCH3(g)��H2O(g)
CH3OCH3(g)��H2O(g)
���������գ�
28���л�������ж���̼Ԫ�أ�д��̼ԭ���������ӵĹ����ʾʽ_______________��
д���״������й����ŵĵ���ʽ_________________��
29��̼��ͬ����Ķ�����Ԫ����ȣ��ǽ����Խ�ǿ����_________����Ԫ�ط��ţ���д��һ����֤����Ľ��۵Ļ�ѧ����ʽ_____________________________________��
30�����¶Ⱥ�������������£���˵����Ӧ�Ѵﵽƽ��״̬����______��ѡ���ţ�
a.CH3OH������������CH3OCH3����������֮��Ϊ2��1
b.������ѹǿ���ֲ���
c.H2O(g��Ũ�ȱ��ֲ���
d.����ƽ����Է����������ֲ���
31��һ���¶��£����������ԼΪ2.0 L�ĺ����ܱ������з���������Ӧ��
���� | �¶ȣ����� | ��ʼ���ʵ�����mol�� | ƽ�����ʵ�����mol�� | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
I | 387 | 0.40 | 0.16 | 0.16 |
�� | 387 | 0.80 | a | |
�� | 207 | 0.40 | 0.18 | 0.18 |
��1����Ҫ���CH3OH��ƽ��ת���ʣ����Բ�ȡ�Ĵ�ʩ��______��ѡ���ţ���
a.��ʱ���߲��� b.�����¶� c.����CH3OH d.�����¶�
��2��I�������ڵķ�Ӧ����t min�ﵽƽ�⣬��CH3OH��ƽ����Ӧ����Ϊ_____________���ú�t��ʽ�ӱ�ʾ����II��������a =___________mol��
32������ʼʱ������I�г���CH3OH 0.2mol��CH3OCH3 0.30mol��H2O 0.20mol����Ӧ����__________��������������������Ӧ������С�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���绯ѧ�̵������ڳ��³�ѹ��ʵ�ֵ����Ļ�ԭ�ϳɰ���ij���������һ��ȫ�µĵ绯ѧ�̵��������������⻯����ʾ��ͼ���£����й�˵���������
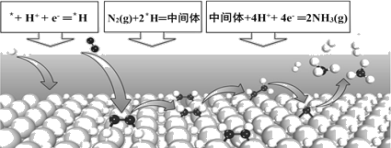
A.�ڱ����⻯�����У���һ����H+�Ļ�ԭ��Ӧ
B.�ڱ���*Hԭ���������Эͬ�����£�N2�����*Hԭ�ӷ�Ӧ����*N2H4�м���
C.�绯ѧ�̵����ϴ�ͳ��ҵ�ϳɰ����������ܺ�С�������Ѻõ��ŵ�
D.��������Ӧ�����ⷴӦ���Ļ���������ڹ̵���Ӧ�������ⷴӦ������ҪԶԶ���ڹ̵���Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�о���AgNO3��Һ�������Һ�е�Cl-��CrO42-�������룬������25��ʱAgCl��Ag2CrO4�������ܻ�������ܽ�ƽ�����ߡ����У�pAg+= -lgc(Ag+)�������������ơ������ཻ���ܽ�ƽ�����߰�ͼ��ֳ���X��Y��Z��M�ĸ���������˵���������( )

A.Ksp(Ag2CrO4)ԼΪ1 ��10-12��Ksp(AgCl)��������Ϊ10-10
B.M�����ڿ�����Ag2CrO4��������������AgCl����
C.��Cl-��CrO42-��Ϊ0.1 mol/ L�Ļ����Һ����μ���ϡ��������Һ��������AgCl����
D.��Ag2CrO4��AgCl��Ϲ����ˮ���ܽ�ƽ����ϵ�м�������ˮ�� ����
����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
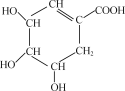
����Ŀ����������ç������Ϊ�ϳɴ��(�������Ϳ���ҩ)���м�����ܵ����ӣ���ṹ��ʽ��ͼ��ʾ��
 ��
��
(1)ç�����к������������ǻ���________(������)��
(2)ç����ķ���ʽΪ________��
(3)��ç������Һ�е���2��3����ɫʯ����Һ������Ϊ________��
(4)1 molç������һ�������º�H2�����ӳɷ�Ӧ���������________mol H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£��ֱ���1L0.1mol��L-1MgCl2��MnCl2��Һ�м���Na2CO3������(��������仯)����ͼΪ����Na2CO3�����ʵ�����-1gc(Mg2+)��-lgc(Mn2+)֮��Ĺ�ϵ����֪������Ksp(MgCO3)>Ksp(MnCO3)������˵����ȷ���ǣ� ��
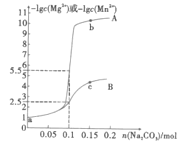
A.����A��n(Na2CO3)��-lgc(Mg2+)�Ĺ�ϵ����
B.Ksp(MnCO3)��Ksp(MgCO3)���3��������
C.����b���c����Һ��ϣ�����![]() =1��106
=1��106
D.a��(MgCl2��Һ)�д��ڣ�c(Mg2+)+c(H+)=c(OH-)+c(Cl-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)��ԭ�ӵ����������Ų�ʽ��__����Ԫ���ж��ֻ��ϼۣ��о�һ�������ֵ�Ԫ�ػ��ϼ۵Ļ�����__��
(2)��(N2H4)���ӿ���ΪNH3���ӵ�һ����ԭ�ӱ�-NH2(����)ȡ���γɵ���һ�ֵ����⻯�NH3���ӵĿռ乹����__����N2H4���Ӿ�����ͬ�������ķ����ж��֣����о��п�ȼ�Ե�������__(��ѧʽ)��
(3)�¿��������ȼ�ϣ�ȼ��ʱ�����ķ�Ӧ�ǣ�N2O4(l)+2N2H4(l)��3N2(g)+4H2O(g)+1038.7kJ�����÷�Ӧ����4molN-H�����ѣ����γɵ�������__mol������ת�Ƶ�����Ϊ__��
(4)���������ᷴӦ����N2H6SO4��N2H6SO4�����������������ͬ����N2H6SO4�ľ����ڲ�����__(����)
a�����Ӽ� b�����ۼ� c�������� d�����»���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����(VB2)-���������Ŀǰ����������ߵĵ��,���ʾ��ͼ����,�õ�ع���ʱ��ӦΪ:4VB2+11O2=4B2O3 +2V2O5������˵������ȷ����
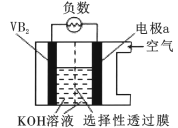
A. �缫a Ϊ�������
B. ͼ��ѡ������ĤΪ����������Ĥ
C. ��ع���������,�缫a��������pH��С
D. VB2�������ĵ缫��ӦΪ:2VB2 +22OH--22e- = V2O5+2B2O3 + 11H2O
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com