
【题目】如图为配制240mL0.2mol·L-1Na2CO3溶液的示意图。回答下列问题:
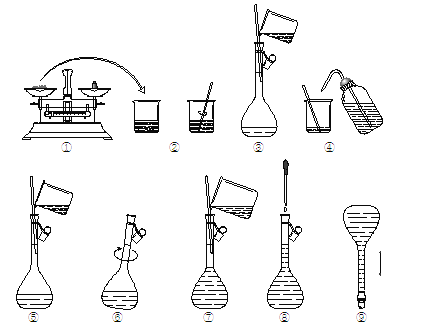
(1)①中称得Na2CO3__________g。
(2)玻璃棒在②、③两步中的作用分别是____________、_____________。
(3)若出现如下情况,对所配溶液浓度有何影响?(填 “偏高”“偏低”或“无影响”)
A.某同学在第⑧步观察液面时时俯视___________;
B.没有进行操作步骤④和⑤ ___________;
C.在第⑤步不慎有少量液体流到容量瓶外_____________。
科目:高中化学 来源: 题型:
【题目】2016年9月8日iphone7发布,软磁铁氧体是生产手机必不可少的材料,这种材料的原料之一是四氧化三锰。四氧化三锰的制法有焙烧法和还原法,某生产流程4:

(1)写出反应②的化学方程式:____________________________。实验室焙烧固体时用到的硅酸盐仪器是______________。
(2)通常所说的四氧化三锰中,锰元素的价态既有+2,可能也有+3和+4价。
假设一:锰的价态是+2和+4价。
假设二:锰的价态是____________。
假设三:锰的价态是_______________。
(3)查阅资料得知硫酸铵-硫酸溶液可选择性溶解试样中的二价锰。基于假设一成立,某化学兴趣小组同学进行如下表的研究,请完成表中的内容:
实验步骤(不要求写详细的操作过程) | 预期的实验结果和结论 |
①准确称取6.87克Mn3O4样品 | |
② | |
③ | |
④称量剩余固体的质量 |
(4)用高锰酸钾标准溶液滴定未知浓度的草酸氢钾溶液,滴定终点的标志是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ι)HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物。试回答下列问题:
(1)下列方法中,不能用来区分NaNO2和NaCl的是________(填序号)。
A.测定这两种溶液的pH
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI—淀粉溶液来区别
D.用AgNO3和HNO3两种试剂来区别
(2)某同学把新制的氯水加到NaNO2溶液中,请写出反应的离子方程式:________________。
(3)铝能溶解在碱性亚硝酸盐溶液中,生成能使湿润的红色石蕊变蓝的气体,请写出反应的离子方程式__________________;
(Ⅱ)某暗紫色化合物A在常温和干燥的条件下,可以稳定存在,但它在水溶液中不稳定,一段时间后转化为红褐色沉淀,同时产生一种气体单质。为探究其成分,某学习兴趣小组的同学取化合物A粉末进行试验。经组成分析,该粉末仅含有O、K、Fe三种元素。另取3.96g化合物A的粉末溶于水,滴加足量稀硫酸,向反应后的溶液中加入含有0.08mol KOH的溶液,恰好完全反应。过滤,将洗涤后的沉淀充分灼烧,得到红棕色固体粉末1.60g;将所得滤液在一定条件下蒸发可得到一种纯净的不含结晶水的盐10.44g。
(1)目前,人们针对化合物A的稳定性进行了大量的探索,并取得了一定的进展。
下列物质中有可能提高化合物A水溶液稳定性的是 。
A.醋酸钠 B.醋酸 C.Fe(NO3)3 D.KOH
(2)请设计一个实验方案,研究温度对化合物A溶液稳定性的影响
(3)下图表示足量 Fe粉还原KNO3溶液过程中,测出的溶液中相关离子浓度、pH随时间的变化关系(部分副反应产物曲线略去)。请根据图中信息写出t1时刻前该反应的离子方程式:
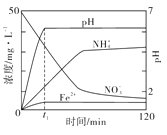
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学方程式是一种重要的化学用语。所写的化学方程式不能用来正确解释化学过程或事实的是
A.熔融烧碱时不能使用石英坩埚:SiO2+2NaOH![]() Na2SiO3 + H2O
Na2SiO3 + H2O
B.在海带灰的浸出液(含有I-)中滴加H2O2得到I2:2I-+3H2O2+2H+ →I2 +O2↑+4H2O
C.红热的铁丝与水接触,表面形成蓝黑色(或黑色)保护层:3Fe+4H2O(g)![]() Fe3O4+4H2
Fe3O4+4H2
D.“84消毒液”(有效成分NaClO)和“洁厕灵”(主要成分盐酸)混合使用时会放出氯气:
ClO-+Cl-+2H+→Cl2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由水电离出来的氢离子浓度为10-13 mol/L,在此溶液中一定能大量共存的离子组是
A. ClO—、K+、Cl— B. Ba2+、Na+、Br—
C. Na+、Fe3+、SO42— D. K+、NO3—、NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T时,向2.0L恒容密闭容器中充入1.0mol PCl5,反应PCl5(g)![]() PCl3(g)+Cl2(g)经一段时间后达到平衡.反应过程中测定的部分数据见下表:
PCl3(g)+Cl2(g)经一段时间后达到平衡.反应过程中测定的部分数据见下表:
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
下列说法正确的是
A.反应在前50s的平均速率为v(PCl3)=0.0032molL﹣1s﹣1
B.保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11molL﹣1,则反应的△H<0
C.相同温度下,起始时向容器中充入1.0mol PCl5、0.20mol PCl3和0.20mol Cl2,达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入2.0mol PCl3、2.0mol Cl2,达到平衡时,PCl3的转化率小于80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
I.根据下列物质的名称(俗名)写出相应的化学式。
(1) 二氧化碳: ;(2) 硫粉: ;(3) 亚硫酸: ;
(4) 氢氧化钙: ;(5) 纯碱: ;(6) 氧化铝: 。
II.根据下列反应写出相应的化学方程式。
(7) 稀盐酸与CaCO3反应: ;
(8) 制作Fe(OH)3胶体: 。
III.现有三种可加热的仪器:①试管;②烧杯;③蒸发皿。
(9) 其中能够直接加热的是(填序号): ;
(10)仪器①在加热固体时,试管口应 ;仪器③在蒸发实验中,所加液体体积不超过容积的 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100℃时,水的离子积为1×10-12 mol2·L-2,若该温度下某溶液中的H+浓度为1×10-7 mol·L-1,则该溶液是
A. 酸性 B. 中性 C. 碱性 D. 无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数的数值,下列说法中正确的是( )
A.常温常压下,18 g重水(D2O)所含的中子数为10NA
B.100℃时,1L pH=1的硫酸溶液中,含有0.2NA个H+
C.71g氯气发生氧化还原反应,一定失去2NA个电子
D.室温下,14gN2和CO的混合气体中含有的原子数目为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com