
����Ŀ����25��ʱ����100mL���Ȼ���14.6g��������Һ�����5.6g�����ۣ������Ƿ�Ӧǰ����Һ����ı仯������Ӧ��ʼ��2minĩ�ռ�������1.12L����������ڴ�֮���־���4min����ȫ���ܽ⣮��
��1����ǰ2min����FeCl2��ʾ��ƽ����Ӧ�����Ƕ��٣�
��2���ں�4min����HCl��ʾ��ƽ����Ӧ�����Ƕ��٣�
��3��ǰ2min���4min��ȣ���Ӧ�����ĸ��Ͽ죿Ϊʲô���Խ���ԭ��
���𰸡�
��1���⣺��Ӧǰ�Ȼ����������ʵ���Ϊ0��
Fe+2HCl= | FeCl2 + | H2 �� |
56g | 1mol | 22.4L |
2.8g | 0.05mol | 1.12L |
v��FeCl2 ��= ![]() =0.25 mol/��L��min����
=0.25 mol/��L��min����
�ʴ�Ϊ 0.25 mol/��L��min����
��2���⣺��Ӧǰ�Ȼ�������ʵ���Ϊ ![]() =0.4mol���������ʵ���Ϊ
=0.4mol���������ʵ���Ϊ ![]() ��Ϸ���ʽ֪���Ȼ��������ͨ����1��֪��ǰ�����ӣ�����Ӧ2.8g����ʣ2.8g��2min��4minʱ������Ӧ2.8g��
��Ϸ���ʽ֪���Ȼ��������ͨ����1��֪��ǰ�����ӣ�����Ӧ2.8g����ʣ2.8g��2min��4minʱ������Ӧ2.8g��
Fe+ | 2HCl=FeCl2 +H2 �� |
56g | 2 mol |
2.8g | 0.1mol |
�����Ȼ�������ʵ����ı仯��Ϊ0.1mol��
���� 4min��C��HCl ��= ![]() =0.25 mol/��L��min����
=0.25 mol/��L��min����
�ʴ�Ϊ 0.25 mol/��L��min����
��3���⣺����ͬһ��Ӧ��ͬһʱ������У������ʵķ�Ӧ����֮�ȵ��ڼ�����֮�ȣ�����ǰ�������ڣ��Ȼ����ƽ����Ӧ����Ϊ0.5mol/��L��min����2min��4minʱ���Ȼ����ƽ����Ӧ����Ϊ0.25 mol/��L��min����
����ǰ�������ڷ�Ӧ���ʿ죬ԭ���ǣ����ŷ�Ӧ�Ľ��У������ӵ�Ũ�Ȳ��ϼ�С�����Է�Ӧ���ʽ��ͣ�
����������1����������������������ɵ��Ȼ����������ʵ����������÷�Ӧ���ʹ�ʽ�����Ȼ�������ƽ����Ӧ���ʣ���2�������2min�������ӵ����ʵ����ı仯�����ٸ���ƽ����Ӧ���ʹ�ʽ���㣻��3������Ũ���뷴Ӧ���ʵĹ�ϵ������
�����㾫�������÷�Ӧ���ʵĶ�����ʾ��������Ŀ�����жϼ��ɵõ��𰸣���Ҫ��֪��Ӧ���ʵĵ�λ��mol/(L��min)��mol/(L��s) v=��c-��t��


 ��ѧ����ϵ�д�
��ѧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͬ��ͬѹ�£���ͬ���������и�����ȫȼ������O2���������ǣ� ��
A.����
B.��ϩ
C.��Ȳ
D.����ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Т�������������������Һ�����廯����Һ����ˮ�Ļ��Һ���������ǵ���ȷ���������ǣ�������
A. ��Һ������B. ��Һ����ȡC. ��ȡ����ҺD. ����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2L�ܱ������У�����3A��g��+B��g��2C��g����Ӧ�����������A��B����4mol��A��ƽ����Ӧ����Ϊ0.12mol/��Ls������10���Ӻ������е�B�ǣ� ��
A.2.8mol
B.1.6mol
C.3.2mol
D.3.6mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ѧϰС����ͨ��ʵ�飬̽��Mg��NO3��2���ȷֽ�IJ��
С����룺����������������Mg��NO2��2��MgO��Mg3N2�е�һ�ֻ���
����������������NO2��N2��O2�е�һ�ֻ���
���������ϣ�a��Mg��NO2��2��Mg��NO3��2������ˮ��MgO������ˮ��
b.2NO2+2NaOH�TNaNO3+NaNO2+H2O
c��Mg3N2+6H2O�T3Mg��OH��2��+2NH3��
������ϲ��룬�������ͼ��ʾʵ�飨ͼ�м��ȡ��г�������װ�þ�ʡ�ԣ���
����ʵ��
��������װ�������ԣ�
��ȡ3.7gMg��NO3��2���壬����Ӳ�ʲ�����A�У���K��ͨ��һ��ʱ��N2 �� ���������������������
�ر�K���þƾ��Ƴ�����װ��A���ȣ������и�װ������Һ��δ����������װ�ã�
������Mg��NO3��2��ȫ�ֽ⣬װ����ȴ�����£���K���ٻ���ͨ��һ��N2���ٳ������Ƶ�A��ʣ���������Ϊ1.0g��B��C��D��E��F����Һ�����ֱ�������2.3g��0.0g��0.1g��0.3g��0.05g��
����ȡ����ʣ��������Թ��У���������ˮ��δ������������
�ش�����
��С��Ԥ��һ����O2���ɣ������� ��
��N2�ĵ���ʽ�� �� ������У�ͨ��һ��ʱ��N2��Ŀ���� ��
�۲�����У�װ��A���������˺���ɫ���壬�仯ѧʽ�� ��
��װ��C������ɫʼ��δ�ʣ�����Ƶ�Ŀ���� ��
��ʵ���з���Mg��NO3��2�ֽ�ʱ��O2���ɣ���ʵ�������� �� �û�ѧ������Ͳ������������ԭ���� ��
��ʵ����Mg��NO3��2�ֽ�û��N2���ɵ������� ��
��Mg��NO3��2�ֽ�Ļ�ѧ����ʽ�� ��
��װ��F����Һ�������ӵ�ԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ԫ�����ڱ���˵����ȷ����
A. Ԫ�����ڱ���8������B. ��A���Ԫ��ȫ���ǽ���Ԫ��
C. ��������ָ��һ��������D. Ԫ�����ڱ���7������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����
A. 1molNe��1molO2�������ͬ
B. 1mol��������ԼΪ22.4L
C. �ڱ�״���£�1mol�κ����ʵ����ԼΪ22.4L
D. �ڱ�״���£�1molNe��Cl2�Ļ����������ԼΪ22.4L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ѻ��Ҵ���ͬ���칹�壬�����ɲ��û�ѧ�������������������м����в��ܶԶ��߽��м�����ǣ� ��
A.���ý����ƻ��߽�����
B.��������
C.���ú������
D.���ú˴Ź�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������пƬ�ʹ�ͭƬ��ͼʾ��ʽ����ͬŨ�ȵ�ϡ������һ��ʱ�䣬����������ȷ���ǣ� �� 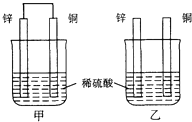
A.���ձ���ͭƬ����������ݲ���
B.���ձ�����Һ��pH������
C.����ͭƬ������������ͭƬ�Ǹ���
D.�������ݵ��ٶȼױ�����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com