
| A. | ①②③④⑤ | B. | ⑤④③①② | C. | ②④③①⑤ | D. | ③④②①⑤ |
分析 由于海水含有大量的氯化镁,因此常用海水来制备金属镁,大体步骤为:将石灰乳加入海水或卤水中,沉淀出氢氧化镁,氢氧化镁再和稀盐酸反应生成氯化镁,然后对得到的氯化镁溶液蒸发结晶,电解熔融状态的氯化镁,就能得到金属镁.
解答 解:根据题意提供的五个步骤采用逆推法分析:最后一步应该是⑤电解熔融的氯化镁MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑;
再往前一步应该是制备熔融的氯化镁,分析应该是①浓缩结晶;
再往前一步应该是制备氯化镁溶液了,Mg(OH)2+2HCl═MgCl2+2H2O,分析应该是③;
再往前一步应该是④过滤得到氢氧化镁沉淀.
第一步应该是将海水的中镁离子富集起来,常用的方法是沉淀,应该是②MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2;所以顺序为②④③①⑤.
故选:C.
点评 本题难度不大,主要考查了海水制镁的过程,培养学生解决问题的能力,更全面地了解分离混合物的方法.


科目:高中化学 来源: 题型:多选题
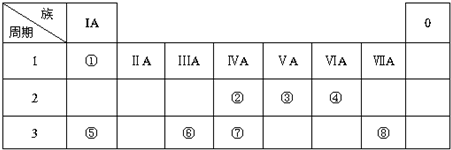
| A. | B位于第二周期第ⅣA族 | |
| B. | A在同周期元素中原子半径最小 | |
| C. | A、B没有最高正化合价 | |
| D. | B、C所形成的化合物会引发温室效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2CH2CH3和CH3CH(CH3)2 | B. | CH2═C(CH3)2和CH3CH═CHCH3 | ||
| C. | CH3CH2OH和CH3OCH3 | D. | CH3CH2CH2COOH和CH3COOCH2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 直线形;三角锥形 | B. | V形;三角锥形 | ||
| C. | 直线形;平面三角形 | D. | V形;平面三角形 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ② | C. | ③ | D. | ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
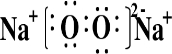 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
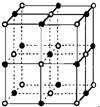 决定物质性质的重要因素是物质结构.请回答下列问题:
决定物质性质的重要因素是物质结构.请回答下列问题:| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
| 共价键 | C-C | C-N | C-S |
| 键能/kJ•mol-1 | 347 | 305 | 259 |
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ•mol-1 | 786 | 715 | 3401 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com