
| A. | 1:2:3 | B. | 1:2:2 | C. | 6:3:2 | D. | 1:1:1 |
分析 钠和稀硫酸、水都反应,镁和铝分别与稀硫酸反应方程式为Mg+H2SO4=MgSO4+H2↑、2Al+3H2SO4=Al2(SO4)3+3H2↑,0.1molMg、Al完全反应需要硫酸的物质的量分别是0.1mol、0.15mol,实际上n(H2SO4)=1mol/L×0.1L=0.1mol,所以铝剩余.
解答 解:钠和稀硫酸、水都反应,镁和铝分别与稀硫酸反应方程式为Mg+H2SO4=MgSO4+H2↑、2Al+3H2SO4=Al2(SO4)3+3H2↑,0.1molMg、Al完全反应需要硫酸的物质的量分别是0.1mol、0.15mol,实际上n(H2SO4)=1mol/L×0.1L=0.1mol,所以铝都剩余.
根据2Na~H2↑可知,0.1molNa完全反应,生成氢气的物质的量=0.1mol×$\frac{1}{2}$=0.05mol,
Mg与硫酸恰好反应生成的氢气为0.1mol;
铝剩余,按照硫酸的物质的量计算氢气为0.1mol;
同温同压下产生的气体体积比=0.05mol:0.1mol:0.1mol=1:2:2,
故选B.
点评 本题考查有关方程式的计算,把握反应方程式中物质之间的关系以及过量判断为解答的关键,侧重分析与计算能力的考查,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CCl4和CH2Cl2 | B. | H3O+和NH4+ | C. | CaO2和CaF2 | D. | Ba(OH)2和NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
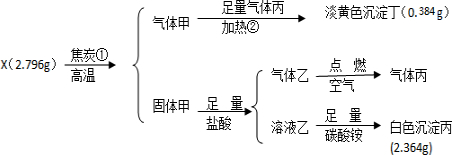
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v1>v2 | B. | v1<v2 | C. | v1=v2 | D. | 无法肯定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该反应的平衡常数表达式为K=$\frac{{c}^{2}(CO)}{c(C{O}_{2})•c(C)}$ | |
| B. | 550℃时,反应达平衡后CO2的转化率约为5.7% | |
| C. | 650℃时,平衡后再充入体积比为3:2的CO2和CO的混合气体,则平衡不移动 | |
| D. | T℃时,该反应的平衡常数的数值为1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⑤①⑥③⑦ | B. | ⑤②⑥③⑦ | C. | ⑤②⑥④⑦ | D. | ⑤①⑥④⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 2NaOH+H2↑+Cl2↑;
2NaOH+H2↑+Cl2↑;| 温度(℃) | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 70℃ | 80℃ | 90℃ | 100℃ |
| NaOH | 42 | 51 | 109 | 119 | 129 | 145 | 174 | 299 | 314 | 329 | 347 |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com