
有氧化镁、氧化铝的混合物完全溶于200mL盐酸,而后逐滴加入1.0mol·L-1的NaOH溶液。当加入的NaOH的体积V1=20mL时,开始有沉淀析出,且沉淀量随NaOH加入量逐渐增加。当NaOH的体积V2=520mL时,沉淀量达最大值,继续滴加NaOH时,沉淀量逐渐减小。当V3=620mL时,沉淀量不再减少。
(1)最初加入的20mL NaOH溶液的作用是什么?
(2)所用盐酸的物质的量浓度为多少?
(3)氧化镁、氧化铝物质的量比为多少?
(共8分)(1)中和过量的盐酸(2分)
(2)沉淀量最大时所用OH-的物质的量与100mL强酸中H+的物质的量相等,n(OH-)=1.0mol·L-1×0.52L=0.52mol,故n(H+)也为0.52mol,盐酸的浓度为2.6mol·L-1 (2分)
(3) 根据Al(OH)3+OH-=AlO2-+2H2O
该反应用去的n(NaOH)=1.0mol·L-1×(0.62-0.52)L=0.10mol
故Al(OH)3为0.10mol,而Al2O3为0.050mol
根据Al3++3OH-=Al(OH)3生成Al(OH)3用去0.30mol NaOH。而生成氢氧化镁也用去0.20mol NaOH,氢氧化镁为0.10mol,氧化镁、氧化铝物质的量比为2:1(4分)说明:所有合理答案均给分。


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:阅读理解
| 实验步骤 | 预期实验现象 | 预期实验结论 |
分别取30mL 0.5mol?L-1 MgCl2、AlCl3溶液于烧杯中,充分混合 分别取30mL 0.5mol?L-1 MgCl2、AlCl3溶液于烧杯中,充分混合 |
无现象 无现象 |
溶液中水解不能生成沉淀 溶液中水解不能生成沉淀 |
向混合溶液中滴入2滴酚酞试液,逐滴加入1mol?L-1 NaOH溶液 向混合溶液中滴入2滴酚酞试液,逐滴加入1mol?L-1 NaOH溶液 |
当溶液中生成大量的白色絮状沉淀后溶液的颜色不变 当溶液中生成大量的白色絮状沉淀后溶液的颜色不变 |
产生的沉淀可能是氢氧化铝、氢氧化镁或二者的混合物 产生的沉淀可能是氢氧化铝、氢氧化镁或二者的混合物 |
将上述混合溶液过滤,洗涤,再向滤渣中加入过量的1mol?L-1 NaOH溶液 将上述混合溶液过滤,洗涤,再向滤渣中加入过量的1mol?L-1 NaOH溶液 |
滤渣全部溶解 滤渣全部溶解 |
产生的沉淀只有氢氧化铝 产生的沉淀只有氢氧化铝 |
空 空 |
空 空 |
空 空 |
| 实验步骤 | 实验现象 | 实验结论 |
| ①另取0.5mol?L-1 MgCl2、AlCl3溶液各30mL于不同烧杯中 | 溶液中无现象 溶液中无现象 |
水溶液中无氢氧化镁、氢氧化铝沉淀生成 水溶液中无氢氧化镁、氢氧化铝沉淀生成 |
| ②向0.5mol?L-1 AlCl3溶液中逐滴加入NaOH溶液至刚好反应完全 | 产生沉淀,沉淀溶解,沉淀消失 | 产生氢氧化铝沉淀,加过量的氢氧化钠溶液后氢氧化铝又溶解 |
| ③将MgCl2溶液全部倒入②反应后的溶液中 | 产生大量白色沉淀 | 二者混合时相互促进水解最终生成Mg(OH)2和Al(OH)3沉淀. 二者混合时相互促进水解最终生成Mg(OH)2和Al(OH)3沉淀. |
查看答案和解析>>
科目:高中化学 来源:学习周报 化学 人教课标高一版(必修1) 2009-2010学年 第13期 总第169期 人教课标版 题型:038
将一定量氧化镁、氧化铝的混合物完全溶于
200 mL盐酸中,而后逐滴加入1.0 mol/L NaOH溶液.溶液中生成沉淀的物质的量随加入NaOH溶液的体积的变化趋势如图所示.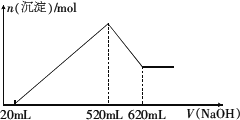
(1)说明最初加入20 mL NaOH溶液的作用.
(2)求所用盐酸的物质的量浓度.
(3)求原混合物中氧化镁、氧化铝的物质的量之比.
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:013
有氧化镁、氧化铝混合粉未18.2g,将它溶于500mL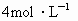 的盐酸里,若要使沉淀质量达到最大值,则需加入
的盐酸里,若要使沉淀质量达到最大值,则需加入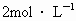 的氢氧化钠溶液的体积为
的氢氧化钠溶液的体积为
[ ]
查看答案和解析>>
科目:高中化学 来源: 题型:
有氧化镁、氧化铝的混合物完全溶于200mL盐酸,而后逐滴加入1.0mol?L-1的NaOH溶液。当加入的NaOH的体积V1=20mL时,开始有沉淀析出,且沉淀量随NaOH加入量逐渐增加。当NaOH的体积V2=520mL时,沉淀量达最大值,继续滴加NaOH时,沉淀量逐渐减小。当V3=620mL时,沉淀量不再减少。
(1)最初加入的20mL NaOH溶液的作用是什么?
(2)所用盐酸的物质的量浓度为多少?
(3)氧化镁、氧化铝物质的量比为多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com