
| A��������50�棬��Һ��Ca2+��Ũ������ | ||
B�����¶���Ca��OH��2���ܽ��Ϊ
| ||
| C���ñ���ʯ��ˮ�У�ˮ�������OH-��Ũ��Ϊ10-12mol/L | ||
D��������ʯ�Ҳ��ָ������º�
|
| 0.37 |
| 1000d |
| a |
| 100+a |
| 37 |
| 1000d-0.37 |
| c(H+)c(OH-) |
| c(Ca2+) |


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��C12ͨ��KI��Һ |
| B����ˮ���������Һ |
| C��������ͭ����ϡ���� |
| D��KSCN��Һ����FeCl3��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ȹ������Ͼ������ͽṹ |
| B����Ȼ������������ǿ�� |
| C�����������ȶ�����Ȼ��ά |
| D���л���������ʱ�����������ڼӹ����ͣ���һ�ֹ����β��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
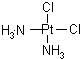 ���п������ã���
���п������ã��� û�������ã��Դ�����������ȷ���ǣ�������
û�������ã��Դ�����������ȷ���ǣ�������| A������Ϊͬ���칹�壬������Ptԭ��Ϊ���ĵ�������ṹ |
| B������Ϊͬ���칹�壬������Ptԭ��Ϊ���ĵ�ƽ��ṹ |
| C������Ϊͬһ���ʣ�������Ptԭ��Ϊ���ĵ�������ṹ |
| D������Ϊͬһ���ʣ�������Ptԭ��Ϊ���ĵ�ƽ��ṹ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
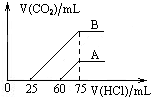 ȡA��B�������ʵ���Ũ����ȵ�NaOH��Һ�������Ϊ50mL���ֱ�������ͨ��һ������CO2���ٷֱ�ϡ�͵�100mL����ϡ�ͺ����Һ�зֱ�μ�0.1mol/L�����ᣬ������CO2�������״��������������������ϵ��ͼ��ʾ������˵����ȷ���ǣ�������
ȡA��B�������ʵ���Ũ����ȵ�NaOH��Һ�������Ϊ50mL���ֱ�������ͨ��һ������CO2���ٷֱ�ϡ�͵�100mL����ϡ�ͺ����Һ�зֱ�μ�0.1mol/L�����ᣬ������CO2�������״��������������������ϵ��ͼ��ʾ������˵����ȷ���ǣ�������| A��ԭNaOH��Һ�����ʵ���Ũ��0.075mol?L-1 |
| B��A���߱���ԭ��Һͨ��CO2����������ΪNaOH��Na2CO3����ʱ�÷�̪��ָʾ������Һ��ɫ�仯ʱ������������Ϊ75mL |
| C��B���߱���ԭ��Һͨ��CO2����������ΪNa2CO3��NaHCO3�����ʵ���֮��Ϊ1��1 |
| D��B���߱���ԭ��Һͨ��CO2���������������ᷴӦ���������������Ϊ33.6mL����״���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ڳ��³�ѹ�£�11.2LN2���еķ�����С��0.5NA |
| B����״���£�2.24LSO3���е�ԭ����Ϊ0.4NA |
| C����1L 2 mol/L��FeCl3��Һ�Ƴɽ�������к�����������������Ϊ2NA |
| D��46gNO2��N2O4�������������ԭ����Ŀ�п���Ϊ3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1molCH3+��̼�����ӣ�����9 NA������ |
| B��2.5molHe ���10 NA������ |
| C��6.02��1022 ��H2SO4��������Һ�пɵ����2NA��H+ |
| D��1molFe��������ȫ��Ӧ��ʧȥ���ӵ����ʵ���Ϊ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��̼�������Һ�еμ�����������������Һ��Ca2++HCO3-+OH-=CaCO3��+H2O | ||||
| B����������ϡ���ᷴӦ��2Al+6H+=2Al3++3H2�� | ||||
C����NH4HCO3��Һ�мӹ���NaOH��Һ�����ȣ�NH4++OH-
| ||||
| D��̼�������Һ�м������ϡ���CO32-+2H+=CO2��+H2O |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com