
【题目】钴是一种中等活泼金属,化合价为+2价和+3价,其中CoC12易溶于水。某校同学设计实验制取(CH3COO)2Co(乙酸钴)并验证其分解产物。回答下列问题:
(1)甲同学用Co2O3与盐酸反应制备CoC124H2O,其实验装置如下:
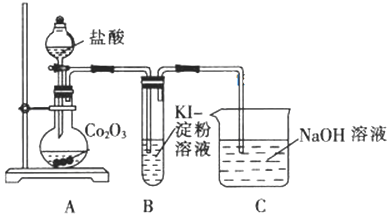
①烧瓶中发生反应的离子方程式为______。
②由烧瓶中的溶液制取干燥的CoC124H2O,还需经过的操作有蒸发浓缩、______、洗涤、干燥等。
(2)乙同学利用甲同学制得的CoC124H2O在醋酸氛围中制得无水(CH3COO)2Co,并利用下列装置检验(CH3COO)2Co在氮气气氛中的分解产物。已知PdC12溶液能被CO还原为Pd。
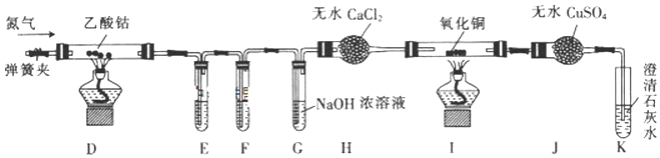
①装置E、F是用于检验CO和CO2的,其中盛放PdC12溶液的是装置______(填“E”或“F”)。
②装置G的作用是______;E、F、G中的试剂均足量,观察到I中氧化铜变红,J中固体由白色变蓝色,K中石灰水变浑浊,则可得出的结论是______。
③通氮气的作用是______。
④实验结束时,先熄灭D和I处的酒精灯,一段时间后再关闭弹簧夹,其目的是______。
⑤若乙酸钴最终分解生成固态氧化物X、CO、CO2、C2H6,且n(X):n(CO):n(CO2):n(C2H6)=1:4:2:3(空气中的成分不参与反应),则乙酸钴在空气气氛中分解的化学方程式为______。
【答案】Co2O3+6H++2Cl-=2Co2++Cl2↑+3H2O 冷却结晶、过滤 F 除去CO2 分解产物中还含有一种或多种含C、H元素的物质 将D中的气态产物被后续装置所吸收,或排除装置中的空气或不使K中水蒸气进入盛无水CuSO4的干燥管中 防止倒吸 3(CH3COO)2Co![]() Co3O4+4CO↑+2CO2↑+3C2H6↑
Co3O4+4CO↑+2CO2↑+3C2H6↑
【解析】
(1)①已知,盐酸、COCl2易溶于水,写离子形式,氧化物、单质写化学式,反应的离子方程式: Co2O3+2Cl-+6H+=2Co2++Cl2↑+3H2O;
②因反应产物中含有结晶水,则不能直接加热制取,应采用:蒸发浓缩、降温结晶、过滤、洗涤干燥等操作;
(2)①装置E、F是用于检验CO和CO2,PdCl2溶液能被CO还原为Pd,因此装置E用于检验CO2,F装置用于检验CO,装盛足量PdCl2溶液;
②装置G的作用是吸收CO2,以防在装置内对后续实验产生干扰;氧化铜变红,则氧化铜被还原,无水硫酸铜变蓝,说明反应中产生水,石灰水变浑浊,则说明产生二氧化碳气体,则说明分解产物中含有一种或多种含有C、H元素的物质;
③通入氮气的作用为使D装置中产生的气体全部进入后续装置,且排净后续装置内的氧气等;
④实验结束时,先熄天D和I处的酒精灯,一段时间后装置D、E内的温度降低后再停止通入气体可以有效防止倒吸;
⑤乙酸钴受热分解,空气中的成分不参与反应生成物有固态氧化物X、CO、CO2、C2H6,且n(X) ︰ n(CO)︰n(CO2) ︰n(C2H6)=1︰4︰2︰3,根据原子守恒配平即可;
(1)①已知,盐酸、COCl2易溶于水,写离子形式,氧化物、单质写化学式,反应的离子方程式: Co2O3+2Cl-+6H+=2Co2++Cl2↑+3H2O;
②因反应产物中含有结晶水,则不能直接加热制取,应采用:蒸发浓缩、降温结晶、过滤、洗涤干燥等操作;
(2)①装置E、F是用于检验CO和CO2,PdCl2溶液能被CO还原为Pd,因此装置E用于检验CO2,F装置用于检验CO,装盛足量PdCl2溶液;
②装置G的作用是吸收CO2,以防在装置内对后续实验产生干扰;氧化铜变红,则氧化铜被还原,无水硫酸铜变蓝,说明反应中产生水,石灰水变浑浊,则说明产生二氧化碳气体,则说明分解产物中含有一种或多种含有C、H元素的物质,答案为:除去CO2;分解产物中含有一种或多种含C、H元素的物质;
③通入氮气的作用为使D装置中产生的气体全部进入后续装置,且排净后续装置内的氧气等,答案为:将D中的气态产物带入后续装置(或排除装置中的空气或不使K中水蒸气进入盛无水硫酸铜的干燥管等);
④实验结束时,先熄天D和I处的酒精灯,一段时间后装置D、E内的温度降低后再停止通入气体可以有效防止倒吸,答案为:防止倒吸;
⑤乙酸钴受热分解,空气中的成分不参与反应生成物有固态氧化物X、CO、CO2、C2H6,且n(X) ︰ n(CO)︰n(CO2) ︰n(C2H6)=1︰4︰2︰3,根据原子守恒配平即可,反应式为:3(CH3COO)2Co ![]() Co3O4+4CO↑+2CO2↑+3C2H6↑;
Co3O4+4CO↑+2CO2↑+3C2H6↑;


 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:高中化学 来源: 题型:
【题目】常温下,将100 mL 1 mol·L-1的氨水与100 mL a mol·L-1盐酸等体积混合,忽略反应放热和体积变化,下列有关推论不正确的是
A. 若混合后溶液pH=7,则c(NH4+)=c(Cl-)
B. 若a=2,则c(Cl-)>c(NH4+)>c(H+)>c(OH-)
C. 若a=0.5,则c(NH4+)>c(Cl-)>c(OH-)>c(H+)
D. 若混合后溶液满足c(H+)=c(OH-)+c(NH3·H2O),则可推出a=1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲、乙两装置电极材料都是铁棒与碳棒,请回答下列问题:
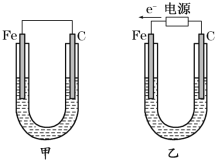
(1)若两装置中均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲装置中的________棒,乙装置中的________棒。
②乙装置中阳极的电极反应式是:_______________________________。
(2)若两装置中均为饱和NaCl溶液:
①写出乙装置中总反应的离子方程式:__________________________________。
②甲装置中碳极的电极反应式是____________________,乙装置碳极的电极反应属于________(填“氧化反应”或“还原反应”)。
③将湿润的淀粉KI试纸放在乙装置碳极附近,发现试纸变蓝,解释其原因:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】奈必洛尔是一种用于血管扩张的降血压药物,一种合成奈必洛尔中间体G的部分流程如下:
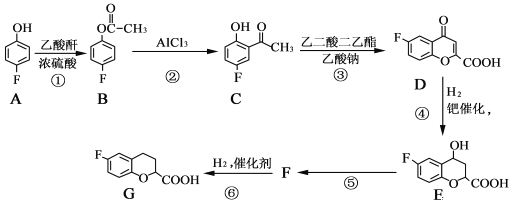
已知:乙酸酐的结构简式为![]() 。
。
请回答下列问题:
(1)A的名称是______;B中所含官能团的名称是______。
(2)反应⑤的化学方程式为______,该反应的反应类型是______。
(3)G的分子式为______。
(4)写出满足下列条件的E的同分异构体的结构简式:______、______。
Ⅰ.苯环上只有三个取代基
Ⅱ核磁共振氢谱图中只有4组吸收峰
Ⅲ.1mol该物质与足量NaHCO3溶液反应生成2molCO2
(5)根据已有知识并结合相关信息,写出以![]() 为原料制备
为原料制备 的合成路线流程图(无机试剂任选)______,合成路线流程图示例如下:CH3CH2Br
的合成路线流程图(无机试剂任选)______,合成路线流程图示例如下:CH3CH2Br![]() CH3CH2OH
CH3CH2OH![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)2012年伦敦奥运会火炬采用丙烷为燃料。丙烷热值较高,污染较小,是一种优良的燃料。试回答下列问题:

①如图是一定量丙烷完全燃烧生成CO2和1 mol H2O(l)过程中的能量变化图,请在图中的括号内填入“+”或“-”。
②写出表示丙烷燃烧热的热化学方程式:___________________________________。
③二甲醚(CH3OCH3)是一种新型燃料,应用前景广阔。1 mol二甲醚完全燃烧生成CO2和液态水放出1 455 kJ热量。若1 mol丙烷和二甲醚的混合气体完全燃烧生成CO2和液态水共放出1 645 kJ热量,则混合气体中,丙烷和二甲醚的物质的量之比为________。
(2)盖斯定律认为:不管化学过程是一步完成或分几步完成,整个过程的总热效应相同。试运用盖斯定律回答下列问题:
①已知:H2O(g)=H2O(l) ΔH1=-Q1 kJ/mol C2H5OH(g)=C2H5OH(l) ΔH=-Q2 kJ/mol
C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g) ΔH3=-Q3 kJ/mol
若使46 g液态无水酒精完全燃烧,并恢复到室温,则整个过程中放出的热量为________kJ。
②碳(s)在氧气供应不充足时,生成CO同时还部分生成CO2,因此无法通过实验直接测得反应: C(s)+![]() O2(g)=CO(g)的ΔH。但可设计实验、利用盖斯定律计算出该反应的ΔH,计算时需要测得的实验数据有________。
O2(g)=CO(g)的ΔH。但可设计实验、利用盖斯定律计算出该反应的ΔH,计算时需要测得的实验数据有________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下有:①6.72LCH4,②3.01×1023个HCl分子,③13.6gH2S,④0.2molNH3。下列对这四种气体的描述正确的是( )
a.体积②>③>①>④ b.密度②>③>④>①
c.质量②>③>①>④ d.氢原子个数①>③>④>②
A.abcB.bcdC.cbdD.abcd
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池是化学对人类的一项重大贡献。
(1)某兴趣小组为研究原电池原理,设计如图装置。
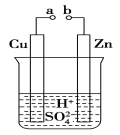
①a和b不连接时,烧杯中发生反应的离子方程式是 ________________________________________。
②a和b用导线连接,Cu极为原电池________极(填“正”或“负”),该电极反应式是_____________________________,溶液中的H+移向________(填“Cu”或“Zn”)极。
③无论a和b是否连接,Zn片均被腐蚀,若转移了0.2 mol电子, 则理论上Zn片质量减轻________g。
(2)如图是甲烷燃料电池原理示意图,回答下列问题:
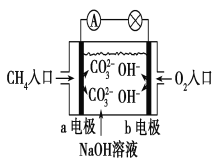
①电池的负极是________(填“a”或“b”)电极,该极的电极反应式为: _________________________。
②电池工作一段时间后电解质溶液的pH__________(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某二元弱酸H2A溶液,按下式发生电离:H2A![]() H++HA-、HA-
H++HA-、HA-![]() H++A2-,下列四种溶液中c(H2A)最大的是( )
H++A2-,下列四种溶液中c(H2A)最大的是( )
A. 0.01 mol·L-1的H2A溶液
B. 0.01 mol·L-1的NaHA溶液
C. 0.02 mol·L-1的盐酸与0.04 mol·L-1的NaHA溶液等体积混合液
D. 0.02 mol·L-1的NaOH与0.02 mol·L-1的NaHA溶液等体积混合液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应的离子方程式中正确的是( )
A. 盐酸与碳酸钡反应:CO32-+2H+ = CO2↑+H2O
B. 硫酸铜溶液中滴加氢氧化钡溶液:Ba2++SO42-= BaSO4↓
C. 澄清石灰水与少量小苏打溶液混合:Ca2+ + OH-+ HCO3-= CaCO3↓ + H2O
D. 向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com