
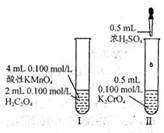
研究教材中演示实验,如右图所示,下列有关分析正确是
A.I、II中随反应进行反应速率均逐渐减小,直至为零
B.H2C2O4和H2SO4均为电解质
C.反应I和II均为氧化还原反应
D.其他条件不变,若将I反应中H2C2O4浓度改为0.2 mol·L-1,溶液褪色时间缩短,是因为增大反应物浓度,反应物中活化分子百分数提高
 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
下列各组离子在指定溶液中能大量共存的是( )
①pH=11的溶液中:CO32﹣、Na+、AlO2﹣、NO3﹣
②无色溶液中:K+、Na+、MnO4﹣、SO42﹣
③加入Al能放出H2的溶液中:Cl﹣、HCO3﹣、SO42﹣、NH4+
④含有Fe2+的溶液中:[Fe(CN)6]3﹣、NO3﹣、Cl﹣
⑤由水电离出的c(OH﹣)=1×10﹣13mol•L﹣1的溶液中:Na+、Ba2+、Cl﹣、Br﹣.
|
| A. | ①⑤ | B. | ②③ | C. | ②④ | D. | ③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知水的电离平衡曲线如图所示,
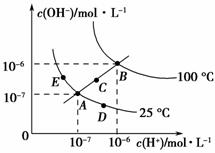
试回答下列问题:
(1)图中五点的KW间的关系是______________________________________。
(2)若从A点到D点,可采用的措施是________。
a.升温
b.加入少量的盐酸
c.加入少量的NH4Cl
(3)点E对应的温度下,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为________。
(4)点B对应的温度下,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在现代化学分析测试中,常借助一些仪器来分析化学物质的组成.下列有关说法不正确的是()
A. 用红外光谱仪确定物质中是否存在Na+、K+、Cu2+等离子
B. 用元素分析仪确定物质中是否含有C、H、O、N、S等
C. 用原子吸收光谱确定物质中含有哪些金属元素
D. 用pH计来测量溶液的酸碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:KClO3+NH4NO2→KCl+NH4NO3
(1)指出以上反应中的氧化剂是KClO3,被氧化的元素是N;
(2)配平上述反应方程式并标明电子转移的方向和数目 .
查看答案和解析>>
科目:高中化学 来源: 题型:
在一绝热且体积不变的密闭容器中发生以下反应:
N2(g)+3H2(g)  2NH3(g)ΔH=-92.2 kJ·mol-1,可以判断该反应已经达到化学平衡的是
2NH3(g)ΔH=-92.2 kJ·mol-1,可以判断该反应已经达到化学平衡的是
①单位时间内生成n molN2的同时生成2n molNH3
②1个N≡N 键断裂的同时,有2个N-H键断裂
③N2、H2 NH3 的物质的量浓度之比为1 : 3 : 2的状态
④混合气体的压强不再改变的状态
⑤混合气体的密度不再改变的状态
⑥ 混合气体的平均相对分子质量不再改变的状态
⑦ 3v正(H2)=2v逆(NH3)的状态
⑧NH3占混合气体的体积分数不再改变的状态 ⑨反应容器温度不再改变的状态
A. ①②⑤⑥⑨ B.③④⑤⑥⑧⑨ C.①④⑤⑥⑦⑨ D. ①④⑤⑥⑧⑨
查看答案和解析>>
科目:高中化学 来源: 题型:
某烯烃与氢气加成后得到2,2﹣二甲基丁烷,则该烯烃的名称是( )
|
| A. | 3,3﹣二甲基﹣1﹣丁烯 | B. | 2,2﹣二甲基﹣2﹣丁烯 |
|
| C. | 2,2﹣二甲基﹣1﹣丁烯 | D. | 2,2﹣二甲基﹣3﹣丁烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
写出下列反应化学方程式,并写出该反应属于何反应类型.
(1)乙烯使溴水退色 ;
(2)实验室制取乙烯的反应 ;
(3)由乙炔制聚氯乙烯 nH ;
(4)乙烷与Cl2在光照条件下1:1反应 .
查看答案和解析>>
科目:高中化学 来源: 题型:
纳豆是一种减肥食品,从纳豆中分离出一种由C、H、O 3种元素组成的有机物A,为确定其结构,现进行如下各实验:
①6.0 g物质A在一定条件下完全分解,生成3.36 L(标准状况)一氧化碳和1.8 g水;
②中和0.24 g物质A,消耗0.20 mol·L-1的氢氧化钠溶液20.00 mL;
③0.01 mol物质A完全转化为酯,需乙醇0.92 g;0.01 mol A能与足量钠反应放出0.336 L标准状况下的氢气。
试确定:
(1)A的摩尔质量及化学式。
(2)A的结构简式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com