
有机物CH3﹣CH═CH﹣Cl不 能发生的反应有( )
①取代反应 ②加成反应 ③消去反应 ④使溴水褪色 ⑤使酸性KMnO4溶液褪色 ⑥与AgNO3溶液生成白色沉淀 ⑦聚合反应.
|
| A. | ①②③④⑤⑥⑦ | B. | ⑦ | C. | ⑥ | D. | ② |
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:
NA为阿伏加德罗常数,下列说法正确的是( )
A. 标准状况下,11.2 L的戊烷所含的分子0.5NA
B. 28 g乙烯所含共用电子对数目为4NA
C. 标准状况下,11.2 L二氯甲烷所含分子数为0.5 NA
D. 现有乙烯、丙烯、丁烯的混合气体共14 g,其原子数为3 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)图1为元素X的前五级电离能的数值示意基态图,已知X的原子序数小于20,请写出X基态原子的核外电子排布式

(2)A、B、C、D、E、F、G、H八种连续短周期元素,其单质的沸点如图2所示.请回答:
①上述元素中,某些元素的常见单质所形成的分子中既含有σ键又含有π键的是 (填化学式).
②已知D、F、G三种元素的离子具有跟E相同的电子层结构,则B、C、D三种元素的第一电离能由大到小的顺序为(用相关元素符号表示) .
③B元素与D元素形成的化合物的电子式为 ,价层电子对互斥模型为 ,中心原子的杂化方式为 .
④已知H的电负性为1.5,而氯元素的电负性为3.0,二者形成的化合物极易水解,且易升华.据此推测该化合物的化学键类型为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,对于可逆反应N2(g)+3H2(g)⇌2NH3(g),若X、Y、Z的起始浓度分别为C1、C2、C3(均不为零),到达平衡时,N2、H2、NH3的浓度分别为0.1mol•L﹣1、0.3mol•L﹣1、0.08mol•L﹣1,则下列判断正确的是( )
|
| A. | C1:C2=1:3 |
|
| B. | 平衡时,H2和NH3的生成速率之比为2:3 |
|
| C. | N2、H2的转化率之比为1:3 |
|
| D. | C1的取值范围为0.04mol•L﹣1<Cl<0.14mol•L﹣1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
将一定量的CO2气体通入500mL某NaOH溶液中,充分反应后,将溶液在低温进蒸发,得到不含结晶水的白色固体A.取三份质量不同的A样品分别与50mL相同浓度的盐酸反应,得到气体的体积(标准状况)与固体A的质量关系职下表所示:
| 组 别 | ① | ② | ③ |
| 盐酸体积(mL) | 50 | 50 | 50 |
| A的质量 (g) | 3.80 | 5.70 | 7.60 |
| 气体体积(mL) | 896 | 1344 | 1344 |
(1)上表中第 组数据加入的50mL盐酸的反应后有剩余,
(2)试推断:A的成份为
(3)盐酸的物质的量的浓度为 mol•L﹣1.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验处理不可行的是( )
①将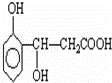 与NaOH的醇溶液共热制备CH3﹣CH═CH2
与NaOH的醇溶液共热制备CH3﹣CH═CH2
②向甲酸和甲醛的混合物中加入氢氧化钠溶液,中和甲酸后,加入新制的氢氧化铜加热﹣﹣检验混合物中是否含有甲醛
③向丙烯醛(CH2=CH﹣CHO)中滴入KMnO4(H+)溶液,观察紫色褪去,能证明结构中存在碳碳双键
④为验证某RX是碘代烷,把RX与烧碱水溶液混合加热后,将溶液冷却后再滴入几滴硝酸银溶液,观察现象.
|
| A. | 只有①③ | B. | 只有①②④ | C. | 只有②③④ | D. | 都不能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)饱和一元醇通式为CnH2n+1OH.
①出现醇类同分异构体时,n最小值为 ;
②出现官能团异构体时,n最小值为 .
(2)已知戊醇(C5H12O)共有8种属于醇类的异构体,请回答:
在戊醇的这些同分异构体中,能氧化生成醛的有4种,它们的结构简式分别是 、 、 、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式的是( )
A.向Fe(NO3)2稀溶液中加入盐酸:3Fe2++4H++NO3﹣═3Fe3++NO↑+2H2O
B.铜片与浓硝酸:Cu+NO3﹣+4H+═Cu2++NO2↑+2H2O
C.氯化铵浓溶液跟浓NaOH溶液混合后加热:NH4++OH﹣═NH3•H2O
D.碳酸氢铵溶液与足量的NaOH溶液混合后加热:NH4++ OH﹣═NH3↑+H2O
OH﹣═NH3↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物A、B是中学常见的物质,其阴、阳离子只能从下表中选择:
| 阳离子 | K+、Na+、Fe2+、Ba2+、NH |
| 阴离子 | OH-、NO |
(1) 若A、B的水溶液均为无色,且A的水溶液呈强酸性,B的水溶液呈强碱性。混合后产生不溶于稀盐酸的白色沉淀及能使湿润的红色石蕊试纸变蓝色的气体。
① B的化学式为_____________。
② A、B溶液混合加热反应的离子方程式_____________________________________。
(2) 若A的水溶液呈浅绿色,B的水溶液无色且其焰色反应为黄色。向A的水溶液中加入稀盐酸无明显现象,再加入B后溶液变黄,但A、B的水溶液混合亦无明显变化。则
① A的化学式为_____________。
② 经分析上述过程中溶液变黄的原因可能有两种(用离子方程式表示)
Ⅰ___________________ __;Ⅱ_____________________________________。
③ 请用一简易方法证明上述溶液变黄的原因_______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com