
如何降低大气中CO2的含量及有效地开发利用CO2,已引起了全世界的普遍重视。“低碳经济”正成为科学家研究的主要课题。
(1)已知: ① CO(g)+H2O(g) H2(g)+CO2(g) ΔH=-41kJ·mol-1
H2(g)+CO2(g) ΔH=-41kJ·mol-1
② C(s)+2H2(g) CH4(g) ΔH=-73kJ·mol-1
CH4(g) ΔH=-73kJ·mol-1
③ 2CO(g) C(s)+CO2(g) ΔH=-171kJ·mol-1
C(s)+CO2(g) ΔH=-171kJ·mol-1
写出CO2与H2反应生成CH4和H2O的热化学方程式 。
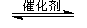 (2)将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g) + 6H2(g) CH3OCH3(g) + 3H2O(g)
(2)将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g) + 6H2(g) CH3OCH3(g) + 3H2O(g)
已知一定条件下,该反应中CO2的平衡转化率随温度、投料比[n(H2) / n(CO2)]的变化曲线如下左图:
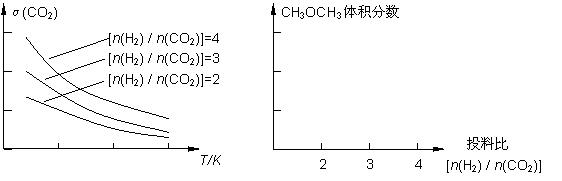
①在其他条件不变时,请在下图中画出平衡时CH3OCH3的体积分数随投料比[n(H2)/n(CO2)]变化的曲线图。
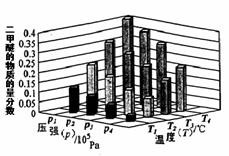
②某温度下,将2.0molCO2(g)和6.0mol(g)充入容积为2L的密闭容器中,反应到达平衡时,改变压强和温度,平衡体系中CH3OCH3(g)的物质的量分数变化情况如图所示,关于温度和压强的关系判断正确的是 ;
A. P3>P2,T3>T2 B. P1>P3,T1>T3
C. P2>P4,T4>T2 D. P1>P4,T2>T3
③在恒容密闭容器里按体积比为1:3充入二氧化碳和氢 气,一定条件下反应达到平衡状态。当改变反应的某一个条件后,下列变化能说明平衡一定向逆反应方向移动的是 ;
A. 正反应速率先增大后减小 B. 逆反应速率先增大后减小
C. 化学平衡常数K值增大 D. 反应物的体积百分含量增大
E. 混合气体的密度减小 F. 氢气的转化率减小
(3)最近科学家再次提出“绿色化学”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为可再生燃料甲醇。甲醇可制作燃料电池,写出以稀硫酸为电解质甲醇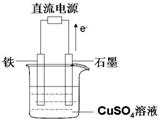 燃料电池负极反应式____ 。以此燃料电池作为外接电源按右图所示电解硫酸铜溶液,如果起始时盛有1000mL pH=5的硫酸铜溶液(25℃,CuSO4足量),一段时间后溶液的pH变为1,此时可观察到的现象是 ;若要使溶液恢复到起始浓度(温度不变,忽略溶液体积的变化),可向溶液中加入 (填物质名称),其质量约为 g。
燃料电池负极反应式____ 。以此燃料电池作为外接电源按右图所示电解硫酸铜溶液,如果起始时盛有1000mL pH=5的硫酸铜溶液(25℃,CuSO4足量),一段时间后溶液的pH变为1,此时可观察到的现象是 ;若要使溶液恢复到起始浓度(温度不变,忽略溶液体积的变化),可向溶液中加入 (填物质名称),其质量约为 g。
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
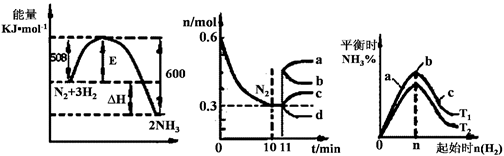
将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡: NH2COONH4(s) 2NH3(g)+CO2(g);不能判断该分解反应已经达到平衡的是:( )
2NH3(g)+CO2(g);不能判断该分解反应已经达到平衡的是:( )
A.密闭容器中氨气的浓度不变 B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.2v(NH3)=v(CO2)
查看答案和解析>>
科目:高中化学 来源: 题型:
 可经三步反应制取
可经三步反应制取 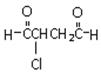 ,发生反应的类型依次是
,发生反应的类型依次是
A.水解反应、加成反应、氧化反应 B.加成反应、水解反应、氧化反应
C.水解反应、氧化反应、加成反应 D.加成反应、氧化反应、水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
 A是生产某新型工程塑料的基础原料之一,分子式为C10H10O2,其分子结构模型如图所示(图中球与球之间连线代表单键或双键)。
A是生产某新型工程塑料的基础原料之一,分子式为C10H10O2,其分子结构模型如图所示(图中球与球之间连线代表单键或双键)。
Ⅰ.根据分子结构模型写出A的结构简式________________________________ ______________________________________________。
Ⅱ.拟从芳香烃 出发来合成A,其合成路线如下:
出发来合成A,其合成路线如下:
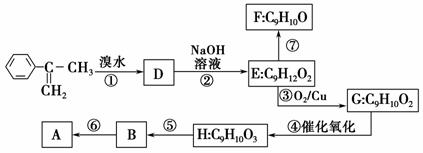
已知:A在酸性条件下水解生成有机物B和甲醇。
(1)写出⑤的反应类型______________________________________________。
(2)写出H的结构简式______________________________________________。
(3)已知F分子中含有“—CH2OH”,通过F不能有效、顺利地获得B,其原因是__________________ __________________________________________。
__________________________________________。
(4)写出反应方程式(注明必要的反应条件):
⑥_______________________________________________________________;
⑦_________________________________ ______________________________。
______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是
| 选项 | 叙述I | 叙述II |
| A | NaHCO3能与碱反应 | NaHCO3用作糕点的膨松剂 |
| B | 实验室常用MgSO4溶液与NaOH溶液制备Mg(OH)2沉淀 | Mg(OH)2不溶于强碱 |
| C | Cl2与Fe反应生成FeCl3 | 把FeCl3溶液直接蒸发结晶可以制备出FeCl3固体 |
| D | 铜丝与浓硫酸反应完,冷却后向试管中加入水来观察CuSO4溶液的蓝色 | 铜与浓硫酸反应生成了CuSO4和SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
对于实验I〜IV的描述正确的是
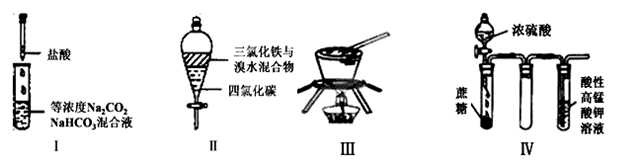
A.实验I :逐滴滴加稀盐酸时,试管中立即产生大量气泡
B.实验II:充分振荡后静置,下层溶液为橙红色,上层无色
C.实验III:从饱和食盐水中提取NaCl晶体
D.装置IV:酸性KMnO4溶液中有气泡出现,且溶液颜色逐渐变浅乃至褪去
查看答案和解析>>
科目:高中化学 来源: 题型:
运用化学反应原理研究氮、硫等单质及其化合物的反应有重要意义
(1)硫酸生产过程中2SO2(g)+O2(g)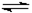 2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如右图所示,根据右图回答下列问题:
2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如右图所示,根据右图回答下列问题:
①2SO2(g)+O2(g)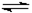 2SO3(g)的△H__________0(填“>”或“<”),
2SO3(g)的△H__________0(填“>”或“<”),
②一定条件下,将SO2与O2以体积比2:1置于一体积不变的密闭容器中发生以上反应,能说明该反应已达到平衡的是 。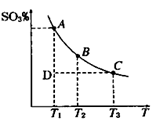
a.体系的密度不发生变化 b.SO2与SO3的体积比保持不变
c.体系中硫元素的质量百分含量不再变化
d.单位时间内转移4 mol 电子,同时消耗2 mol SO3
e.容器内的气体分子总数不再变化
 (2)一定的条件下,合成氨反应为:N2(g)+3H2(g)
(2)一定的条件下,合成氨反应为:N2(g)+3H2(g) 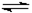 2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
图1 图2 图3
①该反应的平衡常数表达式为 ,升高温度,平衡常数 (填“增大”或“减小”或“不变”)。
②由图2信息,计算0~10min内该反应的平均速率v(H2)= ,从11min起其它条件不变,压缩容器的体积为1L,则n(N2)的变化曲线为 (填“a”或“b”或“c”或“d”)
③图3 a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是 点,温度T1 T2(填“>”或“=”或“<”)
(3)若将等物质的量的SO2与NH3溶于水充分反应,所得溶液呈 性,所得溶液中c(H+)-c(OH-)= (填表达式)(已知:H2SO3:Ka1=1.7×10-2,Ka2=6.0×10-8,NH3·H2O:Kb=1.8×10-5)
查看答案和解析>>
科目:高中化学 来源: 题型:
西维因是一种高效低毒杀虫剂,在碱性条件下可水解:
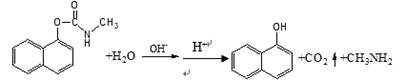 有关说法正确的是
有关说法正确的是
A.西维因分子式为C12H10NO2 B.西维因分子中至少有21个原子共平面
C.水解后的两种有机产物,各有一种官能团
D.反应后的溶液经酸化,不可用FeCl3溶液检验西维因是否已经发生水解
查看答案和解析>>
科目:高中化学 来源: 题型:
在含有I-且能使甲基橙试液变红的溶液中能大量共存的离子组为 ( )
A.Fe3+、Na+、Br- B.NH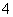 、Na+、[Al(OH)4]-
、Na+、[Al(OH)4]-
C.Ba2+、Al3+、Cl- D.K+、MnO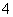 、NO
、NO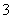
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com