
| A. |  将海带灼烧灰化 | B. | 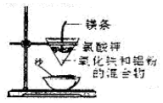 铝热反应 | ||
| C. | 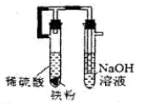 制取氢氧化亚铁 | D. | 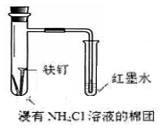 验证铁的吸氧腐蚀 |
分析 A.灼烧固体应在坩埚中进行;
B.在镁引燃条件下,可发生铝热反应,反应放出大量的热,可用沙子接收熔化的固体;
C.实验装置无法将硫酸亚铁溶液转移到氢氧化钠溶液中;
D.氯化铵溶液呈酸性,应发生析氢腐蚀.
解答 解:A.蒸发皿用于蒸发溶液,灼烧固体应在坩埚中进行,故A错误;
B.氧化铁和铝在高温下发生置换反应,图示装置能够发生铝热反应,故B正确;
C.实验装置无法将硫酸亚铁溶液转移到氢氧化钠溶液中,不能完成实验,故C错误;
D.氯化铵溶液呈酸性,应发生析氢腐蚀,如发生吸氧腐蚀,应在中性或碱性条件下,故D错误.
故选B.
点评 本题考查了化学实验方案的评价,为高考常见题型,涉及海带灼烧、铝热反应、物质的制备装置等知识,明确常见化学实验基本操作方法为解答关键,试题培养了学生的化学实验能力,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 物质的量浓度为0.5 mol/L的MgCl 2溶液中,共含有Cl - 个数为 N A | |
| B. | 1mol任何气体的体积都为 22.4L | |
| C. | 7.8gNa 2O 2中所含阴离子的数目是0.1N A | |
| D. | 标准状况下,2.24L水中含有的分子数为0.1N A |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
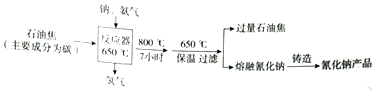

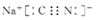 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 称取碳酸钠晶体(Na2CO3•10H2O)100g来配制0.5mol/L的Na2CO3溶液1000mL | |
| B. | 配制NH3NO3溶液,在烧杯中溶解后立即注入容量瓶,并立即进行下面的各项操作 | |
| C. | 定容后,将容量瓶振荡均匀,静置时发现液面低于刻度线,于是又加入少量水至刻度线 | |
| D. | 容量瓶用蒸馏水洗净后未经干燥马上用来配制溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO3-、OH-、Na+ | B. | Fe2+、H+、Cl- | C. | Fe2+、OH-、NO3- | D. | Fe2+、H+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
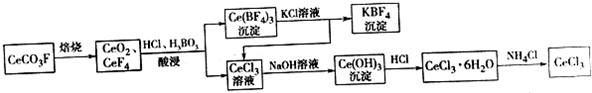
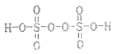 ,其中S元素的化合价为:+6.过硫酸铵(NH4)2Fe(SO4)2溶液将Ce3+氧化Ce4+为的离子方程式为:S2O42-+2Ce3+=2Ce4++2SO42-
,其中S元素的化合价为:+6.过硫酸铵(NH4)2Fe(SO4)2溶液将Ce3+氧化Ce4+为的离子方程式为:S2O42-+2Ce3+=2Ce4++2SO42-查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烷和乙烯均可使酸性KMnO4溶液褪色 | |
| B. | 甲烷燃烧会生成CO2,因此不属于清洁能源 | |
| C. | 向甲苯中滴入少量浓溴水,振荡,静置,溶液分层,上层呈橙红色,下层几乎无色,可知甲苯和溴水发生取代反应,使溴水褪色 | |
| D. | 水煤气、裂解气、焦炉气、天然气都是混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入足量的NaOH溶液充分振荡后,用分液漏斗分液弃除下层溶液 | |
| B. | 加入溴水,生成三溴苯酚,再过滤除去 | |
| C. | 加水,加热超过 70℃(苯酚在热水中溶解度很大),然后用分液漏斗振荡分液后,弃除下层溶液 | |
| D. | 将混合物蒸馏(甲苯沸点110℃,苯酚沸点182℃),可先蒸出甲苯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com