
| A. | 0.1mol/LCH3COONa与0.1mol/LHCl溶液等体积混合:c(Na+)=c(Cl-)>c(CH3COO-)>c(OH-) | |
| B. | 0.1mol/LNa2CO3与0.1mol/LNaHCO3溶液等体积混合:2c(Na+)=3c(CO32-)+3c(HCO3-)+3c(H2CO3) | |
| C. | Na2C2O4溶液与HCl溶液等体积混合(H2C2O4是二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)+c(Cl-)=c(Na+)+c(H+) | |
| D. | 0.1mol/LNH4Cl与0.1mol/L氨水溶液等体积混合:c(NH3•H2O)>c(NH4+)>c(Cl-)>c(OH-) |
分析 A.0.1mol/LCH3COONa与0.1mol/LHCl溶液等体积混合,生成等物质的量CH3COOH和NaCl;
B.根据物料守恒分析;
C.根据电荷守恒分析;
D.NH3•H2O的电离程度大于NH4+的水解程度.
解答 解:A.0.1mol/LCH3COONa与0.1mol/LHCl溶液等体积混合,生成等物质的量CH3COOH和NaCl,钠离子与氯离子不水解,二者的浓度相同,即c(Na+)=c(Cl-),CH3COOH是弱酸在溶液中部分电离,所以c(Na+)=c(Cl-)>c(CH3COO-)>c(OH-),故A正确;
B.0.1mol/LNa2CO3与0.1mol/LNaHCO3溶液等体积混合,钠离子的总浓度是C的最浓度的1.5倍,所以溶液中:2c(Na+)=3c(CO32-)+3c(HCO3-)+3c(H2CO3),故正确;
C.Na2C2O4溶液与HCl溶液等体积混合(H2C2O4是二元弱酸)生成等物质的量浓度的NaHC2O4和NaCl,溶液中存在电荷守恒为:2c(C2O42-)+c(HC2O4-)+c(OH-)+c(Cl-)=c(Na+)+c(H+),故C正确;
D.0.1mol/LNH4Cl与0.1mol/L氨水溶液等体积混合,溶液显碱性,NH3•H2O的电离程度大于NH4+的水解程度,所以溶液中c(NH4+)>c(Cl-)>c(NH3•H2O)>c(OH-),故D错误.
故选D.
点评 本题考查了混合溶液中离子浓度大小比较,题目难度中等,注意把握弱电解质的电离和盐的水解、以及电荷守恒和物料守恒的应用,侧重于考查学生的分析能力.


 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 若反应A(s)=B(s);△H<O,则说明A物质比B物质稳定 | |
| B. | Zn(s)+CuSO4 (aq)═ZnSO4 (aq)+Cu(s);△H=-216kJ•mol-1.则反应物总能量<生成物总能量 | |
| C. | 101kPa时,2H2(g)+O2(g)═2H2O(l);△H=-QkJ•mol-1,则H2的燃烧热为$\frac{1}{2}$QkJ•mol-l | |
| D. | H+(aq)+OH- (aq)=H2O(l);△H=-57.3 kJ•mol-1,含1mol NaOH的氢氧化钠溶液与含0.5mol H2SO4的浓硫酸混合后放出57.3kJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将少量的两种白色固体分别加入1 mol/L的盐酸中,看有无气泡产生 | |
| B. | 分别取样在试管中加热,将可能产生的气体通入澄清石灰水,观察有无白色浑浊 | |
| C. | 分别取样配成溶液,滴加BaCl2溶液,观察有无白色沉淀 | |
| D. | 分别配成溶液,用铂丝蘸取溶液在酒精灯火焰上灼烧,观察火焰的颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放射元素 | B. | ⅦA族元素 | C. | 卤化银 | D. | ⅠA族元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| pH | 6.5~6.8 |
| Ca2+、Mg2+总浓度 | <0.0045mol/L |
| 细菌总数 | <100个/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
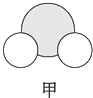 | 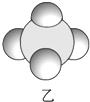 |  |
| 是地球上最常见的物质之一,常温为液态,是包括人类在内所有生命生存的重要资源,也是生物体最重要的组成部分 | 无色,无味且易燃,是21世纪的主要能源 | 弱酸,有强氧化性,可以用于消毒杀菌 |
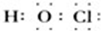 ,丙与SO2水溶液可发生氧化还原反应,生成两种强酸,化学反应方程式为HClO+H2O+SO2=H2SO4+HCl.
,丙与SO2水溶液可发生氧化还原反应,生成两种强酸,化学反应方程式为HClO+H2O+SO2=H2SO4+HCl.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
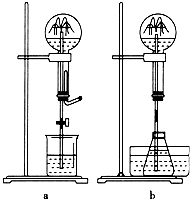 喷泉是一种常见的自然现象,其产生原因通常是装置内外存在压强差.
喷泉是一种常见的自然现象,其产生原因通常是装置内外存在压强差.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com