
下列叙述中正确的是
A.氯化铝溶液中加入过量氨水反应实质是:Al3++3NH3•H2O═Al(OH)3↓+3NH4+
B.存在于污水的重金属离子,常用投加明矾等电解质的方法进行处理
C.镁铝合金既可完全溶于过量盐酸又可完全溶于过量NaOH溶液
D.依据铝热反应原理,能发生反应2Al+3MgO 3Mg+Al2O3
3Mg+Al2O3
科目:高中化学 来源: 题型:解答题
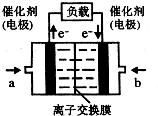 “温室效应”是哥本哈根气候变化大会研究的环境问题之一.CO2是目前大气中含量最高的一种温室气体.因此,控制和治理CO2是解决“温室效应”的有效途径.
“温室效应”是哥本哈根气候变化大会研究的环境问题之一.CO2是目前大气中含量最高的一种温室气体.因此,控制和治理CO2是解决“温室效应”的有效途径.温度(K) CO2转化率(%) $\frac{n({H}_{2})}{n(C{O}_{2})}$ | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
查看答案和解析>>
科目:高中化学 来源:2017届重庆市高三上适应性考试二化学试卷(解析版) 题型:实验题
固体硝酸盐加热易分解且产物较复杂,某学习小组以Fe(NO3)2为研究对象,通过实验探究其热分解的产物,查阅资料,根据硝酸盐受热分解的规律,提出如下4种猜想:
甲:Fe2O3、NO2乙:Fe2O3、NO2、O2丙:Fe3O4、NO2、O2丁:FeO、NO2、N2
(1).实验前,小组成员经讨论认定猜想丁不成立,理由是__________________.
针对上述猜想,设计如图所示的实验装置(图中加热、夹持仪器等均省略):
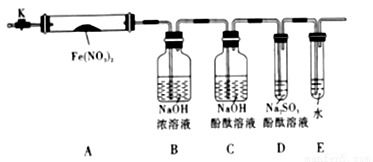
(2).实验过程
①仪器连接后,放人固体试剂之前,应______________
②称取Fe(NO3)2固体3.6g置于A中,加热前先打开K,___________,后再关闭K,用酒精灯加热
③观察到A中有红棕色气体出现,C、D中未见明显变化.
④待样品完全分解,A装置冷却至室温、称量,测得剩余固体的质量为1.6g
⑤取少量剩余固体于试管中,加人适量水,未见明显现象.
(3).实验结果分析讨论:
①根据实验现象和剩余固体的质量经分析,可初步确认分解产物中有____________。
②根据D中无明显现象,一位同学认为不能确认分解产物中有O2,因为若有O2,D中溶液颜色会退去;另一个同学认定分解产物中有O2存在,未检侧到的原因是_________________。
③为了验证是否有O2,某同学另称Fe(NO3)2固体3.6g,充分加热,收集气体,假设产生的气体全部收集,将集满气体的试管倒放在水槽中,观察到的现象是红棕色消失,液面上升,进入试管中的溶液大于2/3,通入一定量的O2后,气体全部被吸收,请写出Fe(NO3)2受热分解的化学方程式______________,通入O2的物质的量为_____________。
④小组讨论后达成的共识是上述实验设计仍不完善,需改进装置进一步研究。写一点不足之处:__________________________。
查看答案和解析>>
科目:高中化学 来源:2017届山西省高三上期中化学试卷(解析版) 题型:选择题
下列有关NH4Fe(SO4)2水溶液的叙述正确的是
A.该溶液中Mg2+、H+、NO3-、Cl-可以大量共存
B.该溶液能使碘化钾试纸变蓝,反应的离子方程式为:Fe3++2I-=Fe2++I2
C.该溶液和足量的Ba(OH)2溶液反应的离子方程式为: Fe3++SO42-+Ba2++3OH-=BaSO4↓+Fe(OH)3↓
D. 该溶液与足量铜粉 反应的离子方程式为:2Fe3++3Cu=2Fe+3Cu2+
查看答案和解析>>
科目:高中化学 来源:2017届山西省高三上期中化学试卷(解析版) 题型:选择题
下列说法中不正确的是
A.SO2使溴水褪色与乙烯使KMnO4溶液褪色的原理相同
B.浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体
C.硅胶可做袋装食品的干燥剂
D.晶体硅可用于制作半导体材料与其熔点高硬度大无关
查看答案和解析>>
科目:高中化学 来源:2017届山西省高三上期中化学试卷(解析版) 题型:选择题
下列叙述正确的是(NA为阿伏加德罗常数的值)
A.7.8gNa2O2含有的共价键数为0.2NA
B.7.8gNa2S与Na2O2的混合物,含离子总数为0.3NA
C.标准状况下,22.4L溴单质含有NA个溴分子
D.0.2 molNa被完全氧化生成7.8gNa2O2,转移电子的数目为0.4NA
查看答案和解析>>
科目:高中化学 来源:2017届山西大学附中高三上10月模块诊断化学试卷(解析版) 题型:推断题
中学化学中几种常见物质的转化关系如图所示(图中部分反应物或生成物及反应条件未列出)。
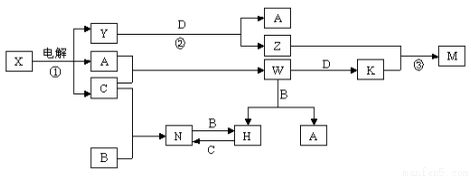
已知:A 、B、C、D是单质,其余是化合物。其中B、D是常见金属。又知A在C中点燃有苍白色火焰,M既可溶于盐酸又可溶于NaOH溶液。请回答下列问题:
、B、C、D是单质,其余是化合物。其中B、D是常见金属。又知A在C中点燃有苍白色火焰,M既可溶于盐酸又可溶于NaOH溶液。请回答下列问题:
(1) W的电子式是____________;Y中含有的化学键类型为____________。
(2)写出N的化学式__________;并任写一种N的主要用途_______________ 。
。
( 3)写出下列反应的离子方程式:
3)写出下列反应的离子方程式:
反应① 。
反应③ 。
查看答案和解析>>
科目:高中化学 来源:2017届山西大学附中高三上10月模块诊断化学试卷(解析版) 题型:选择题
化学与人类生活、能源开发、资源利用等密切相关。下列说法正确的是 ( )
A.家中做卫生保洁时,可将漂白粉与洁厕精(含浓盐酸)混合使用
B.Na2O2可作漂白剂和供氧剂,碳酸钠可用于 治疗胃酸过多
治疗胃酸过多
C.可以用湿润的碘化钾淀粉试纸鉴别Br2(g)和NO2(g)
D.施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用
查看答案和解析>>
科目:高中化学 来源:2016-2017学年海南省琼海市高一上学期第一次月考化学试卷 题型:选择题
下列实验操作中不正确的是
A. CO气体有毒,处理CO气体时可以将其点燃,转化为无毒的CO2
B. 在盛有O2的集气瓶中进行铁丝燃烧实验时,事先在集气瓶底部放一些水
C. 稀释浓硫酸时,先在量筒中加入一定量的水,再慢慢地加入浓硫酸并搅拌
D. 给试管内的液体加热时,试管口不能对着他人或自己
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com