
| A. | 推广使用氢能、太阳能,减少化石燃料的使用,有助于减少雾霾天气的发生 | |
| B. | 将太阳能转化为氢能是减少污染、缓解能源危机的一种构想 | |
| C. | 石油的分馏、催化裂化、裂解等石油的加工方法,其目的均为得到更多的汽油 | |
| D. | 煤干馏可以得到煤焦油,煤焦油进一步分离又可得到苯、甲苯等有机物 |
分析 A.化石燃料的使用,能够产生大量灰尘等空气污染物而引起雾霾天气;
B.氢气燃烧生成水,不会造成环境污染;
C.裂解的目的是得到小分子的烯烃;
D.煤的干馏能制得苯及其同系物.
解答 解:A.推广使用氢能、太阳能,减少化石燃料的使用,能够减少灰尘等空气污染物的排放,有利于减少雾霾天气的发生,故A正确;
B.氢能是一种清洁可再生能源,将太阳能转化为氢能是减少污染、缓解能源危机的一种构想,故B正确;
C.石油裂解的目的是得到小分子的烯烃,故C错误;
D.煤的干馏是指在隔绝空气条件下加热、分解,生成焦炭(或半焦)、煤焦油、粗苯、煤气等产物的过程,煤的干馏能制得苯及其同系物,故D正确;
故选:C.
点评 本题考查了能源的开发与利用,石油的综合利用,熟悉新型能源特点、明确石油不同加工方式产物是解题关键,题目难度不大,注意对相关知识积累.


科目:高中化学 来源: 题型:选择题
| A. | 甲=丙>乙 | B. | 丙>乙>甲 | C. | 乙>丙>甲 | D. | 甲=乙=丙 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO(g)+$\frac{1}{2}$O2(g)═CO2(g);△H=-283.0 kJ/mol | |
| B. | C(s)+$\frac{1}{2}$O2(g)═CO(g);△H=-110.5 kJ/mol | |
| C. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g);△H=-241.8 kJ/mol | |
| D. | 2C8H18(l)+25O2(g)═16CO2(g)+18H2O(l);△H=-11 036 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
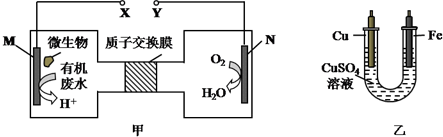
| A. | H+透过质子交换膜由左向右移动 | |
| B. | M电极反应式:H2NCONH2+H2O-6e-═CO2↑+N2↑+6H+ | |
| C. | 铁电极应与X相连接 | |
| D. | 当N电极消耗0.5mol气体时,则铁电极增重32g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,26gC2H2和C6H6的混合物所含原子数为4NA | |
| B. | 标准状况下,11.2LH2O中所含O-H键数目为NA | |
| C. | 1molCl2与足量Fe在点燃条件下发生反应,转移电子数为3NA | |
| D. | 常温下,pH=13的NaOH溶液,OH-离子的数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图,将锥形瓶置于水槽内,瓶中加入酒精.水槽中加入冷水后,再加入足量的下列物质,结果产生了酒精喷泉.水槽中加入的物质可以是( )
如图,将锥形瓶置于水槽内,瓶中加入酒精.水槽中加入冷水后,再加入足量的下列物质,结果产生了酒精喷泉.水槽中加入的物质可以是( )| A. | 生石灰 | B. | 食盐 | C. | 蔗糖 | D. | 固体NH4NO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com