
| 容器 编号 | 起始时各物质物质的量/mol | 达到平衡的时间/min | 达平衡时体系能量的变化/kJ | |||
| CO | H2O | CO2 | H2 | |||
| ① | 1 | 4 | 0 | 0 | t1 | 放出热量:32.8 kJ |
| ② | 2 | 8 | 0 | 0 | t2 | 放出热量:Q |
分析 (1)正反应为放热反应,则断键吸收的总能量小于成键放出的总能量;
(2)平衡时放出热量为32.8 kJ,则参加反应的CO为$\frac{32.8kJ}{41kJ/mol}$=0.8mol,进而计算CO转化率;
(3)容器①、②温度相同,平衡常数相同,根据容器①中消耗CO物质的量,计算平衡时各物质的物质的量,反应前后气体体积不变,用物质的量代替浓度代入K=$\frac{c(CO{\;}_{2})×c(H{\;}_{2})}{c(CO)×c(H{\;}_{2}O)}$计算平衡常数;
(4)a.容器①、②中CO、H2O起始物质的量之比均为1:4,反应前后气体体积不变,恒温恒容下二者为等效平衡,平衡时同种物质的含量相等;
b.容器①、②为等效平衡,平衡时CO转化率相等,计算容器②中反应CO的物质的量,结合热化学方程式计算放出的热量;
c.浓度越大,反应速率越快;
d.由方程式可知生成的水的物质的量等于消耗CO物质的量,根据v=$\frac{△c}{△t}$计算v(H2O);
(5)已知:①CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41kJ/mol
②2H2(g)+O2(g)═2H2O (g)△H=-484kJ/mol,
根据盖斯定律,①×2+②可得:2CO(g)+O2(g)﹦2CO2(g).
解答 解:(1)正反应为放热反应,反应物分子化学键断裂时所吸收的总能量小于生成物分子化学键形成时所释放的总能量,
故答案为:小于;
(2)平衡时放出热量为32.8 kJ,则参加反应的CO为$\frac{32.8kJ}{41kJ/mol}$=0.8mol,则CO转化率为$\frac{0.8mol}{1mol}$×100%=80%,
故答案为:80%;
(3)容器①、②温度相同,平衡常数相同,容器①中消耗CO物质的量为0.8mol,则:
CO(g)+H2O(g)═CO2(g)+H2(g)
起始量(mol):1 4 0 0
变化量(mol):0.8 0.8 0.8 0.8
平衡量(mol):0.2 3.2 0.8 0.8
反应前后气体体积不变,用物质的量代替浓度计算平衡常数,则K=$\frac{c(CO{\;}_{2})×c(H{\;}_{2})}{c(CO)×c(H{\;}_{2}O)}$=$\frac{0.8×0.8}{0.2×3.2}$=1,
故答案为:1;
(4)a.容器①、②中CO、H2O起始物质的量之比均为1:4,反应前后气体体积不变,恒温恒容下二者为等效平衡,两容器中H2的体积分数相等,故a正确;
b.容器①、②为等效平衡,平衡时CO转化率相等,容器②中反应CO的物质的量为2mol×80%=1.6mol,放出的热量为1.6mol×41kJ/mol=65.6kJ,故b错误;
c.容器②中反应物起始浓度比①中的大,故容器②中开始反应速率较快,故c错误;
d.由方程式可知生成的水的物质的量等于消耗CO物质的量,则v(H2O)=$\frac{\frac{0.8mol}{VL}}{t{\;}_{1}min}$=$\frac{0.8}{V{t}_{1}}$mol/(L.min),故d错误,
故选:a;
(5)已知:①CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41kJ/mol
②2H2(g)+O2(g)═2H2O (g)△H=-484kJ/mol,
根据盖斯定律,①×2+②可得:2CO(g)+O2(g)﹦2CO2(g)△H=-566 kJ/mol,
故答案为:2CO(g)+O2(g)﹦2CO2(g)△H=-566 kJ/mol.
点评 本题考查化学平衡计算与影响因素、盖斯定律应用、平衡常数等,注意理解效平衡规律:1、恒温恒容,反应前后气体体积不等,按化学计量数转化一边,对应物质满足等量;反应前后气体体积相等,按化学计量数转化一边,对应物质满足等比,2:恒温恒压,按化学计量数转化一边,对应物质满足等比.


科目:高中化学 来源: 题型:选择题
| A. | 全部 | B. | ②③④ | C. | ③④ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg2+、Fe3+、SO42-、I- | B. | Fe2+、H+、Cl-、NO3- | ||
| C. | Na+、Fe3+、HCO3-、Cl- | D. | Mg2+、Fe3+、SO42-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ②④ | C. | ②⑤ | D. | ③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 15% | B. | 20% | C. | 30% | D. | 40% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
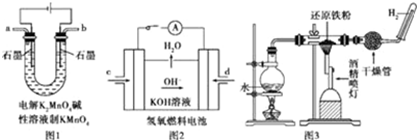
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molN≡N键断裂的同时,有6molN-H键断裂 | |
| B. | 反应器中压强不随时间变化而变化 | |
| C. | v正(NH3)=v逆(H2) | |
| D. | 混合气体平均相对分子质量保持不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com