
����Ŀ���������ȣ�ClNO�������ںϳ�ϴ�Ӽ�����ý�������м��壬ijѧϰС����ʵ������Cl2��NO�Ʊ�ClNO���ⶨ�䴿�ȣ���������ʵ�飨�г�װ����ȥ����

�������ϣ��������ȣ�ClNO�����۵�Ϊ��64.5�桢�е�Ϊ��5.5�棬��̬�ʻ�ɫ��Һ̬ʱ�ʺ��ɫ����ˮ��Ӧ����һ���Ȼ�������ֵ��ij������������һ�ֳʺ���ɫ��
��ش��������⣺
��Cl2���Ʊ������շ��������ķ���������ʵ������ȡ��������Ҫ����֮һ��
��1���÷�������ѡ����ͼ�е�______������ĸ��ţ�ΪCl2����װ�ã��÷�Ӧ�б������뱻��ԭ���ʵ����ʵ���֮��Ϊ____________��
��2�����ռ�һƿ���������������ѡ����ͼ�е�װ�ã�������˳��Ϊ��a��______��i��h��������������Сд��ĸ��ţ���
���������ȣ�ClNO�����Ʊ���ʵ���ҿ�����ͼװ���Ʊ��������ȣ�ClNO����

��3��ʵ����Ҳ����Bװ���Ʊ�NO����Bװ����ȣ�ʹ��Xװ�õ��ŵ�Ϊ___________��
��4����װ��ʵ��װ�ú�Ӧ��________________________��Ȼ��װ��ҩƷ��һ��ʱ�������������Z�з�Ӧ������Ϊ____________________________��
III���������ȣ�ClNO�����ȵIJⶨ���������������ȣ�ClNO����Ʒ13.10 g����ˮ�����Ƴ�250 mL��Һ��ȡ��25.00 mL����K2CrO4��ҺΪָʾ������0.8 mol��L��1AgNO3����Һ�ζ����յ㣬���ı���Һ�����Ϊ 22.50 mL������֪��Ag2CrO4Ϊש��ɫ���壩
��5���������ȣ�ClNO����ˮ��Ӧ�����ӷ���ʽΪ__________________________��
��6���ζ��յ��������________________________________________��
��7���������ȣ�ClNO������������Ϊ____________��
���𰸡�C 2��1 g��f��e��d��c��b �ų�װ���ڿ����ĸ��ţ������濪���ã������ͣ ���װ�õ������� ���ֺ��ɫҺ�� 2ClNO + H2O == 2H+ + 2Cl- + NO��+ NO2�� �������һ�α�Һ����ש��ɫ�������Ұ��������ɫ�ޱ仯 90%
��������
��1��ʵ���Ʊ�������ԭ����MnO2��Ũ���ᣬ������Ӧ����ʽΪMnO2��4HCl(Ũ)![]() MnCl2��Cl2����2H2O�������Ҫ�Ʊ�������װ��ΪC�������Ʊ���������ʽ��MnO2Ϊ��������һ��HClΪ��ԭ����һ��HCl�����ԣ���������HCl��MnO2���ʵ���֮��Ϊ2��1��
MnCl2��Cl2����2H2O�������Ҫ�Ʊ�������װ��ΪC�������Ʊ���������ʽ��MnO2Ϊ��������һ��HClΪ��ԭ����һ��HCl�����ԣ���������HCl��MnO2���ʵ���֮��Ϊ2��1��
��2��װ��C�Ʊ�Cl2���Ʊ�Cl2�л���HCl��H2O(g)���õ������������������ͨ������ʳ��ˮ��Ȼ��ͨ��Ũ���ᣬͨ��ϴ��ƿ�����̳����ռ��������������ܶȴ��ڿ������������ſ������ռ����������ж������β����������˲�����a�� g��f��e��d��c��b��i��h��
��3��NO���������O2������Ӧ���õ�NO2�����װ��X��װ��B����ŵ����ų�װ���ڿ����ĸ��ţ������濪���ã������ͣ��
��4���Ʊ����壬��װ��ʵ��װ�ú���Ҫ�ȼ���װ�õ������ԣ���ʵ��Ŀ�����Ʊ�ClNO��ClNO������ΪҺ�壬�ʺ��ɫ�����װ��Z�з�Ӧ�����dz��ֺ��ɫҺ�壻
��5��ClNO��ˮ��Ӧ����һ���Ȼ�������ֵ��ij������������һ�ֳʺ���ɫ�������ֵ���������ΪNO��NO2������ԭ���غ㣬�Ȼ�����HCl������Ӧ�����ӷ���ʽΪ2ClNO + H2O 2H�� + 2Cl�� + NO��+ NO2����
��6��K2CrO4Ϊָʾ����Ag2CrO4Ϊש��ɫ���壬��˵ζ��յ�������Ǽ������һ�α�Һ����ש��ɫ��������30s����������ɫ�ޱ仯��
��7��ClNO��ˮ��Ӧ����ʽ2ClNO + H2O=2H�� + 2Cl�� + NO��+ NO2�����μ�����������Cl����Ag��=AgCl����������ϵʽΪClNO��Cl����AgCl��ClNO������������![]() =90%��
=90%��


 ��һ������ĩ�ٷֳ�̾�ϵ�д�
��һ������ĩ�ٷֳ�̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ�������й�������ȷ����
A. ���³�ѹ�£�30g���������������еĹ��ۼ���ĿΪ6NA
B. �����£�100mL0.1mol/L NH4Cl��Һ�к���NH4+��ĿΪ0.01NA
C. 1molFe�ֱ���������ϡ�����ϡ���ᷴӦת�Ƶ�������Ϊ2 NA
D. 0.1molH2��0.1molI2���ܱ������г�ַ�Ӧ�����������Ϊ0.2 NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���Ԫ�����ڱ�����������ȷ����
A. Ԫ�������������ǵڢ�B��B. �ڢ�A��Ԫ�ص��ʾ�����ˮ��Ӧ
C. �ڢ�A�����ǽ���Ԫ��D. Ԫ�����ڱ��н���Ԫ�ص�����ȷǽ���Ԫ�ض�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯�����У�û�л�ѧ�����ѻ����ɵ��ǣ� ��
A. ���ʯת��ΪʯīB. �Ȼ��ƾ�������ˮ
C. HCl����ˮD. ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У��Ⱥ������Ӽ����ֺ��зǼ��Թ��ۼ����ǣ� ��
A. K2O2B. NaOHC. MgCl2D. H2O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܸ߷���I��һ�ֺϳ�·�����£�����D����Na��Ӧ����H2����D�����ϵ�һ�ȴ�����2�֡�
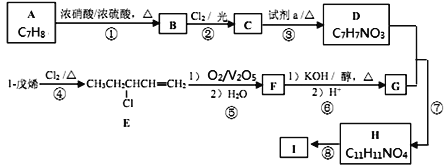
��֪��![]()
�ش��������⣺
��1��A������Ϊ________���Լ�aΪ________________��
��2��C�Ľṹ��ʽΪ________________________��
��3��F�еĹ���������Ϊ________��
��4������������ķ�Ӧ�У�������ȡ����Ӧ����________�������ֱ�ţ���д����Ӧ�ߵĻ�ѧ����ʽ________________________________________��
��5����������������B��ͬ���칹����________�֡�
�ٱ������а�������NH2�� ���ܷ���������Ӧ
���к˴Ź���������4��壬�ҷ������Ϊ2��2��2��1�Ľṹ��ʽΪ__________��
��6�����������ϳ�·�ߣ���1-��ϩΪԭ�ϣ����Լ���ѡ��������Ʊ���ϩ��(CH2=CHCOOH)�ĺϳ�·��________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ϩΪ�л�ԭ���Ʊ����������ĺϳ�·���У����һ����ѧ��Ӧ�ķ�Ӧ�����ǣ� ��
A.������ӦB.������ӦC.�ӳɷ�ӦD.ˮ�ⷴӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڻ�ѧ��ӦC(s)��O2(g) =CO2(g)��˵�������й�˵������ȷ���ǣ� ��
A. ����ľ̿�����ʵ�������ѧ��Ӧ���ʻ�ӿ�
B. �����¶ȣ���ѧ��Ӧ���ʻ�ӿ�
C. ����Ӧ�����������С����ѧ��Ӧ���ʻ�ӿ�
D. ��ľ̿����ɷ�ĩ״����ѧ��Ӧ���ʻ�ӿ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����Zn(s)��![]() O2(g)��ZnO(s)��H����348.3kJ��mol��1
O2(g)��ZnO(s)��H����348.3kJ��mol��1
��2Ag(s)��![]() O2(g)��Ag2O(s)��H����31.0kJ��mol��1
O2(g)��Ag2O(s)��H����31.0kJ��mol��1
��Zn��Ag2O��Ӧ����ZnO��Ag���Ȼ�ѧ����ʽΪ
A. 2Zn(s)��2Ag2O(s)===2ZnO(s)��4Ag(s)��H����634.6 kJ��mol��1
B. Zn��Ag2O===ZnO��2Ag����H����317.3kJ��mol��1
C. Zn(s)��Ag2O(s)===ZnO(s)��2Ag(s)��H����317.3kJ
D. Zn(s)��Ag2O(s)===ZnO(s)��2Ag(s)��H����317.3kJ��mol��1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com