
| A. | 实验桌上的酒精灯倾倒了燃烧起来,马上用水扑灭 | |
| B. | 不慎将酸或碱液溅入眼内,立即闭上眼睛,用手揉擦 | |
| C. | 皮肤上溅有较多的浓硫酸,赶紧用水冲洗 | |
| D. | 分液时,下层液体从下端放出,上层液体从上口倒出 |
分析 A.根据灭火的原理和方法判断;
B.如果药液不慎溅入眼中或皮肤上,应立即用大量清水冲洗;
C.浓硫酸溶于水放出大量的热;
D.分液漏斗下层液体从下口放出,上层液体从上口倒出.
解答 解:A.当酒精洒在桌面上并着火燃烧时,应用湿抹布扑盖,不能泼水,因为酒精和水互溶,故A错误;
B.应该用干抹布迅速擦去,然后再用大量的水冲洗,故B错误;
C.浓硫酸溶于水放出大量的热,并有强烈的腐蚀性,浓硫酸沾到皮肤或衣服上,应先用布试去,再用大量水冲洗,然后涂上3%~5%的碳酸氢钠溶液,故C错误;
D.分液时,为不产生杂质,分液漏斗下层液体从下口放出,上层液体从上口倒出,故D正确.
故选D.
点评 本题考查化学实验室安全及事故处理,该题是基础性试题的考查,难度不大,侧重对学生实验基础知识的检验和训练,有利于培养学生的实验能力.在实验过程中应学会处理常见意外事故的方法技巧.


科目:高中化学 来源: 题型:选择题
| A. | 同温同压下,体积相同的氢气和氩气所含的分子数相等 | |
| B. | 标准状况下22.4 L乙醇中分子数为NA | |
| C. | 在1 L 2 mol/L的盐酸中,存在2NA个氯化氢分子 | |
| D. | 1.8g的NH4+中含有的电子数为1.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸溶液与氢氧化钡溶液混合:SO${\;}_{4}^{2-}$+Ba2+═BaSO4↓ | |
| B. | 氯化钙溶液中通入CO2气体:Ca2++CO2+H2O═CaCO3↓+2H+ | |
| C. | 硫酸铜溶液中加入烧碱溶液:Cu2++2OH-═Cu(OH)2↓ | |
| D. | 碳酸钙固体上滴加醋酸溶液:CO${\;}_{3}^{2-}$+2H+═CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
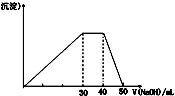 学习化学要准确掌握化学基本概念和研究方法.按要求回答下列问题:
学习化学要准确掌握化学基本概念和研究方法.按要求回答下列问题:| | 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 |
| 第一组 | Na2CO3 | H2SO4 | NaHCO3 | CaO | CO2 |
| 第二组 | NaOH | HCl | NaCl | Na2O | SO2 |
| 第三组 | NaOH | CH3COOH | CaF2 | Al2O3 | SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A配置0.10mol/LNaOH溶液 | B.除去CO中的CO2 | C.苯萃取碘水中的I2分出水层后的操作 | D.记录滴定终点读数为12.20mL |
 |  |  |  |
| A. | 配制0.10mol/L NaOH溶液 | |
| B. | 除去CO中的CO2 | |
| C. | 苯萃取碘水中的I2分出水层后的操作 | |
| D. | 记录滴定终点读数为12.20mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com