
��������������ɴ���ʹ�õ�����ȼ�ϵ����һ�����͵Ļ�ѧ��Դ������ȼ�ϵ�ص�ͻ���ŵ��ǰѻ�ѧ��ֱ��ת��Ϊ���ܣ��������������м��γɣ������ķ�ӦΪ��2H2+O2 2H2O
2H2O
��1����ͨ��Ӧ��H2��������ӦʽΪ ������ӦʽΪ ��
��2�����KOH��Ϊϡ�������������ʣ�����ӦʽΪ ��
��3�����H2��ΪCH4��KOH���������ʣ�����ӦʽΪ ��
��4��д�����Ե缫���������Һ���ܷ�Ӧ�Ļ�ѧ����ʽ
��NaCl��Һ
��CuSO4��Һ
���㣺 ԭ��غ͵��صĹ���ԭ����
������ ��1������ȼ�ϼ��Ե���У�������ȼ��ʧ���Ӻ����������ӷ�Ӧ����ˮ�������������õ��Ӻ�ˮ��Ӧ�������������ӣ�
��2������ȼ�����Ե���У�������ȼ��ʧ�������������ӣ������������õ��Ӻ������ӷ�Ӧ����ˮ��
��3������ȼ�ϼ��Ե���У������ϼ���ʧ���Ӻ����������ӷ�Ӧ����̼������Ӻ�ˮ��
��4���ٵ��NaCl��Һʱ�����������ӵõ��ӣ�������������ʧ���ӣ�
�ڵ��CuSO4��Һʱ�����������ӵõ��ӣ�����������������ʧ���ӣ�
��� �⣺��1������ȼ�ϼ��Ե���У�������ȼ��ʧ���Ӻ����������ӷ�Ӧ����ˮ��������ӦΪH2+2OH﹣﹣2e﹣=2H2O�������������õ��Ӻ�ˮ��Ӧ�������������ӣ�������ӦΪO2+2H2O+4e﹣=4 OH﹣���ʴ�Ϊ��H2+2OH﹣﹣2e﹣=2H2O�� O2+2H2O+4e﹣=4 OH﹣��
��2������ȼ�����Ե���У�������ȼ��ʧ�������������ӣ��缫��ӦʽΪH2﹣2e﹣=2H+���ʴ�Ϊ��H2﹣2e﹣=2H+��
��3������ȼ�ϼ��Ե���У������ϼ���ʧ���Ӻ����������ӷ�Ӧ����̼������Ӻ�ˮ���缫��ӦʽΪCH4+10OH﹣﹣8e﹣=7H2O+CO32﹣��
�ʴ�Ϊ��CH4+10OH﹣﹣8e﹣=7H2O+CO32﹣��
��4���ٵ��NaCl��Һʱ�����������ӵõ��ӣ�������������ʧ���ӣ���缫����ʽΪ��2NaCl+2H2O H2��+Cl2��+2NaOH��
H2��+Cl2��+2NaOH��
�ʴ�Ϊ��2NaCl+2H2O H2��+Cl2��+2NaOH��
H2��+Cl2��+2NaOH��
�ڵ��CuSO4��Һʱ�����������ӵõ��ӣ�����������������ʧ���ӣ����ⷽ��ʽΪ��2CuSO4+2H2O 2Cu+O2��+2H2SO4��
2Cu+O2��+2H2SO4��
�ʴ�Ϊ��2CuSO4+2H2O 2Cu+O2��+2H2SO4��
2Cu+O2��+2H2SO4��
������ ���⿼���˵缫��Ӧʽ��д�������������ϵ�ʧ������д�缫��Ӧʽ��ע��Ҫ��ϵ������Һ�������д��ע�⣺���Ե������Һ�в������������ӡ����Ե������Һ�в������������ӣ�Ϊ�״��㣮


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
3.84gFe��Fe2O3�Ļ�������ڹ��������У�����0.03molH2����Ӧ�����Һ�м���KSCN���飬��Һ������������ԭ�������Fe2O3��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������ȷ���ǣ���
A�� ��ҵ�ϵ�����ڵ�Al2O3ұ��������������
B�� �ö��Ե缫���Na2SO4��Һ��������������������ʵ���֮��Ϊ1��2
C�� �ö��Ե缫��ⱥ��NaCl��Һ������1mol����ת�ƣ�������1mol NaOH
D�� �ö��Ե缫���ŨCuSO4��ҺһС��ʱ�����Cu2O�������ʹCuSO4��Һ�ָ�ԭ��Ũ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������ı仯������Ϊ���ͷ�Ӧ��������������ӵ�λ����ڵķ�Ӧ�����Ӱٷ�����ʹ��Ӧ���ʼӿ���ǣ���
A�� ����Ũ�� B�� ����ѹǿ C�� �����¶� D�� ʹ�ô���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����йػ�ѧ��Ӧ���ʵ�˵����ȷ���ǣ���
A�� ����Ƭ��ϡ���ᷴӦ��ȡ����ʱ������98%��Ũ������Լӿ��������������
B�� 100mL2mol•L﹣1�������пƬ��Ӧ�������������Ȼ�����Һ����Ӧ���ʲ���
C�� SO2�Ĵ�������һ�����ȵķ�Ӧ�����������¶ȣ���Ӧ���ʼ���
D�� ����β���е�NO��CO���Ի�����Ӧ����N2��CO2����Сѹǿ��Ӧ���ʼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪��ͪ��C3H6O��ͨ������ɫҺ�壬������ˮ���ܶ�С��1 g•mL﹣1���е�ԼΪ55�森Ҫ��ˮ���ͪ�Ļ�����н���ͪ������������з�������Ϊ�������ǣ���
A�� ���� B�� ��Һ C�� ���� D�� ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
0.5L 1mol/L FeCl3��Һ�е�Cl﹣�����ʵ���Ũ��Ϊ����
A�� 3 mol/L B�� 1.5 mol/L C�� 1 mol/L D�� 0.5 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ȡ1.43g Na2CO3•10H2O����ˮ���100mL��Һ����
��1��Na2CO3��Һ�����ʵ���Ũ��
��2��Na+���ʵ���Ũ��
��3��ȡ��20ml����Һ��ˮϡ�ͣ�ʹNa2CO3��Һ�����ʵ���Ũ�ȱ�Ϊ0.004mol/L�������ˮ���������ϡ��ʱ������Һ�����Ӱ����Բ��ƣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͼ��ʾװ���У��۲쵽������ָ��ƫת��M����֣�N����ϸ���ɴ��ж��±�������M��N��P���ʣ����п��Գ������ǣ���
M N P
A п ͭ ϡ������Һ
B ͭ �� ϡ����
C �� п ��������Һ
D п �� ��������Һ
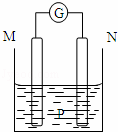
A�� A B�� B C�� C D�� D
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com