
����Ŀ�������£���a mol N2��b mol H2�Ļ������ͨ��һ���̶��ݻ����ܱ������У��������·�Ӧ��N2 (g) �� 3 H2(g) ![]() 2NH3(g)��
2NH3(g)��
��1������Ӧijʱ��tʱ��n t (N2) = 13 mol��n t (NH3) = 6 mol����a =____mol��
��2����Ӧ��ƽ��ʱ�������������Ϊ716.8 L������£�������NH3�ĺ���(�������)Ϊ25%��ƽ��ʱNH3�����ʵ���_____��
��3��ԭ���������ƽ��������������ʵ���֮�ȣ�д����������ȡ���ͬ����n(ʼ)��n(ƽ) =______��
��4��ԭ��������У�a��b =_____��
��5���ﵽƽ��ʱ��N2��H2��ת����֮�ȣ���(N2)�æ�(H2)= ______��
��6��ƽ���������У�n(N2)��n(H2)��n(NH3) =______��
���𰸡�16 mol 8 mol 5��4 2��3 1��2 3��3��2
��������
��1�����ݻ�ѧ����ʽ����aֵ��
��2����Ӧ��ƽ��ʱ�������������Ϊ716.8 L������£�������������ʵ�����![]() 32mol������NH3�ĺ���(�������)Ϊ25%���㰱�������ʵ�����
32mol������NH3�ĺ���(�������)Ϊ25%���㰱�������ʵ�����
��3�����ò���������ԭ�����������ʵ�����
��4�����ݣ�1����֪a=16�����ݣ�3����֪ԭ�����������ʵ�����40mol��
��5�����á�����ʽ������N2��H2��ת����֮�ȣ�
��6�����ݡ�����ʽ���ж�ƽ���������и���������ʵ����ȣ�
��1������N2 (g)�� 3H2(g)![]() 2NH3(g)��Ӧ����֪����Ӧijʱ��tʱ��n (NH3) = 6 mol��������n (N2) =3 mol����ʼ����n (N2)= 13mol+ 3mol =16mol��
2NH3(g)��Ӧ����֪����Ӧijʱ��tʱ��n (NH3) = 6 mol��������n (N2) =3 mol����ʼ����n (N2)= 13mol+ 3mol =16mol��
��2����Ӧ��ƽ��ʱ�������������Ϊ716.8 L������£�������������ʵ�����![]() 32mol��NH3�ĺ���(�������)Ϊ25%�������������ʵ�����32mol��25%=8mol��
32mol��NH3�ĺ���(�������)Ϊ25%�������������ʵ�����32mol��25%=8mol��
��3���跴Ӧ���������ʵ�������n��
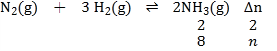
n=![]() 8mol������ԭ�����������ʵ�����32mol+8mol=40mol��ԭ���������ƽ��������������ʵ���֮��40:32=5:4��
8mol������ԭ�����������ʵ�����32mol+8mol=40mol��ԭ���������ƽ��������������ʵ���֮��40:32=5:4��
��4�����ݣ�1����֪a=16�����ݣ�3����֪ԭ�����������ʵ�����40mol������b=40mol-16mol=24mol��a��b =16:24=2:3��
��5��
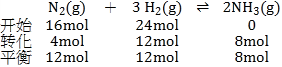
N2��ת����Ϊ![]() ��H2��ת����Ϊ
��H2��ת����Ϊ![]() ��������(N2)����(H2)=1:2��
��������(N2)����(H2)=1:2��
��5������
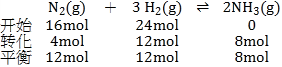
ƽ���������У�n(N2)��n(H2)��n(NH3) =12:12:8=3:3:2��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij�ܱ������м��� 0.3 mol A��0.1 mol C ��һ������ B �������壬 һ�������·������·�Ӧ�� 3A(g) ![]() B(g)��2C(g)�������ʵ�Ũ����ʱ��仯��ͼ��ʾ[t0��t1 �ε� c(B)�仯δ����]������˵������ȷ����( )
B(g)��2C(g)�������ʵ�Ũ����ʱ��仯��ͼ��ʾ[t0��t1 �ε� c(B)�仯δ����]������˵������ȷ����( )

A. �� t1��15 s������ A ��Ũ�ȱ仯��ʾ t0��t1�ε�ƽ����Ӧ����Ϊ 0.004 mol��L��1��s��1
B. t1ʱ�÷�Ӧ�ﵽƽ�⣬ A ��ת����Ϊ 60%
C. ���������ݻ�Ϊ2 L��B����ʼ�����ʵ���Ϊ 0.02 mol
D. t0��t1 �Σ� �˹����������������Ƚ�������Ϊ a kJ���÷�Ӧ���Ȼ�ѧ����ʽΪ 3A(g)![]() B(g)��2C(g) ��H����50a kJ��mol��1
B(g)��2C(g) ��H����50a kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���A��D������Ҫ���л��ϳ��м��壬D����Ϊ��ζ��![]() ���������ⷼ���Һ�壬Ҳ��ֱ����ũҩʹ�á���ͼ��ʾ�����ɱ���Ϊԭ�Ϻϳ�A��D�����̣�
���������ⷼ���Һ�壬Ҳ��ֱ����ũҩʹ�á���ͼ��ʾ�����ɱ���Ϊԭ�Ϻϳ�A��D�����̣�
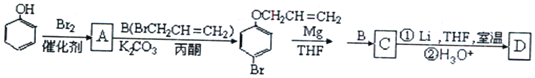
��֪��
��BrR1![]() BrMR1
BrMR1![]() R1��R2(THFΪһ���л��ܼ�)
R1��R2(THFΪһ���л��ܼ�)
��C6H5��O��R![]() C6H5��OH
C6H5��OH
��ش��������⣺
(1)д��A��C�Ľṹ��ʽ ______��______��
(2)![]() �ǻ�����B��һ��ͬ���칹�壬�ú˴Ź���������֤���û���������______ ����ڲ�ͬ�Ļ�ѧ������
�ǻ�����B��һ��ͬ���칹�壬�ú˴Ź���������֤���û���������______ ����ڲ�ͬ�Ļ�ѧ������
(3)ָ��![]() ���л���Ӧ���� ______��
���л���Ӧ���� ______��
(4)������B��������ת�����ɺϳ�����������֬���ϳ�����Һ���л�ԭ�ϱ�ϩ�
B![]() E
E ![]() F
F![]()
![]()
![]()
![]() G
G
�����÷�Ӧ�ڡ���Ŀ���� ______��
��д����Ӧ�۵Ļ�ѧ��Ӧ����ʽ ______��
��д����Ӧ�ܵĻ�ѧ��Ӧ����ʽ ______��
��G��״���Ӧ���ɵ���H��������ϩ����֬��һ����Ҫ���壬д��H�ۺϵĻ�ѧ��Ӧ����ʽ _________________��
(5)д����������Ҫ��Ļ�����D������ͬ���칹��Ľṹ��ʽ______________��
����FeCl3��Һ����ɫ��
�ڱ�����������ȡ�������ұ����ϵ�һ�ȴ��������֡�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ɽ����ٴ���ż����Ӧ�ǽ������л��ϳɵ��ȵ�֮һ���練Ӧ����

������II�������ºϳ�·��ã�

��1��������I���������ŵ�����Ϊ______________��������II�ķ���ʽΪ_____________��
��2��������IV�Ľṹ��ʽΪ______________________��ijͬѧ�������辭��Ӧ����������������ֱ��������KMnO4��Һ�Ϳɽ�������III����Ϊ������VII�����������Բ���������������__________________________________________________________��
��3��������VII�ж���ͬ���칹�壬��д��һ�ַ�������Ҫ��Ľṹ��ʽ____________��
i��������������ȡ����
ii��1 mol �����ʷ���������Ӧ������4 mol Ag
��4����Ӧ���Ļ�ѧ����ʽΪ________________________________________����ע��������
��5��������![]() �뻯����
�뻯����![]() ��һ�������°����ʵ���֮��1��2�ɷ������Ʒ�Ӧ���ķ�Ӧ����д�������Ľṹ��ʽ________________________________��
��һ�������°����ʵ���֮��1��2�ɷ������Ʒ�Ӧ���ķ�Ӧ����д�������Ľṹ��ʽ________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ��С������ͼ��ʾװ�ý���ʵ����̽��Fe3+��Cl2��SO2��������ǿ��(�г���������)��
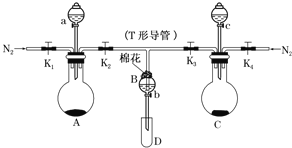
��1����ͼ���Ӻ�װ�ã����Aװ�õ������Եķ���Ϊ___��
��2�������װ�õ������ԣ�����ҩƷ����Aװ�õķ�Һ©���м���Ũ���ᣬ��Բ����ƿ�м������KMnO4����Bװ���м���10mLFeCl2��Һ����Cװ�õķ�Һ©���м���70%�����ᣬ��Բ����ƿ�м������Na2SO3��������___��Һ�����ɼ�K1��K4��ͨ��һ��ʱ��N2���ٽ�T�ε��ܲ���B�У�����ͨ��N2��Ȼ��ر�K1��K3��K4��ͨ��һ��ʱ��N2��Ŀ����___��
��3������a����μ���Ũ���ᣬ��B����Һ��Ϊ�ػ�ɫʱ��ֹͣ�μ�Ũ���ᣬ�н�K2������b��ʹԼ2mL����Һ����D�Թ��У��ֱ�ȡ1mL��Һ����___(���Լ�����)�����軯����Һ����֤�����к���Fe3+��Fe2+��Aװ���з�����Ӧ�����ӷ���ʽΪ___��
��4����K3�ͻ���c����μ���70%�����ᣬ��B����Һ��ɫ��Ϊ___ɫ��ֹͣ�μ�70%�����ᣬ�н�K3������b��ʹԼ2mL����Һ����D�Թ��У����������е����ӡ�B�з�����Ӧ�����ӷ���ʽΪ___��
��5�����ʵ�������ж�Fe3+��Cl2��SO2������������ǿ��˳��Ϊ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о���ͭ������Cu��Sn�ȣ��ڳ�ʪ�����з����ĸ�ʴ�������ﱣ����������Ҫ���塣��ͼΪ��ͭ���ڳ�ʪ�����з����绯ѧ��ʴ��ԭ��ʾ��ͼ������˵������ȷ����
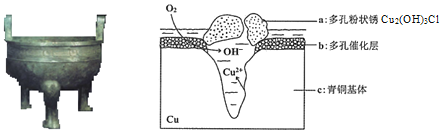
A.��ͭ������������ʴ��ͼ��c��������������
B.���������ĵ缫��ӦΪO2+ 4e��+2H2O=4OH��
C.������0.2 mol Cu2(OH)3Cl�������������ĵ�O2���Ϊ4.48L
D.�����е�Cl����缫��������a�����ӷ���ʽΪ2Cu2��+3OH��+Cl��=Cu2 (OH)3Cl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A����Ȼ�л��߷��ӻ����D��һ����Ҫ�Ļ���ԭ�ϣ�����ͬ�����£�G�������ܶ���E��2��������֮���ת����ϵ��ͼ��
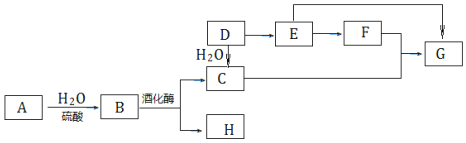
(1)���F����������������______��
(2)�������Ϊ������E����������G���÷�Ӧ�Ļ�ѧ����ʽ��______��
(3)����Aת����������B���ɣ����к�ˮ��Һ�����������Լ���______��
(4)����˵������ȷ����______��
A.����ת����ϵ���мӳɷ�Ӧ��ȡ����Ӧ��������Ӧ
B.�л���B��C��D��E����ʹ����KMnO4��Һ��ɫ
C.�л���C��F��ŨH2SO4�����¿����Ƶ�G���÷�Ӧ��ŨH2SO4�Ǵ�������ˮ��
D.ij��X����Է���������D��H֮�ͣ���X������ˮ�����ӳɷ�Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����NaHCO3��Һ�е������ᣬ�����Һ��pH������Ũ�ȱ仯�Ĺ�ϵ��ͼ��ʾ����������������ǣ� ��
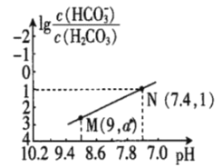
A.25��ʱ��H2CO3��һ������K(H2CO3)=1.0��10-6.4
B.ͼ��a=2.6
C.25��ʱ��HCO3-+H2O![]() H2CO3+OH-��Kh=1.0��10-7.6
H2CO3+OH-��Kh=1.0��10-7.6
D.M����Һ�У�c(H+)+c(H2CO3)=c(Cl-)+2c(CO32-)+c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯�У����屻��ԭ����
A.ˮ����ʹ CuSO4�������B.����ʹdz��ɫ FeC12 ��Һ���
C.H2ʹ����CuO ������D.����ʹA1Cl3��Һ������ɫ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com