
【题目】已知溶液中:还原性HSO3―>I―,氧化性IO3―>I2>>SO32―。向含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如下图所示,下列说法正确的是
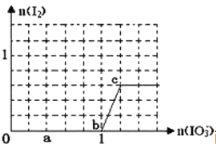
A.a点反应的还原剂是NaHSO3,被氧化的元素是碘元素
B.b点反应的离子方程式是:3HSO3-+IO3-+3OH-=3SO42-+I-+3H2O
C.c点到d点的反应中共转移0.6mol电子
D.往200ml 1mol/LKIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式是:
5HSO3-+2IO3-=I2+5SO42-+3H++H2O
【答案】D
【解析】
试题分析:还原性HSO-3>I-,所以首先是发生以下反应离子方程式:IO3-+3HSO3-═I-+3SO42-+3H+,继续加入KIO3,氧化性IO-3>I2,所以IO3-可以结合H+氧化I-生成I2,离子方程式是IO3-+6H++5I-═3H2O+3I2。A.a点反应离子方程式为:3HSO3-+IO3-═3SO42-+I-+3H+,还原剂是NaHSO3,被氧化的元素是S元素,故A错误;B.b点反应的离子方程式是:3HSO3-+IO3-═3SO42-+I-+3H+,故B错误;C.c点到d点的反应离子方程式是IO3-+6H++5I-═3H2O+3I2,反应中生成0.3molI2,则转移电子为0.5mol,故C错误;D.往200mL 1 mol/L的KIO3溶液中滴加NaHSO3溶液,生成硫酸钠和单质碘,发生的反应为:5HSO3-+2IO3-═I2+5SO42-+3H++H2O,故D正确;故选D。


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:
【题目】I、今有A.醋酸,B.盐酸,C.硫酸三种酸,请用三种酸的序号和“>”“<”或“=”填空。
(1)在同体积,同pH的三种酸中,分别加入足量的NaHCO3粉末,在相同条件下产生CO2的体积由大到小的顺序是 。
(2)物质的量浓度均为0.1 mol/L的三种酸溶液的pH由大到小的顺序是 ;如果取等体积的0.1 mol/L的三种酸溶液,用0.1 mol/L的NaOH中和,当恰好完全反应时,消耗NaOH溶液的体积由大到小的顺序是 。
II、用实验确定某酸HB的弱电解质。两同学的方案是:
甲:①称取一定质量的HB配制0.1mol/L的溶液100mL;
②用pH试纸测出该溶液的pH值,即可证明HB是弱电解质。
乙:①用已知物质的量浓度的HB溶液、盐酸,分别配制pH = 1的两种酸溶液各100mL;
②分别取这两种溶液各10mL,加水稀释为100mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HB是弱电解质。
(1)甲方案中,说明HB是弱电解质的理由是测得溶液的pH 1(选填>、<、=)
(2)请你评价乙方案中难以实现之处和不妥之处: 。
III、硼酸(H3BO3)是生产其它硼化物的基本原料。已知H3BO3的电离常数为5.8×10-10,H2CO3的电离常数为K1=4.4×10-7、K2=4.7×10-11。向盛有饱和硼酸溶液的试管中,滴加0.1 mol/LNa2CO3溶液, (填“能”或“不能”)观察到气泡逸出。
已知H3BO3与足量NaOH溶液反应的离子方程式为H3BO3+OH-=B(OH)4-,写出硼酸在水溶液中的电离方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在含有FeBr2和FeI2的混合溶液中,通入过量的氯气,然后把溶液加热蒸干、灼烧,最后留下的是
①FeCl2②FeCl3③I2④Br2⑤Fe(OH)3⑥Fe2O3⑦FeO
A.①③④
B.③⑦
C.③⑤
D.⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是元素周期表的一部分,A、B、C、D、E、X 是元素周期表给出元素组成的常见单质或化合物。已知 A、B、C、D、E、X 存在如图所示转化关系(部分生成物和反应条件略去)。
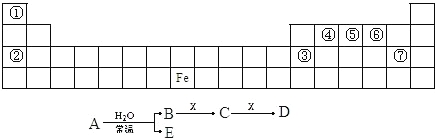
(1)若 E 为氧化物,则 A 与水反应的方程式为____ ___,该反应中氧化剂和还原剂物质的量之比为__________ 。
①当 X 为碱性盐溶液,C 分子中有 22 个电子时,D 是__________(写化学式)。
②当 X 为金属单质时,X 与足量 B 的稀溶液反应生成 C 的离子方程式为________ __,写出检验生成物 C 的阳离子所用试剂的电子式__________。
(2)若 E 为单质气体,D 为白色沉淀,A 可能是________(写化学式), X是_______(写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前世界上 60%的镁是从海水中提取的。学生就这个课题展开了讨论。已知海水提镁的主要步骤如下:
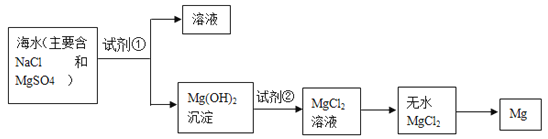
(一)在海水提镁的过程中如何实现对镁离子的富集? 学生提出三个不同观点。
观点 1:直接往海水中加入沉淀剂。
观点 2:高温加热蒸发海水后,再加入沉淀剂。
观点 3:利用晒盐后的苦卤水,再加入沉淀剂。
请你评价三个学生提出的观点是否正确(填是或否),并简述理由。

(二)在海水提镁的过程中如何实现对镁离子的分离?
(1)为了使镁离子沉淀下来,加入的足量试剂①是____________________(填化学式)。
(2)加入的足量试剂②是____________________(填化学式)。
(3)试从节约能源,提高金属镁的纯度分析,以下适宜的冶镁方法是__________。
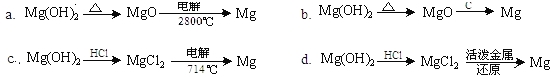
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应aA(g)+bB(g)![]() cC(g)(△H<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:
cC(g)(△H<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:
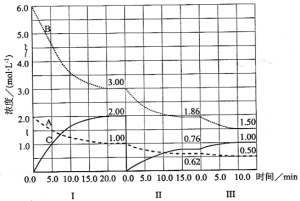
回答问题:
(1)反应的化学方程式中a∶b∶c为 ;
(2)由第一次平衡到第二次平衡,平衡移动的方向是_____,采取的措施是____________。
(3)比较第Ⅱ阶段反应温度(T2)和第Ⅲ阶段反应温度(T3)的高低;T2 T3(填“<”“>”“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分。
碳 | Y | Z | |
X | 硫 | W |
回答下列问题
(1)W元素在周期表中的位置为__________。
(2)表中元素原子半径最大的是(写元素符号)__________。
(3)写出由上表中两种元素组成,可用作制冷剂的一种化合物的电子式__________。
(4)下列事实不能说明Z元素的非金属性比S元素的非金属性强的是__________;
A.Z单质与H2S溶液反应,溶液变浑浊
B.在氧化还原反应中,1molY单质比1molS得电子多
C.Z和S两元素的简单氢化物受热分解,前者的分解温度高
(5)X与W两元素的单质反应生成1molX的最高价化合物,恢复至室温,放热687kJ,已知该化合物的熔、沸点分别为-69℃和58℃,写出该反应的热化学方程式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、W为五种短周期元素。X原子的质子数与电子层数相同,W原子核外电子数是M原子最外层电子数的2倍,Y、Z、M、W在周期表中的相对位置如图所示。下列说法不正确的是
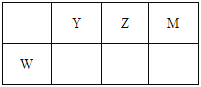
A. 原子半径:W>Y>Z>M>X
B. 热稳定性:XM>X2Z,沸点:X2Z>YX3
C. X、Y、Z三种元素形成的化合物中不可能含离子键
D. ZM2、YM3、WM4分子中每个原子最外层均满足8电子结构
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com