
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下,22.4L一氯甲烷中含极性共价键数目为4NA
B. 常温下,46g NO2、N2O4组成的混合气体中所含有的分子数为NA
C. 36g3H2中含有的中子数目为12NA
D. 2.24 L(标准状况)O2与足量钠反应时,转移电子数目不可能为0.3NA
【答案】A
【解析】A,n(CH3Cl)=![]() =1mol,1个CH3Cl分子中含3个C-H极性共价键和1个C-Cl极性共价键,标准状况下22.4LCH3Cl中含4mol极性共价键,A项正确;B,若46g气体全为NO2,所含分子物质的量为
=1mol,1个CH3Cl分子中含3个C-H极性共价键和1个C-Cl极性共价键,标准状况下22.4LCH3Cl中含4mol极性共价键,A项正确;B,若46g气体全为NO2,所含分子物质的量为![]() =1mol,若46g气体全为N2O4,所含分子物质的量为
=1mol,若46g气体全为N2O4,所含分子物质的量为![]() =0.5mol,46gNO2、N2O4的混合气体中所含分子物质的量大于0.5mol小于1mol,B项错误;C,3H2的摩尔质量为6g/mol,n(3H2)=
=0.5mol,46gNO2、N2O4的混合气体中所含分子物质的量大于0.5mol小于1mol,B项错误;C,3H2的摩尔质量为6g/mol,n(3H2)=![]() =6mol,1个3H2中含有4个中子,所含中子物质的量为24mol,C项错误;D,n(O2)=
=6mol,1个3H2中含有4个中子,所含中子物质的量为24mol,C项错误;D,n(O2)=![]() =0.1mol,若足量Na与O2反应生成Na2O,转移电子物质的量为0.4mol,若足量Na与O2反应生成Na2O2,转移电子物质的量为0.2mol,则足量Na与O2反应转移电子物质的量为0.2mol
=0.1mol,若足量Na与O2反应生成Na2O,转移电子物质的量为0.4mol,若足量Na与O2反应生成Na2O2,转移电子物质的量为0.2mol,则足量Na与O2反应转移电子物质的量为0.2mol![]() n(e-)
n(e-)![]() 0.4mol,可能为0.3mol,D项错误;答案选A。
0.4mol,可能为0.3mol,D项错误;答案选A。


科目:高中化学 来源: 题型:
【题目】向50 mL 18 mol·L-1的H2SO4溶液中加入适量的铜片并加热。充分反应后,被还原的H2SO4的物质的量( )
A. 小于0.45 mol B. 等于0.45 mol
C. 在0.45~0.90 mol之间 D. 大于0.45 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)0.01mol某气体的质量为0.44g,该气体的摩尔质量为_______;在标准状况下,该气体的密度是_______
(2)0.3 mol氨气和0.4 mol二氧化碳的质量________(填“相等”或“不相等”,下同),所含分子数________,所含原子数________.
(3) 质量都是50 g的HCl、NH3、CO2、O2四种气体中,含有分子数目最少的是________,在相同温度和相同压强条件下,体积最大的是________,体积最小的是________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴的化合物在磁性材料生产、电池制造、催化剂制备等方面应片非常广泛。
(1)Co2+基态外围电子排布式为______________。
(2)制备[Co(H2O)6]2+反应为(NH4)2[Co(SCN)4]+6H2O=[Co(H2O)6](SCN)2+2NH4SCN。
①配合物[Co(H2O)6]2+中与Co2+形成配位键的原子是_______(填元素符号);SCN-的空间构型为_____(用文字描述)。
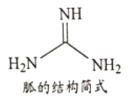
②NH4SCN在180-190℃分解并制得胍(结构简式如下图所示),胍分子中氮原子杂化轨道类型____;lmol胍中含σ键数目为___________。
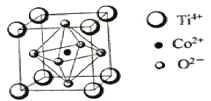
(3)一种钴的化合物可用作石油脱硫的催化剂,其晶胞结构如下图所示,则晶体中与每个O2-紧邻的O2-有________个(填数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】摩尔质量是指单位物质的量的物质所具有的质量,已知NA为阿伏加德罗常数的值,请回答下列问题:
(1)已知NH3的相对分子质量为17,则NH3的摩尔质量为________。
(2)已知一个铁原子的质量为b g,则铁原子的摩尔质量为________。
(3)已知a g某气体中含分子数为b,则该气体的摩尔质量为________。
(4)有以下四种物质:①22 g二氧化碳 ②8 g氢气 ③1.204×1024个氮气分子 ④4 ℃时18 mL水
它们所含分子数最多的是__________,所含原子数最多的是________,质量最大的是________,所含电子数最多的是________(填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲、乙两种有机物(结构简式如下图),下列说法不正确的是
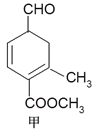
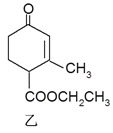
A. 二者与溴的CCl4溶液发生加成反应,消耗溴的物质的量分别为2mol、1mol
B. 甲、乙互为同分异构体
C. 1mol甲与H2在一定条件下反应,最多消耗3mol H2
D. 等物质的量的甲、乙分别与NaOH溶液反应,消耗NaOH的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)从氯化钾溶液中得到氯化钾固体,选择装置________(填代表装置图的字母,下同);除去自来水中 的Cl-等杂质,选择装置________________。
(2)从碘水中分离出I2,选择装置________,该分离方法的名称为________________。
(3)装置A中①的名称是________,进水的方向是从________口进水。
II.某化学课外小组用海带为原料制取了少量碘水.现用CCl4从碘水中萃取碘并用分液漏斗分离两种溶液.其实验操作可分解为如下几步:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把50 mL碘水和15 mL CCl4加入分液漏斗中,并盖好玻璃塞;
C.检验分液漏斗活塞和上口玻璃塞是否漏液;
D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.放开活塞,用烧杯接收溶液;
F.从分液漏斗上口倒出上层水溶液;
G.将漏斗上口的玻璃塞打开,或使溶液上的凹槽或小孔对准漏斗口上的小孔;
H.静置、分层.
就此实验,完成下列填空:
(1)正确操作步骤的顺序是(用上述各操作的编号字母填空):
________→________→________→A→H→________→E→F._____________
(2)上述E步骤的操作中应注意______________________________________.上述G步骤操作的目的是_____________________________________________.
(3)能选用CCl4从碘水中萃取碘的原因是______________________________________.
(4)下列物质不能作为从溴水中萃取溴的溶剂是________.
A.酒精 B.苯(一种有机溶剂,与水互不相溶,密度比水小) C.汽油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将足量氯气通入盛有KI和KBr混合液的烧杯中,完全反应后,将溶液蒸干,灼烧,最后烧杯中剩余的固体是( )
A.KCl和I2
B.I2
C.KCl
D.KCl、Br2和I2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com