

| A. | 图①可以表示,可逆反应2SO2(g)+O2(g)?2SO3(g)△H<0维持温度、压强不变、t1时充入SO3(g) | |
| B. | 根据图②判断,物质A反应生成物C的△H>0 | |
| C. | 图③表示向一定量的氢氧人钠溶液中滴加一定浓度硫酸溶液时的pH变化 | |
| D. | 图④中开关K置于A或B处均可减缓铁的腐蚀 |
分析 A.恒压容器中某化学平衡体系仅充入生成物后,反应物浓度降低,生成物浓度增大,以此判断反应速率判断;
B.反应物能量大于生成物能量,则反应过程中放出热量;
C.向一定量的氢氧人钠溶液中滴加一定浓度硫酸溶液时,溶液酸碱性的变化是:碱性溶液→中性溶液→酸性溶液,据此判断pH的变化;
D.金属作原电池的正极或电解池的阴极能延缓其被腐蚀.
解答 解:A.恒压容器中某化学平衡体系仅充入生成物后,反应物浓度降低,正反应速率减小,生成物浓度增大,逆反应速率增大,图象符合,故A正确;
B.化学反应中,如果反应物能量大于生成物能量,则反应过程中要放出热量,即△H<0,如果反应物能量小于生成物能量,则反应过程中要吸收能量,即△H>0,该能量图,物质A反应生成物C为放出热量,即△H<0,故B错误;
C.向一定量的氢氧人钠溶液中滴加一定浓度硫酸溶液时,溶液酸碱性的变化是:碱性溶液→中性溶液→酸性溶液,所以溶液的pH在不断减小,故C错误;
D.当开关置于A处时,该装置是电解池,铁作阴极而被保护,当开关置于B处时,该装置是原电池,铁作负极而加快其腐蚀,故D错误;
故选A.
点评 本题是图象分析题,涉及知识点较多,易错选项是A,注意外界条件对化学反应速率及化学平衡移动的影响,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | Na2CO3的热稳定性比NaHCO3强 | |
| B. | 相同温度时,Na2CO3 的溶解度大于NaHCO3 的溶解度 | |
| C. | Na2CO3 和NaHCO3都能和稀盐酸反应产生CO2 气体 | |
| D. | NaHCO3 一定条件下可转化为Na2CO3,但Na2CO3 不能转化为NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
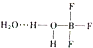 硼元素在化学中很重要的地位,硼及其化合物广泛应用于水磁材料、超导材料、富燃料材料、复合材料等高新材料领域应用.
硼元素在化学中很重要的地位,硼及其化合物广泛应用于水磁材料、超导材料、富燃料材料、复合材料等高新材料领域应用.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 )广泛存在于水果中,尤以苹果、葡萄、西瓜、山楂内最多
)广泛存在于水果中,尤以苹果、葡萄、西瓜、山楂内最多查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1×10-5mol/L | B. | 1×10-6mol/L | C. | 1×10-8mol/L | D. | 1×10-9molL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

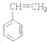 )为原料工业制备苯乙炔(
)为原料工业制备苯乙炔( )的流程如下:
)的流程如下: $→_{(1)}^{Br_{2}}$甲$\overrightarrow{(2)}$
$→_{(1)}^{Br_{2}}$甲$\overrightarrow{(2)}$

 +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$ +2NaBr+2H2O
+2NaBr+2H2O ,其苯环上二氯取代物有三种的芳香烃的名称为对二甲苯或1,4-二甲苯.
,其苯环上二氯取代物有三种的芳香烃的名称为对二甲苯或1,4-二甲苯.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com