
·ÖĪö £Ø1£©ĀĮČČ·“Ó¦ÖŠŃ”ÓĆÓĆĀČĖį¼Ų×öÖśČ¼¼Į£»
£Ø2£©ĀĮ·ŪŗĶŃõ»ÆĢśŌŚøßĪĀĻĀ·“Ӧɜ³ÉŃõ»ÆĀĮŗĶĢś£»
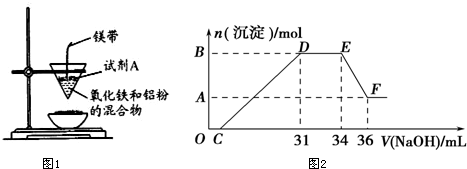
£Ø3£©O”śC Ö®¼äƻӊ³ĮµķÉś³É£¬ĖµĆ÷ĻõĖį¹żĮ棬O”śCÖ®¼ä·¢ÉśµÄ·“Ó¦Ėį¼īÖŠŗĶ·“Ó¦£¬Ąė×Ó·½³ĢŹ½ĪŖH++OH-ØTH2O£¬
DÓėEŅ»¶Ī³ĮµķµÄÖŹĮæƻӊ·¢Éś±ä»Æ£¬ĪŖNH4NO3ŗĶNaOH·“Ó¦£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£¬NH4++OH-ØTNH3•H2O£¬
EÓėFÖ®¼ä³ĮµķµÄĮæ¼õÉŁ£¬æĻ¶ØŹĒŅņĪŖAl£ØOH£©3ČܽāŌŚĒāŃõ»ÆÄĘČÜŅŗÖŠ£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖAl£ØOH£©3+OH-=AlO2-+2H2O£¬ŅŌ“Ė½ųŠŠ½ā“š£®
½ā“š ½ā£ŗ£Ø1£©ĀČĖį¼Ų¼ÓČČ·Ö½āÉś³ÉŃõĘų£¬ĀĮČČ·“Ó¦ÖŠŠčŅŖÓƵ½ĀČĖį¼Ų£¬ŌņAĪŖĀČĖį¼Ų£¬
¹Ź“š°øĪŖ£ŗĀČĖį¼Ų£»
£Ø2£©ĀĮ·ŪŗĶŃõ»ÆĢśŌŚøßĪĀĻĀ·“Ӧɜ³ÉŃõ»ÆĀĮŗĶĢś£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗFe2O3+2Al$\frac{\underline{\;øßĪĀ\;}}{\;}$2 Fe+Al2O3£¬
¹Ź“š°øĪŖ£ŗFe2O3+2Al$\frac{\underline{\;øßĪĀ\;}}{\;}$2 Fe+Al2O3£»
£Ø3£©¢ŁOC·¢ÉśH++OH-ØTH2O£»CD·“Ӧɜ³ÉĒāŃõ»ÆĀĮŗĶĒāŃõ»ÆĢś³Įµķ£¬DÓėEŅ»¶Ī³ĮµķµÄÖŹĮæƻӊ·¢Éś±ä»Æ£¬ĪŖNH4NO3ŗĶNaOH·“Ó¦£¬Ąė×Ó·½³ĢŹ½ĪŖ£¬NH4++OH-ØTNH3•H2O£¬
¹Ź“š°øĪŖ£ŗNH4++OH-ØTNH3•H2O£»
¢Ś¼ÓČė34mLNaoHČÜŅŗŹ±£¬ČÜÖŹĪŖĻõĖįÄĘ£¬ŌČÜŅŗÖŠĻõĖį×Ŗ»ÆĪŖĪŖĻõĖįÄĘŗĶŅ»Ė®ŗĻ°±Į½²æ·Ö£¬
ĘäÖŠĻõĖįÄĘÖŠĻūŗĵÄĻõĖįĪŖ£ŗ4mol/L”Į34”Į10-3L=0.136mol£»Ņ»Ė®ŗĻ°±µÄĪļÖŹµÄĮæĪŖ£ŗ4mol/L”Į£Ø34-31£©”Į10-3L=0.012mol£¬
ŌņĻõĖįµÄ×ÜĪļÖŹµÄĮæĪŖ£ŗ0.136mol+0.012mol=0.148mol£¬ĻõĖįČÜŅŗÅضČĪŖ£ŗ$\frac{0.148mol}{0.1L}$=1.48mol/L£¬
¹Ź“š°øĪŖ£ŗ1.48mol/L£»
¢ŪEÓėFÖ®¼ä³ĮµķµÄĮæ¼õÉŁ£¬ĪŖAl£ØOH£©3ČܽāŌŚĒāŃõ»ÆÄĘČÜŅŗÖŠ£¬
Ęä·“Ó¦·½³ĢŹ½ĪŖAl£ØOH£©3+NaOH=NaAlO2+2H2O£¬
EF¶ĪµÄn£ØNaOH£©=4mol/L”Į2”Į10-3L=0.008mol£¬
Al£ØOH£©3+NaOH=NaAlO2+2H2O
1 mol 1mol
0.008 mol 0.008mol
Al£ØOH£©3µÄĮæŹĒ0.008mol£¬ĖłŅŌAl3+Ņ²ŹĒ0.008mol£¬
ĖłŅŌBÓėA²īÖµĪŖ0.008mol£¬
¹Ź“š°øĪŖ£ŗ0.008£®
µćĘĄ ±¾Ģāæ¼²éĮĖĀĮČČ·“Ó¦”¢Ąė×Ó·½³ĢŹ½¼ĘĖć£¬ĢāÄæÄѶČÖŠµČ£¬×¢ŅāÕĘĪÕĀĮČČ·“Ó¦ŌĄķ£¬£Ø2£©ĪŖÄŃµć”¢Ņדķµć£¬Ć÷Č·Ķ¼ĻóĒśĻß±ä»ÆµÄŗ¬ŅåĪŖ½ā“š¹Ų¼ü£¬ŹŌĢāÅąŃųĮĖѧɜµÄ·ÖĪö”¢Ąķ½āÄÜĮ¦¼°»ÆѧŹµŃ锢»Æѧ¼ĘĖćÄÜĮ¦£®


 ³¤½×÷Ņµ±¾Ķ¬²½Į·Ļ°²įĻµĮŠ“š°ø
³¤½×÷Ņµ±¾Ķ¬²½Į·Ļ°²įĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | BaSO4±ČBaCO3Čܽā¶ČŠ”£¬ĖłŅŌ£¬BaCO3æÉŅŌ×Ŗ»ÆĪŖBaSO4 | |
| B£® | BaCO3”¢BaSO4¾ł²»ČÜÓŚĖ®£¬ĖłŅŌ¶¼æÉŅŌ×ö±µ²ĶŹŌ¼Į | |
| C£® | ĻņNa2CO3ČÜŅŗÖŠ¼ÓČėBaCl2ŗĶNa2SO4£¬µ±Į½ÖÖ³Įµķ¹²“ꏱ£¬$\frac{c£ØS{O}_{4}^{2-}£©}{c£ØC{O}_{3}^{2-}£©}$=4.4”Į10-2 | |
| D£® | ³£ĪĀĻĀ£¬BaCO3ČōŅŖŌŚNa2SO4ČÜŅŗÖŠæŖŹ¼×Ŗ»ÆĪŖBaSO4£¬ŌņNa2SO4µÄÅØ¶Č±ŲŠė²»µĶÓŚ 2.2”Į10-6 mol•L-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·Ø¹ś»Æѧ¼ŅĪ¬ĄÕŹ×“ĪĢį³öÓŠ»ś»ÆѧµÄøÅÄī£»µĀ¹ś»Æѧ¼Ņ±“²ÉĄļĪŚĖ¹ÓÉĒčĖįļ§ŗĻ³ÉĮĖÄņĖŲ£¬Ź×“Ī“ņĘĘĮĖÓŠ»śĪļŗĶĪŽ»śĪļµÄ½ēĻŽ | |
| B£® | Ąī±ČĻ£ÓĆČ¼ÉÕ·ØĄ“²ā¶ØÓŠ»ś»ÆŗĻĪļÖŠĢ¼ĒāŌŖĖŲÖŹĮæ·ÖŹż | |
| C£® | ÓĆŗĖ“Ź²ÕńĒāĘ×ŗĶŗģĶā¹āĘ×·ØæÉŅŌĒų±šŅŅ“¼ŗĶ¶ž¼×ĆŃ£ØCH3OCH3£© | |
| D£® | ÓĆ”°Ķ¬Ī»ĖŲŹ¾×Ł·Ø”±ŹĒŃŠ¾æÓŠ»ś»Æѧ·“Ó¦Ąś³ĢµÄŹÖ¶ĪÖ®Ņ» |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | »Æѧ·“Ó¦ĖŁĀŹÖøµÄŹĒĘ½¾łĖŁĀŹ | |
| B£® | µ±»Æѧ·“Ó¦“ļµ½Ęä×ī“óĻŽ¶ČŹ±£¬²Ī¼Ó·“Ó¦µÄĪļÖŹµÄÖŹĮæ±£³Öŗć¶Ø | |
| C£® | ¶ŌÓŚĶ¬Ņ»»Æѧ·“Ó¦£¬Ń”ÓĆ²»Ķ¬µÄĪļÖŹ±ķŹ¾»Æѧ·“Ó¦ĖŁĀŹŹ±£¬Ę䏿ֵŅ»¶Ø²»Ķ¬ | |
| D£® | æÉÄę·“Ó¦²»ÄܽųŠŠµ½µ×£¬ĢåĻµÖŠ·“Ó¦ĪļÓėÉś³ÉĪļ¹²“ę |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ąė×Ó»ÆŗĻĪļÖŠæÉÄÜŗ¬¹²¼Ū¼ü£¬¹²¼Ū»ÆŗĻĪļÖŠ²»ŗ¬Ąė×Ó¼ü | |
| B£® | ¹²¼Ū»ÆŗĻĪļÖŠæÉÄÜŗ¬Ąė×Ó¼ü£¬Ąė×Ó»ÆŗĻĪļÖŠÖ»ŗ¬Ąė×Ó¼ü | |
| C£® | ¹¹³Éµ„ÖŹ·Ö×ÓµÄĪ¢Į£Ņ»¶Øŗ¬ÓŠ¹²¼Ū¼ü | |
| D£® | Ė«Ō×Ó·Ö×ÓÖŠµÄ¹²¼Ū¼ü£¬Ņ»¶ØŹĒ·Ē¼«ŠŌ¼ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĮņĖįµÄ²śĮæŹĒŗāĮæŅ»øö¹ś¼ŅŹÆÓĶ»Æ¹¤Ė®Ę½·¢Õ¹µÄ±źÖ¾ | |
| B£® | ŹÆÓĶĮŃ»ÆµÄÖ÷ŅŖÄæµÄŹĒĪŖĮĖ»ńµĆ¶ĢĮ“µÄ²»±„ŗĶĢž | |
| C£® | ³ōŃõæÕ¶“µÄŠĪ³ÉÓė»ÆŹÆČ¼ĮĻĆŗ”¢ŹÆÓĶµÄ“óĮæŹ¹ÓĆĪŽ¹Ų | |
| D£® | ŹÆÓĶµÄÖ÷ŅŖ³É·ÖŹĒĢ¼Ēā»ÆŗĻĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 Ę»¹ūĖįŹĒŅ»ÖÖ³£¼ūµÄÓŠ»śĖį£¬Ęä½į¹¹¼ņŹ½ČēĶ¼ĖłŹ¾£ŗ
Ę»¹ūĖįŹĒŅ»ÖÖ³£¼ūµÄÓŠ»śĖį£¬Ęä½į¹¹¼ņŹ½ČēĶ¼ĖłŹ¾£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ņ»¶ØÓŠ¼×ĖįŅŅõ„£¬æÉÄÜÓŠ¼×“¼ | B£® | ĖÄÖÖĪļÖŹ¶¼ÓŠ | ||
| C£® | ÓŠ¼×ĖįŅŅõ„ŗĶ¼×Ėį | D£® | ÓŠ¼×“¼ŗĶ¼×Ėį |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1 mol FeÓėÉŁĮæĀČĘų·“Ó¦Ź±×ŖŅʵĵē×ÓŹżĪŖ2NA | |
| B£® | 0.2 mol SŌŚæÕĘųÖŠ³ä·ÖČ¼ÉÕ£¬×ŖŅʵē×ÓŹżĪŖ0.6NA | |
| C£® | 0.1molCl2ČÜÓŚĖ®ÖŠ·¢Éś·“Ó¦£¬×ŖŅʵē×ÓŹżĪŖ0.1NA | |
| D£® | 1.5 mol Na2O2Óė×ćĮæµÄ¶žŃõ»ÆĢ¼³ä·Ö·“Ó¦£¬×ŖŅʵē×ÓŹżĪŖ1.5NA |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com