
【题目】亚硝酸钙是一种阻锈剂,可用于染料工业,某兴趣小组拟制备Ca(NO2)2并对其性质进行探究。
【背景素材】
Ⅰ.NO+NO2+Ca(OH)2Ca(NO2)2+H2O。
Ⅱ.Ca(NO2)2能被酸性KMnO4溶液氧化成![]() ,
, ![]() 被还原为Mn2+。
被还原为Mn2+。
Ⅲ.在酸性条件下,Ca(NO2)2能将I氧化为I2, ![]() 能将I2还原为I。
能将I2还原为I。
【制备氮氧化物】
(1)甲组同学拟利用如下图所示装置制备氮氧化物。
![]()
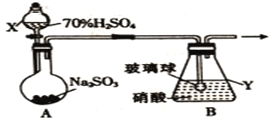
①仪器X的名称是_______________,在制备氮氧化物前要先____________________________。
②装置B中逸出的NO与NO2的物质的量之比为1∶1,则装置B中发生反应的化学方程式为____________________________________________________,若其他条件不变,增大硝酸的浓度,则会使逸出的气体中n(NO2)__________n(NO)(填“>”或“<”)。
【制备Ca(NO2)2】
(2)乙组同学拟利用装置B中产生的氮氧化物制备Ca(NO2)2,装置如图。
![]()
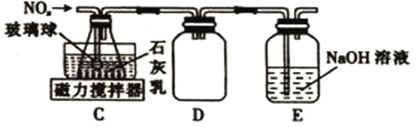
①装置C中导管末端接一多孔玻璃球的作用是______________________________________。
②装置D的作用是_______________________;装置E的作用是______________________。
【测定Ca(NO2)2的纯度】
(3)丙组同学拟用滴定法测定Ca(NO2)2的纯度(杂质不参加反应),可供选择的试剂:
a.稀硫酸 b.c1 mol·L1的KI溶液 c.淀粉溶液
d.c2 mol·L1的Na2S2O3溶液 e.c3 mol·L1的酸性KMnO4溶液
①利用Ca(NO2)2的还原性来测定其纯度,可选择的试剂是________________(填字母)。
②利用Ca(NO2)2的氧化性来测定其纯度的步骤:准确称取m g Ca(NO2)2样品放入锥形瓶中,加适量水溶解,加入______________________________,然后滴加稀硫酸,用c2 mol·L1的Na2S2O3溶液滴定至溶液颜色由________________________,且半分钟内不变色,读取消耗Na2S2O3溶液的体积。为减少误差,须__________________________________________(请补充完整实验步骤)。
【答案】 分液漏斗 检查装置的气密性 2SO2+2HNO3+H2ONO+NO2+2H2SO4 > 增大与石灰乳的接触面积,加快反应速率 防止倒吸(或作安全瓶) 吸收未反应的氮氧化物 e 过量c1 mol·L1的KI溶液、淀粉溶液 蓝色恰好变为无色 重复以上操作2~3次
【解析】(1) ①仪器X、Y分别是分液漏斗、锥形瓶;制备气体时一般必须先检查装置的气密性,故在制备氮氧化物前要先检查装置的气密性;②根据题意,装置B中盛放的是硝酸,二氧化硫与硝酸反应放出一氧化氮和二氧化氮,若逸出的NO与NO2的物质的量之比为1∶1,则装置B中发生反应的化学方程式为2SO2+2HNO3+H2O=NO+NO2+2H2SO4,若其他条件不变,硝酸的浓度越大,生成的二氧化氮越多,则会使逸出的气体中n(NO2)>n(NO);⑵①装置C中导管末端接一多孔玻璃球,可以增大与石灰乳的接触面积,加快反应速率;②反应中,装置内气体的压强会发生变化,装置D可以防止倒吸(或作安全瓶);装置E中的氢氧化钠可以吸收未反应的氮氧化物,防止污染空气;⑶ ①根据信息Ⅱ.Ca(NO2)2能被酸性KMnO4溶液氧化成NO3-,MnO4-被还原为Mn2+,利用Ca(NO2)2的还原性来测定其纯度,可选择的试剂是c3mol·L-1 的酸性 KMnO4 溶液,答案选e;②根据信息Ⅲ.在酸性条件下,Ca(NO2)2能将I-氧化为I2,S2O32-能将I2还原为I-。利用Ca(NO2)2的氧化性来测定其纯度,步骤为:准确称取m g Ca(NO2)2样品放入锥形瓶中,加适量水溶解,加入过量c1mol·L-1的KI溶液、淀粉浓液,然后滴加稀硫酸,用c2 mol·L1的Na2S2O3溶液滴定至溶液颜色由蓝色恰好变为无色,且半分钟内不变色,读取消耗Na2S2O3溶液的体积。为减少误差,须重复以上操作23次。


 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:
【题目】右图为以惰性电极进行电解:
(1)写出A、B、C、D各电极上的电极反应式和总反应方程式:
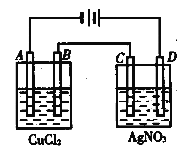
A:________________,B:__________________,总反应方程式:________________________;C:________________________________,D:________________________________,总反应方程式:___________________________;
(2)在A、B、C、D各电极上析出生成物的物质的量比为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】21世纪是钛的世纪.在800℃~1000℃时电解TiO2可制得钛,装置如图所示.下列叙述正确的是( ) 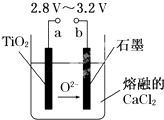
A.a为电源的正极
B.石墨电极上发生还原反应
C.阴极发生的反应为:TiO2+4e﹣═Ti+2O2﹣
D.每生成0.1mol钛,转移电子0.2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,因为反应条件改变,反应产物可以不同的是( )
A. 钠与氧气反应 B. 稀盐酸和硝酸银溶液
C. 铁在氯气中燃烧 D. 一氧化碳在氧气中燃烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施能提高合成氨[N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ/mol]厂的生产效率和经济效益的是
2NH3(g) ΔH=-92.4 kJ/mol]厂的生产效率和经济效益的是
①采用20 MPa~50 MPa的压强;②使用催化剂;③在合适的温度下进行反应;④从平衡混合气体中液化分离出NH3,并将N2、H2循环使用
A. ①③④ B. ③④ C. ①②③ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为﹣285.8kJmol﹣1、﹣283.0kJmol﹣1和﹣726.5kJmol﹣1 . 请回答下列问题:
(1)用太阳能分解10mol水消耗的能量是 kJ.
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为 .
(3)在直接以甲醇为燃料的电池中,理想状态下,该燃料电池消耗1mol甲醇所能产生的最大电能为702.1kJ,则该燃料电池的理论效率为(燃料电池的理论效率是指电池所产生的最大电能占燃料电池反应所能释放的全部能量的百分比).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】容量瓶是用来配制物质的量浓度的溶液的定量仪器,其上标有:①温度、②浓度、③容量、④压强、⑤刻度线、⑥酸式或碱式这六项中的
A. ②④⑥ B. ③⑤⑥ C. ①②④ D. ①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中,既能与盐酸反应又能与氢氧化钠溶液反应的是( )
①NaHCO3 ②Al2O3 ③Al(OH)3 ④NaAlO2 ⑤Na2CO3 ⑥Al
A. ②③⑤ B. ①②③④ C. ①②③⑥ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是( )
A. 温度控制在500℃有利于合成氨反应
B. 用排饱和食盐水法收集Cl2
C. 打开碳酸饮料会有大量气泡冒出
D. 工业制取金属钾Na(l)+KCl(l) ![]() NaCl(l)+K(g)选取适宜的温度,使钾变成蒸气从反应混合物中分离出来
NaCl(l)+K(g)选取适宜的温度,使钾变成蒸气从反应混合物中分离出来
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com