
| A. | M的单质能够用来制造光导纤维 | |
| B. | Z、W、M的氧化物均可做耐高温材料 | |
| C. | 工业上常用电解熔融氯化物的方法制备Z、W的单质 | |
| D. | Y的单质都有剧毒,而且其着火点低,常保存在冷水中 |
分析 X的氢化物和最高价氧化物的水化物能反应生成一种离子化合物,应为N元素,X、Y同主族,则Y为P元素,Z、W、M是第3周期连续的三种元素,其中只有一种是非金属,且原子半径Z>W>M,可知M为Si元素,Z为Mg元素,W为Al元素,结合对应的单质、化合物的性质以及元素周期律知识解答该题.
解答 解:A.M是Si元素,Si单质能作太阳能电池板、能作硅芯片等,二氧化硅是用来制造光导纤维的原料,故A错误;
B.Z、W、M的氧化物分别是MgO、氧化铝、二氧化硅,这几种物质熔沸点都较高,所以均可做耐高温材料,故B正确;
C.Z是Mg、W是Al,工业上用电解熔融氯化镁的方法冶炼Mg,用电解熔融氧化铝的方法冶炼Al,因为氯化铝熔融状态下不导电,故C错误;
D.P的单质中白磷有剧毒,红磷没有剧毒,白磷常保存在冷水中,故D错误.
故选B.
点评 本题考查原子结构与元素周期律知识,为高考常见题型,侧重于学生的分析能力的考查,注意把握元素的结构特点以及性质的递变规律,知道常见元素及其化合物的性质和用途,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 总反应速率由反应②决定 | |
| B. | 在(NH4)2S2O8消耗完后,溶液一定显蓝色 | |
| C. | 若能观察都蓝色出现,刚起始时,n(Na2S2O3)=n[(NH4)2S2O8] | |
| D. | 升高温度,①、②的反应速率均加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④ | B. | ③④⑥ | C. | ④⑤ | D. | ④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
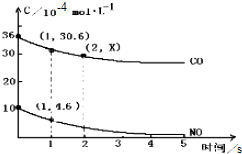
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 400 mL | B. | 200 mL | C. | 150 mL | D. | 80 mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com