
【题目】如图所示装置,电流表指针发生偏转,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液,则A、B、C应是下列各组中的( )
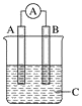
A. A是Zn,B是Cu,C为稀硫酸
B. A是Cu,B是Zn,C为稀硫酸
C. A是Fe,B是Ag,C为稀AgNO3溶液
D. A是Ag,B是Fe,C为稀AgNO3溶液
【答案】D
【解析】
利用原电池的工作原理进行分析,A电极逐渐变粗,说明阳离子在A电极上得到电子,转化成单质,即A电极为正极,B电极逐渐变细,说明电极B失去电子,转化成离子,即B电极为负极,然后逐步分析;
A电极逐渐变粗,A电极为正极,B电极逐渐变细,B电极为负极,
A、Zn比Cu活泼,因此Zn为负极,Cu为正极,A电极为负极,电极反应式为Zn-2e-=Zn2+,A电极逐渐变细,B电极为正极,电极反应式为2H+2e-=H2↑,B电极质量不变,故A不符合题意;
B、根据A选项分析,A为正极,电极反应式为2H++2e-=H2↑,A电极质量不变,B为负极,电极反应式为Zn-2e-=Zn2+,B电极质量减小,故B不符合题意;
C、Fe比Ag活泼,Fe为负极,即A电极上发生Fe-2e-=Fe2+,电极质量减少,B电极为正极,电极反应式为Ag++e-=Ag,电极质量增大,故C不符合题意;
D、根据选项C分析,A为正极,电极反应式为Ag++e-=Ag,电极质量增大,B为负极,电极反应式为Fe-2e-=Fe2+,电极质量减小,故D符合题意。


科目:高中化学 来源: 题型:
【题目】化学在环境保护中起着十分重要的作用,电化学降解NO3-的原理如图所示。下列说法不正确的是( )

A. 电解过程中,每转移1mol电子,则左侧电极就产生16g O2
B. 溶液中H+从阳极向阴极迁移
C. Ag-Pt电极的电极反应式为2NO3-+12H++10e-=N2↑+6H2O
D. B为电源的负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乳酸亚铁晶体{[CH3CH(OH)COO]2Fe·3H2O}是一种很好的食品铁强化剂,易溶于水,吸收效果比无机铁好,可由乳酸与FeCO3反应制得:
2CH3CH(OH)COOH+FeCO3+2H2O→[CH3CH(OH)COO]2Fe·3H2O +CO2↑。
I.制备碳酸亚铁:装置如图所示。
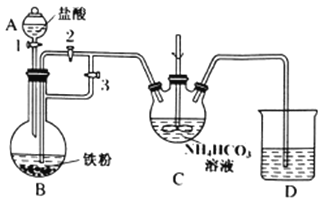
(1)C的名称是___________。
(2)清洗仪器,检查装置气密性,A中加入盐酸,B中加入铁粉,C中加入NH4HCO3溶液。为顺利达成实验目的,上述装置中活塞的打开和关闭顺序为:关闭活塞______,打开活塞______;加入足量盐酸后,关闭活塞1,反应一段时间后,关闭活塞____,打开活塞_____。C中发生的反应的离子方程式为_______________。
Ⅱ.制备乳酸亚铁晶体:
将制得的FeCO3加入乳酸溶液中,加入少量铁粉,在75℃下搅拌使之充分反应。然后再加入适量乳酸。
(3)加入少量铁粉的作用是______________。从所得溶液中获得乳酸亚铁晶体所需的实验操作是隔绝空气低温蒸发,________、干燥。
Ⅲ.乳酸亚铁晶体纯度的测量:
(4)若用KMnO4滴定法测定样品中Fe2+的量进而计算纯度时,发现结果总是大于100%,其原因可能是_____________________。
(5)经查阅文献后,改用Ce(SO4)2标准溶液滴定进行测定。反应中Ce4+离子的还原产物为Ce3+。测定时,先称取5.760g样品,溶解后进行必要处理,用容量瓶配制成250mL溶液,每次取25.00mL,用0.1000mol/LCe(SO4)2标准溶液滴定至终点,记录数据如下表。
滴定次数 | 0.1000mol/LCe(SO4)2标准溶液体积/mL | |
滴定前读数 | 滴定后读数 | |
1 | 0.10 | 19.85 |
2 | 0.12 | 21.32 |
3 | 1.05 | 20.70 |
则产品中乳酸亚铁晶体的纯度为_________(以质量分数表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图像不符合反应Fe(s)+H2O(g)![]() FeO(s)+H2(g) ΔH<0 的是(图中v是速率,φ为混合物中H2的体积百分含量)( )
FeO(s)+H2(g) ΔH<0 的是(图中v是速率,φ为混合物中H2的体积百分含量)( )
A. 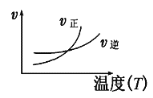 B.
B. 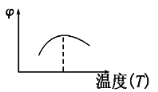
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的X和Y混合气体,通入密闭容器中发生如下反应:X(g)+2Y(g)![]() 2Z(g),平衡时混合气体中反应物的总物质的量与生成物的总物质的量之比为3:2,则Y的转化率最接近于
2Z(g),平衡时混合气体中反应物的总物质的量与生成物的总物质的量之比为3:2,则Y的转化率最接近于
A.33% B.40% C.50% D.67%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于从碘水中萃取碘的实验,下列说法错误的是( )
A.分液漏斗使用前要检验其是否漏液
B.萃取剂要求不溶于水,且碘在其中的溶解度比在水中的大
C.注入碘水和萃取剂,倒转分液漏斗反复用力振荡后立即分液
D.该实验需要选用的仪器是烧杯、分液漏斗、铁架台(带铁圈)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在密闭恒容的容器中,能表示反应达到化学平衡状态的是
3SiCl4(g)+2N2(g)+6H2(g)![]() Si3N4(s)+12HCl(g) ΔH=-Q(Q>0)
Si3N4(s)+12HCl(g) ΔH=-Q(Q>0)
A. v逆(N2)=3v正(H2) B. v正(HCl)=4v正(SiCl4)
C. 混合气体密度保持不变 D. c(N2):c(H2):c(HCl)保持不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com