
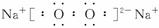
试回答下列问题:
(1)写出下列物质的化学式:A:____________,F:____________。
(2)写出B的电子式____________;A属于____________(填“极性”或“非极性”)分子。
(3)写出J→L的离子反应方程式_____________________________________________。
(1)CO2 Al
(2)![]() 非极性
非极性
(3)![]() +CO2+2H2O====Al(OH)3↓+
+CO2+2H2O====Al(OH)3↓+![]() 或2
或2![]() +CO2+3H2O====2Al(OH)3↓+
+CO2+3H2O====2Al(OH)3↓+![]()
解析:据题意,F常见金属高温下与金属氧化物反应,冶炼金属。推断出铝热反应:2Al+Fe2O3![]() Al2O3+2Fe;B淡黄色固体与A气体反应生成E气体和D物质可推出2CO2+2Na2O2====2Na2CO3+O2这一重要反应。再结合C的状态不难判断B+C
Al2O3+2Fe;B淡黄色固体与A气体反应生成E气体和D物质可推出2CO2+2Na2O2====2Na2CO3+O2这一重要反应。再结合C的状态不难判断B+C![]() E+G反应为2Na2O2+2H2O====4NaOH+O2↑,再据Al的两性,回忆基础反应2Al+2NaOH+2H2O====2NaAlO2+3H2↑,进一步推出L为Al(OH)3,I为Al2O3,
E+G反应为2Na2O2+2H2O====4NaOH+O2↑,再据Al的两性,回忆基础反应2Al+2NaOH+2H2O====2NaAlO2+3H2↑,进一步推出L为Al(OH)3,I为Al2O3,
2Al(OH)3![]() Al2O3+3H2O。
Al2O3+3H2O。


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

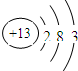
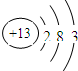
查看答案和解析>>
科目:高中化学 来源: 题型:
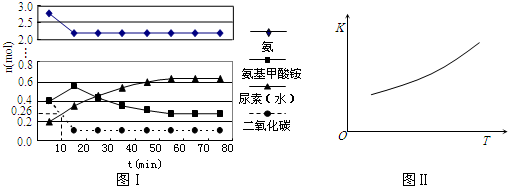
查看答案和解析>>
科目:高中化学 来源: 题型:
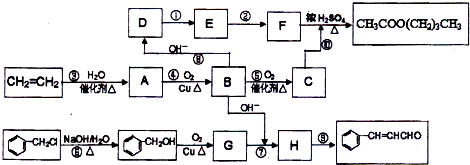
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com