
| 2min | 4min | 6min | 8min | … | |
| CO | 0.07 | 0.06 | 0.06 | 0.05 | … |
| H2 | x | 0.12 | 0.12 | 0.2 | … |
| CH3OH | 0.03 | 0.04 | 0.04 | 0.05 | … |
分析 (1)①已知:Ⅰ.H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H2=-242kJ/mol-1
Ⅱ.CH2OH(g)+$\frac{3}{2}$O2═CO2(g)+2H2O(g)△H2=-676kJ/mol-1
根据盖斯定律,Ⅰ×3-Ⅱ可得:CO2(g)+3H2(g)=CH3OH(g)+H2O(g);
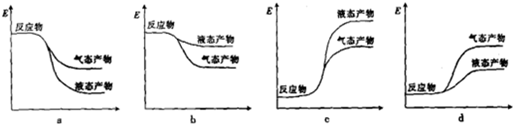
②气态产物能量比液态产物能量高,由①分析可知,合成甲醇的反应为放热反应,反应物的能量高于生成物的能量;
③若起始时c(CO)=1mol•L-1,c(H2O)=2mol•L-1,设H2O的浓度变化量为xmol/L,则:
H2O(g)+CO(g)?H2(g)+CO2(g),
起始量(mol/L):2 1 0 0
变化量(mol/L):x x x x
平衡量(mol/L):2-x 1-x x x
再根据平衡常数列方程计算解答;
(2)①由表中数据可知,从2min到4min,CO的浓度变化量为(0.07-0.06)mol/L=0.01mol/L,根据方程式计算氢气的浓度变化量,2min时氢气浓度=4min时氢气浓度+氢气浓度变化量;
4min与6min时,CO浓度相等,则4min、6min时反应处于平衡状态,平衡常数K=$\frac{c(C{H}_{3}OH)}{c(CO)×{c}^{2}({H}_{2})}$,代入平衡浓度计算;
②对比6min和8min时各物质的浓度可知改变条件后反应反应向正方向进行,按照转化量之比等于计量系数之比△C(CO):△C(H2):△C(CH3OH)=0.01mol/L:0.02mol/L:0.01mol/L,所以8min后三种物质的浓度应为:(0.06-0.01)mol/L、(0.12-0.02)mol/L、(0.04+0.01)mol/L,而8min后氢气的浓度为0.2mol/L,所以多加了0.1mol/L×10=1mol的氢气;
计算浓度商Qc,与平衡常数相比判断第8min时是否达到平衡状态;
③该合成反应的温度一般控制在240~270℃,选择此温度的原因是:此温度下的催化剂活性高;温度低,反应速率慢,单位时间内的产量低,而正反应为放热反应,温度过高,转化率降低;
(3)在常温下,20.00mL0.1000mol•L-1NaOH溶液与等体积、等浓度HCOOH溶液混合后所得溶液为HCOONa,溶液中HCOO-水解,溶液呈碱性.
解答 解:(1)①已知:Ⅰ.H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H2=-242kJ/mol-1
Ⅱ.CH2OH(g)+$\frac{3}{2}$O2═CO2(g)+2H2O(g)△H2=-676kJ/mol-1
根据盖斯定律,Ⅰ×3-Ⅱ可得:CO2(g)+3H2(g)=CH3OH(g)+H2O(g),△H=3×(-242kJ/mol)-(-676kJ/mol)=-50 kJ/mol,
故热化学方程式为:CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H=-50 kJ/mol;
故答案为:CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H=-50 kJ/mol;
②气态产物能量比液态产物能量高,由①分析可知,合成甲醇的反应为放热反应,反应物的能量高于生成物的能量,则符合条件的图象是a,
故选:a;
③若起始时c(CO)=1mol•L-1,c(H2O)=2mol•L-1,设H2O的浓度变化量为xmol/L,则:
H2O(g)+CO(g)?H2(g)+CO2(g)
起始量(mol/L):2 1 0 0
变化量(mol/L):x x x x
平衡量(mol/L):2-x 1-x x x
则$\frac{x×x}{(1-x)×(2-x)}$=4,解得x=$\frac{2}{3}$,
故水的转化率为$\frac{\frac{2}{3}mol/L}{2mol/L}$×100%=33.3%,
故答案为:33.3%;
(2)①由表中数据可知,从2min到4min,CO的浓度变化量为(0.07-0.06)mol/L=0.01mol/L,根据方程式可知氢气的浓度变化量为0.01mol/L×2=0.02mol/L,2min时氢气浓度=0.12mol/L+0.02mol/L=0.14mol/L,
4min与6min时,CO浓度相等,则4min、6min时反应处于平衡状态,故平衡常数K=$\frac{c(C{H}_{3}OH)}{c(CO)×{c}^{2}({H}_{2})}$=$\frac{0.04}{0.06×0.1{2}^{2}}$=46.3,
故答案为:0.14;46.3;
②对比6min和8min时各物质的浓度可知改变条件后反应反应向正方向进行,按照转化量之比等于计量系数之比△C(CO):△C(H2):△C(CH3OH)=0.01mol/L:0.02mol/L:0.01mol/L,所以8min后三种物质的浓度应为:(0.06-0.01)mol/L、(0.12-0.02)mol/L、(0.04+0.01)mol/L,而8min后氢气的浓度为0.2mol/L,所以多加了0.1mol/L×10=1mol的氢气;
8min时浓度商Qc=$\frac{0.05}{0.05×0.{2}^{2}}$=25<K=46.3,故8min时不是平衡状态,反应向正反应进行,
故答案为:加入1mol氢气;不是;
③该合成反应的温度一般控制在240~270℃,选择此温度的原因是:此温度下的催化剂活性高;温度低,反应速率慢,单位时间内的产量低,而正反应为放热反应,温度过高,转化率降低,
故答案为:温度低,反应速率慢,单位时间内的产量低,而正反应为放热反应,温度过高,转化率降低;
(3)在常温下,20.00mL0.1000mol•L-1NaOH溶液与等体积、等浓度HCOOH溶液混合后所得溶液为HCOONa,溶液中HCOO-水解:HCOO-+H2O?+HCOOH+OH-,溶液呈碱性,则pH>7,
故答案为:>;HCOO-+H2O?+HCOOH+OH-.
点评 本题考查化学平衡计算及影响因素、平衡常数计算及应用、热化学方程式书写、盐类水解等,是对学生综合能力的考查,难度中等.


科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| c(SO2)(mol•L-1) | 1.00 | 0.50 | 0.23 | 3.00×10-37 | 3.00×10-37 | 3.00×10-37 |
| c(CO)(mol•L-1) | 4.00 | 3.00 | 2.46 | 2.00 | 2.00 | 2.00 |
| 实验 编号 | T(℃) | SO2初始浓度 (mol•L-1) | CO初始浓度 (mol•L-1) | 催化剂 |
| Ⅰ | 260 | 1.00 | 3.00 | Cr2O3 |
| Ⅱ | Fe2O3 | |||
| Ⅲ | 380 | |||
| Ⅳ | 4.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 沸点/℃ | 密度/(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 11.72 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
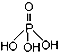 ),次磷酸钠(NaH2PO2)可用于化学镀镍等等.完成下列填空:
),次磷酸钠(NaH2PO2)可用于化学镀镍等等.完成下列填空:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com