
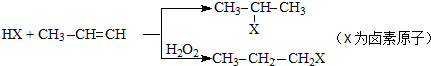
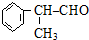 ,该物质是一种香料.
,该物质是一种香料.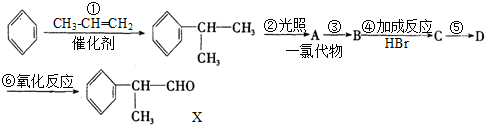
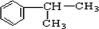 可与氯气发生取代反应生成A为
可与氯气发生取代反应生成A为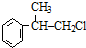 或
或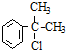 ,B能发生加成反应,则A应发生消去反应生成B,则B为
,B能发生加成反应,则A应发生消去反应生成B,则B为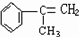 ,根据产物可知D为
,根据产物可知D为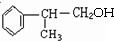 ,则C为
,则C为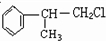 ,以此解答该题.
,以此解答该题.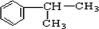 可与氯气发生取代反应生成A为
可与氯气发生取代反应生成A为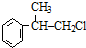 或
或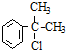 ,B能发生加成反应,则A应发生消去反应生成B,则B为
,B能发生加成反应,则A应发生消去反应生成B,则B为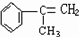 ,根据产物可知D为
,根据产物可知D为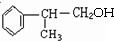 ,则C为
,则C为 ,
,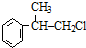 、
、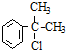 ,故答案为:
,故答案为: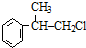 、
、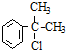 ;
;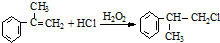 ,反应⑥的化学方程式为:
,反应⑥的化学方程式为: ,
,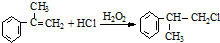 ;
; ;
;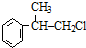 或
或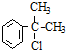 ,D为
,D为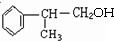 ,中间产物A须经反应③④⑤得D,而不采取直接转化为D的方法的原因是:
,中间产物A须经反应③④⑤得D,而不采取直接转化为D的方法的原因是: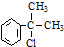 的水解产物
的水解产物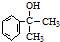 不能经氧化反应⑥而得到产品,会有大量副产物
不能经氧化反应⑥而得到产品,会有大量副产物 生成,
生成, 的水解产物
的水解产物 不能经氧化反应⑥而得到产品,会有大量副产物
不能经氧化反应⑥而得到产品,会有大量副产物 生成;
生成;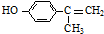 、
、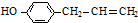 、
、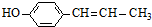 、
、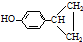 ,
,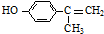 、
、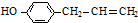 等.
等.


 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
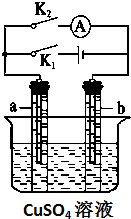 如图所示,某同学按照图装置进行如下实验,请回答下列问题:
如图所示,某同学按照图装置进行如下实验,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
 (每个折点表示一个碳原子,氢原子未画出),具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
(每个折点表示一个碳原子,氢原子未画出),具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )| A、2molBr2 2molNaOH |
| B、2molBr2 3molNaOH |
| C、3molBr2 4molNaOH |
| D、4molBr2 4molNaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
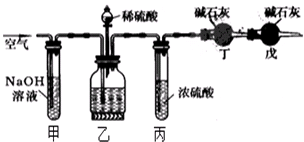 工业生产的纯碱中常含有少量的NaCl杂质,某校研究性活动小组为了测定混合物中纯碱的质量分数,拟使用如图实验装置,先测定一定量的样品和酸反应放出二氧化碳的质量,再计算混合物中纯碱的质量分数.
工业生产的纯碱中常含有少量的NaCl杂质,某校研究性活动小组为了测定混合物中纯碱的质量分数,拟使用如图实验装置,先测定一定量的样品和酸反应放出二氧化碳的质量,再计算混合物中纯碱的质量分数.查看答案和解析>>
科目:高中化学 来源: 题型:
 阅读下列实验内容,根据题目要求回答问题.
阅读下列实验内容,根据题目要求回答问题.查看答案和解析>>
科目:高中化学 来源: 题型:
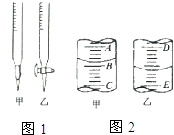 实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验.请你完成下列填空:
实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验.请你完成下列填空:| 实验编号 | NaOH溶液的浓度 (mol/L) | 滴定完成时,消耗NaOH溶液的体积(mL) | 待测盐酸溶液的体积(mL) |
| 1 | 0.10 | 22.02 | 20.00 |
| 2 | 0.10 | 22.00 | 20.00 |
| 3 | 0.10 | 21.98 | 20.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:


 也能发生类似V→Ⅵ的反应,请写出所生成醇的结构简式
也能发生类似V→Ⅵ的反应,请写出所生成醇的结构简式查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用丁达尔现象区分淀粉溶胶和豆浆 |
| B、钠和水反应实验时,余下的金属钠放回原瓶 |
| C、浓硫酸与浓硝酸混合时,将浓硝酸加入浓硫酸中 |
| D、蒸发结晶时,把液体蒸干再停止加热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com