
| A£® | ĶØČėĀČĘųŗóµÄČÜŅŗÖŠŅ»¶Ø²»“ęŌŚI- | |
| B£® | ĶØČėĀČĘųÖ®ŗóŌČÜŅŗÖŠµÄFe2+Č«²æ±»Ńõ»Æ | |
| C£® | ŌČÜŅŗÖŠµÄBr-²»æÉÄܱ»Ńõ»Æ | |
| D£® | ČōȔɣĮæĖłµĆČÜŅŗ£¬ŌŁ¼ÓČėCCl4ČÜŅŗ³ä·ÖÕńµ“£¬¾²ÖĆ”¢·ÖŅŗ£¬ĻĀ²ćČÜŅŗæÉÄܳŹ×ĻŗģÉ« |
·ÖĪö »¹ŌŠŌ£ŗI-£¾Fe2+£¾Br-£¬ĀČĘųĻČŃõ»ÆI-£¬Č»ŗóŃõ»Æ¶ž¼ŪĢś£¬×īŗóŃõ»ÆBr-£¬Ļņ·“Ó¦ŗóµÄČÜŅŗÖŠµĪ¼ÓKSCNČÜŅŗ£¬½į¹ūČÜŅŗ±äĪŖŃŖŗģÉ«£¬ĖµĆ÷I-Č«²æ±»Ńõ»Æ£¬Fe2+²æ·Ö»ņČ«²æ±»Ńõ»Æ£¬Br-æÉÄܱ»Ńõ»ÆĄ“·ÖĪö£®
½ā“š ½ā£ŗA£®»¹ŌŠŌ£ŗI-£¾Fe2+£¾Br-£¬Ļņŗ¬ÓŠFeBr2”¢FeI2µÄČÜŅŗÖŠĶØČėŅ»¶ØĮæµÄĀČĘųŗó£¬Ļņ·“Ó¦ŗóµÄČÜŅŗÖŠµĪ¼ÓKSCNČÜŅŗ£¬½į¹ūČÜŅŗ±äĪŖŃŖŗģÉ«£¬ĖµĆ÷Fe2+²æ·Ö»ņČ«²æ±»Ńõ»Æ£¬I-Ņ»¶ØČ«²æ±»Ńõ»Æ£¬¹ŹAÕżČ·£»
B£®Ļņ·“Ó¦ŗóµÄČÜŅŗÖŠµĪ¼ÓKSCNČÜŅŗ£¬½į¹ūČÜŅŗ±äĪŖŃŖŗģÉ«£¬ĖµĆ÷Fe2+²æ·Ö»ņČ«²æ±»Ńõ»Æ£¬¹ŹB“ķĪó£»
C£®Ļņ·“Ó¦ŗóµÄČÜŅŗÖŠµĪ¼ÓKSCNČÜŅŗ£¬½į¹ūČÜŅŗ±äĪŖŃŖŗģÉ«£¬ĖµĆ÷Fe2+²æ·Ö»ņČ«²æ±»Ńõ»Æ£¬³öĻÖĢśĄė×Ó£¬ŌČÜŅŗÖŠµÄBr-æÉÄܱ»Ńõ»Æ£¬¹ŹC“ķĪó£»
D£®I-Ņ»¶ØČ«²æ±»Ńõ»ÆI2£¬Ōņ¼ÓČėCCl4ČÜŅŗ³ä·ÖÕńµ“£¬¾²ÖĆ”¢·ÖŅŗ£¬ĻĀ²ćČÜŅŗ³Ź×ĻŗģÉ«£¬¹ŹDÕżČ·£®
¹ŹŃ”BC£®
µćĘĄ ±¾Ģāæ¼²éŃõ»Æ»¹Ō·“Ó¦£¬ĪŖøßæ¼³£¼ūĢāŠĶŗĶøßĘµæ¼µć£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦µÄ漲飬±¾ĢāĒŠČėµćŹĒŌŖĖŲ»ÆŗĻ¼Ū£¬×¢Ņā°ŃĪÕŃõ»ÆŠŌĒæČõµÄÅŠ¶Ļ£¬ĪŖ½ā“šøĆĢāµÄ¹Ų¼ü£¬ÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĄūÓĆ“ß»ÆÉ菩£¬æÉŅŌ½«Ęū³µĪ²ĘųÖŠCOŗĶNO×Ŗ»ÆĪŖĪŽŗ¦ĘųĢå | |
| B£® | °ėµ¼Ģ劊ŅµÖŠÓŠŅ»¾ä»°£ŗ”°“ÓɳĢ²µ½ÓĆ»§”±£¬¼ĘĖ滜Š¾Ę¬µÄ²ÄĮĻŹĒ¶žŃõ»Æ¹č | |
| C£® | ¹ųĀÆĖ®¹øÖŠŗ¬ÓŠµÄCaSO4£¬æÉĻČÓĆNa2CO3ČÜŅŗ“¦Ąķ£¬ŗóÓĆĖį³żČ„ | |
| D£® | ·ĄÖ¹ĖįÓź·¢ÉśµÄÖŲŅŖ“ėŹ©Ö®Ņ»ŹĒŹ¹ÓĆĒå½ąÄÜŌ“ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
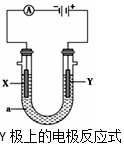 µē½āŌĄķŌŚ»Æѧ¹¤ŅµÖŠÓŠ¹ć·ŗÓ¦ÓĆ£®øł¾ŻČēĶ¼×°ÖĆ£¬»Ų“šŅŌĻĀĪŹĢā£ŗ
µē½āŌĄķŌŚ»Æѧ¹¤ŅµÖŠÓŠ¹ć·ŗÓ¦ÓĆ£®øł¾ŻČēĶ¼×°ÖĆ£¬»Ų“šŅŌĻĀĪŹĢā£ŗ| ·½°ø | X | Y | aČÜŅŗ |
| A | Ņų | ŹÆÄ« | AgNO3 |
| B | Ņų | Ģś | AgNO3 |
| C | Ģś | Ņų | Fe£ØNO3£©3 |
| D | Ģś | Ņų | AgNO3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | pH=7µÄČÜŅŗ | |
| B£® | c£ØH+£©=c£ØOH-£©=10-6mol/LČÜŅŗ | |
| C£® | “×ĖįÄĘČÜŅŗ | |
| D£® | ĖįÓė¼īĒ”ŗĆĶźČ«·“Ӧɜ³ÉÕżŃĪµÄČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | MgOŗĶAl2O3ŌŚ¹¤ŅµÉĻÓĆÓŚÖĘ×÷ÄĶøßĪĀ²ÄĮĻ£¬Ņ²æÉÓĆÓŚµē½ā·ØŅ±Į¶Mg”¢Al | |
| B£® | Ė®ÄąŅ±½š³§³£ÓĆøßŃ¹µē³żČ„¹¤³§ŃĢ³¾£¬ĄūÓĆĮĖ½ŗĢåµÄŠŌÖŹ | |
| C£® | øß“æ¶ČµÄ¶žŃõ»Æ¹č¹ć·ŗÓĆÓŚÖĘ×÷¹āµ¼ĻĖĪ¬£¬¹āµ¼ĻĖĪ¬ÓöĒæ¼ī»į”°¶ĻĀ·”± | |
| D£® | øßĢśĖį¼Ų£ØK2FeO4£©ŹĒŅ»ÖÖŠĀŠĶ”¢øߊ§”¢¶ą¹¦ÄÜĖ®“¦Ąķ¼Į£¬¼ČÄÜɱ¾śĻū¶¾ÓÖÄܾ»Ė® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·ÖŅŗ”¢ŻĶČ””¢ÕōĮó | B£® | ·ÖŅŗ”¢ÕōĮó”¢ŻĶČ” | C£® | ÕōĮó”¢ŻĶČ””¢·ÖŅŗ | D£® | ŻĶČ””¢ÕōĮ󔢷ÖŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ČŻĘ÷±ąŗÅ | ĘšŹ¼Ź±ø÷ĪļÖŹĪļÖŹµÄĮæ/mol | “ļµ½Ę½ŗāŹ±ĢåĻµÄÜĮæµÄ±ä»Æ | ||
| A | B | C | ||
| ¢Ł | 2 | 1 | 0 | 0.75 Q kJ |
| ¢Ś | 0.4 | 0.2 | 1.6 | |
| A£® | ČŻĘ÷¢Ł”¢¢ŚÖŠµÄĘ½ŗā³£Źż¾łĪŖ36 | |
| B£® | ĻņČŻĘ÷¢ŁÖŠĶØČėŗ¤Ęų£¬Ę½ŗāŹ±AµÄ×Ŗ»ÆĀŹ²»±ä | |
| C£® | ČŻĘ÷¢ŚÖŠ“ļµ½Ę½ŗāŹ±·Å³öµÄČČĮæĪŖ0.05 Q kJ£¬“ļµ½Ę½ŗāŹ±£¬Į½øöČŻĘ÷ÖŠCµÄĪļÖŹµÄĮæÅØ¶Č¾łĪŖ1.5 mol•L-1 | |
| D£® | ĘäĖūĢõ¼ž²»±ä£¬ČōČŻĘ÷¢Ś±£³ÖŗćČŻ¾ųČČ£¬Ōņ“ļµ½Ę½ŗāŹ±CµÄĢå»ż·ÖŹżŠ”ÓŚ2/3 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com