
下列叙述正确的是
A.新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色
B.加水稀释溶液,溶液中的所有离子浓度都减小
C.金属铝的生产是以Al2O3为原料,在熔融状态下进行电解
D.NaHCO3溶液中含有少量Na2CO3可以用澄清石灰水除去
科目:高中化学 来源: 题型:
将标准状况下的a L HCl (g)溶于1000 g水中,得到的盐酸密度为b g·cm―3,则该盐酸的物质的量浓度是( )
A.a/22.4 mol·L―1 B.ab/22400 mol·L―1
C.ab/(22400+36.5 a) mol/L D.1000 ab/(22400+36.5 a) mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-、HCO3-等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀物质的量随NaOH溶液的体积变化的图象如图所示,下列说法正确的是( )
A.原溶液中含有的Fe3+和Al3+的物质的量之比为1:1
B.ab段发生的离子反应为:Al3++3OH-= Al(OH)3↓,Mg2++2OH-= Mg(OH)2↓
C.原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+、Na+
D.d点溶液中含有的溶质只有Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
相同物质的量的下列物质:①金属钠 ②烧碱 ③过氧化钠 ④氧化钠,长期放置在空气中(不考虑潮解和水解),最后质量都会增加,按增加的质量由大到小排列,正确的是( )
A. ①>②>④>③ B. ①>②>③>④ C. ④>①>③>② D. ④>①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
用所学的化学知识,回答下列问题:
(1)从海水中提取镁的主要步骤有:①浓缩结晶(在HCl气流中) ②加熟石灰 ③加盐酸
④过滤 ⑤熔融电解,请按照顺序写出正确的操作步骤(填序号):____________________
(2) 化学方程式(未配平)As2S3 +H2O+NO3- = AsO43-+NO+ _______+SO42-,回答下面的问题:
a. 反应后溶液显_____性(写酸、碱、中);
b. 每1mol水参加反应,该反应转移电子的数目为_______
(3) 向过量的FeSO4溶液中加入几滴NaClO溶液,并且加入少量稀硫酸,发现溶液变成黄色。某同学认为该反应的还原产物有两种可能性,可能是Cl2或Cl-;而实验证明还原产物只存在Cl- 。回答下列问题:
a. 还原产物中不存在氯气的原因是__________________________ (用化学用语表示)
b. 写出上述过程的离子方程式____________________________________
c. 为了检验上述反应是否生成了Cl-,请从下面选择合适的序号,并按照先后顺序排列,进行实验操作。则正确的操作顺序为__________________
A. 取一支试管,加入上述反应后的溶液的少许;B. 加入过量的氯化钡溶液;C. 加入过量的硝酸钡溶液; D. 加入硝酸酸化的硝酸银溶液,观察到白色沉淀;E. 过滤,取滤液
查看答案和解析>>
科目:高中化学 来源: 题型:
Ba(NO3)2可用于生产绿色烟花、绿色信号弹、炸药、陶瓷釉药等。钡盐生产中排出大量的钡泥[主要含有BaCO3、BaSO3、Ba (FeO2)2等],某主要生产BaCO3、BaSO4的化工厂利用钡泥制取Ba(NO3)2晶体(不含结晶水),其部分工艺流程如下:
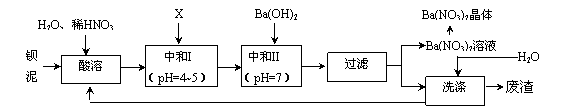
已知:①Fe3+和Fe2+以氢氧化物形式沉淀完全时,溶液的pH分别为3.2和9.7;
②Ba(NO3)2晶体的分解温度:592℃;
③kSP(BaSO4)=l.l×l 0-10,kSP (BaCO3)=5 .l×l0-9。
(1)该厂生产的BaCO3因含有少量BaSO4而不纯,提纯的方法是:将产品加入足量的饱和Na2CO3溶液中,充分搅拌,过滤,洗涤。试用离子方程式说明提纯原理_____________________________________________________________。
(2)上述流程中酸溶时,Ba(FeO2)2与HNO3反应生成两种硝酸盐,反应的化学方程式为_______________________________________________。
(3)该厂结合实际,图中X应选用_____________(填字母)。
A.BaCl2 B.BaCO3 C.Ba(NO3) 2 D.Ba(OH) 2
(4)中和I使溶液的pH为4~5的目的是________________________________;结合离子方程式简述其原理:________________________________。
(5)从Ba(NO3)2溶液中获得其晶体的操作方法是_____________________。
(6)测定所得Ba(NO3)2晶体的纯度:准确称取wg晶体溶于蒸馏水,加入足量的硫酸,充分反应后,过滤、洗涤、干燥,称量其质量为m g,则该晶体的纯度为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生将一小块钠投入滴有酚酞的水中,此实验能证明钠具有下列性质中的( )
①钠密度比水小 ②钠的熔点较低 ③钠与水反应时要放出热量 ④钠与水反应后溶液呈碱性
A.①④ B.①②④
C.①③④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
矿泉水目前已经成为人们常用的饮料,市场上有些不法商贩为牟取暴利,用自来水冒充矿泉水出售,为辨别真假,可用下列的一种化学试剂来鉴别,该试剂是( )
A.酚酞试液 B.氯化钡溶液
C.氢氧化钠溶液 D.硝酸银溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
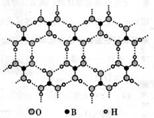 硼酸晶体具有层状结构,每一层的结构结构如右图所示。
硼酸晶体具有层状结构,每一层的结构结构如右图所示。
(1) 硼酸晶体属于____________晶体
(2) 硼酸晶体中,B的杂化轨道类型是____________。
(3) 硼酸晶体内所含有作用力类型有
________________________________________________。
(4)硼酸与水作用时,硼原子与水电离产生的OH—以配位键结合形成Y—离子,导致溶液中C(H+) >c(OH-),Y—离子中的配位键可以表示为______________________。
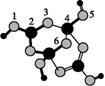 (5) 硼酸与氢氧化钠反应后,将溶液蒸发结晶,可以得到硼砂。硼砂阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示:
(5) 硼酸与氢氧化钠反应后,将溶液蒸发结晶,可以得到硼砂。硼砂阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示:
Xm-的化学式为____________________。
② Xm-离子内部______(填“有”或“没有”配位键),判断的理由是
___________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com