
| A、电解熔融AlCl3获取金属铝 |
| B、电解MgCl2溶液获取金属镁 |
| C、用CO还原铁矿石来获取金属铁 |
| D、电解饱和食盐水来获取金属钠 |


科目:高中化学 来源: 题型:
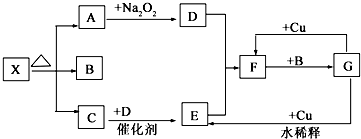 如图的各方框表示有关的一种反应物或生成物(某些物质已略去),其中常温下A、C、D为无色气体,C能使湿润的红色石蕊试纸变蓝,X中阴阳离子个数相等.
如图的各方框表示有关的一种反应物或生成物(某些物质已略去),其中常温下A、C、D为无色气体,C能使湿润的红色石蕊试纸变蓝,X中阴阳离子个数相等.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,11.2L四氯化碳所含分子数为0.5NA |
| B、0.1molNa2O2与足量CO2反应,转移电子数为0.1NA |
| C、1L 1mol?L-1的FeCl3溶液中Fe3+的数目小于NA |
| D、在标准状况下,11.2L氖气中含有氖原子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.0 | 3.0 |
| Fe2+ | 5.8 | 8.8 |
| Cu2+ | 4.2 | 6.7 |
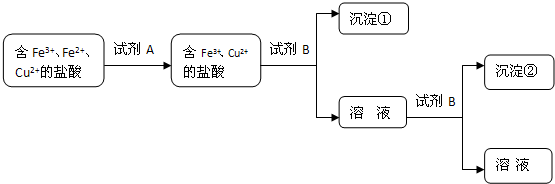
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②④ | B、③⑥⑦ |
| C、②⑤⑦ | D、①③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某化合物溶于水导电,则该化合物为电解质 |
| B、NaCl溶液在电流作用下电离成Na+和Cl- |
| C、在氧化还原反应中,非金属单质一定是氧化剂 |
| D、元素由化合态变成游离态时,它可能被氧化,也可能被还原 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com