
某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列有关叙述正确的是
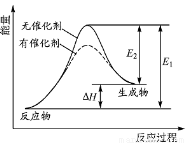
A.该反应为放热反应
B.催化剂能改变反应的焓变
C.催化剂能降低反应的活化能
D.逆反应的活化能大于正反应的活化能
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源:2014秋湖北省武汉市高一上学期期中联考化学试卷(解析版) 题型:选择题
(7分)含有相同氧原子数的CO和CO2两份气体
(1)其质量之比为______,其碳原子数之比为______,其原子数比为_______。
(2)同温同压时,其体积之比为______,密度之比为______。
(3)同温同体积时,其压强之比为_____,密度之比为______。
查看答案和解析>>
科目:高中化学 来源:2014秋浙江省杭州地区六校高二上学期期中考试化学试卷(解析版) 题型:计算题
(6分)在一定温度下,将2molA和2molB两种气体混合放入体积为2L的密闭刚性容器中,发生如下反应:3A(g)+B(g)  xC(g)+2D(g) △H<0,2min末反应达到平衡,生成0.8molD,并测得C的浓度为0.4mol?L-1。请回答:
xC(g)+2D(g) △H<0,2min末反应达到平衡,生成0.8molD,并测得C的浓度为0.4mol?L-1。请回答:
(1)x的值为_______
(2)A的转化率为α(A)%=______ ________
(3)此温度下该反应的平衡常数K=
查看答案和解析>>
科目:高中化学 来源:2014秋浙江省杭州地区六校高二上学期期中考试化学试卷(解析版) 题型:选择题
有关下图及实验的描述不正确的是
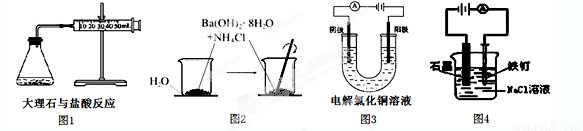
A.图1的实验可以测量大理石与盐酸的反应速率
B.图2的实验说明吸热反应也可能是自发反应
C.图3的两个电极都为铜片时,电解初期溶液的浓度基本不改变
D.图4的实验中,铁钉上会有刺激性气体产生
查看答案和解析>>
科目:高中化学 来源:2014秋浙江省杭州地区六校高二上学期期中考试化学试卷(解析版) 题型:选择题
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O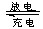 3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述不正确的是:
3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述不正确的是:
A.放电时负极反应为: Zn-2e―+2OH―=Zn(OH)2
B.充电时阳极反应为:Fe(OH)3-3e―+5OH―=FeO42-+4H2O
C.放电时每转移3mol电子,正极有1molK2FeO4被氧化
D.放电时的正极在充电时须接电源正极
查看答案和解析>>
科目:高中化学 来源:2014秋浙江省杭州地区六校高二上学期期中考试化学试卷(解析版) 题型:选择题
美籍华裔科学家钱永健曾于2008年获得诺贝尔化学奖。16岁时,他凭借一个金属易受硫氰酸盐腐蚀的调查项目,荣获有“少年诺贝尔奖”之称的著名奖项。下列说法正确的是:
A.金属的电化学腐蚀和化学腐蚀都是金属原子失去电子而被还原的过程;
B.钢铁发生电化学腐蚀时,其先发生反应:Fe-3e- = Fe3+,继而形成铁锈;
C.减少钢铁中的含碳量,可以增强钢铁的耐腐蚀能力。
D.金属的腐蚀会给社会带来巨大损失,所以金属的腐蚀是百害无一利的。
查看答案和解析>>
科目:高中化学 来源:2014秋浙江省杭州地区六校高一上学期期中考试化学试卷(解析版) 题型:选择题
下列除杂所选用的试剂及操作方法均正确的一组是(括号内为杂质)
选项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
A | NaCl(Na2CO3) | 盐酸 | 蒸发结晶 |
B | CO2(CO) | O2 | 点燃 |
C | Zn (Cu) | 稀硫酸 | 过滤 |
D | 溴(水) | 酒精 | 萃取 |
查看答案和解析>>
科目:高中化学 来源:2014秋河北省高二上学期期中化学试卷(解析版) 题型:填空题
(本题8分)汽车尾气是造成雾霾天气的重要原因之一。已知:
①N2(g)+O2(g)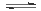 2NO(g) ΔH1 ②2NO(g)+O2(g)
2NO(g) ΔH1 ②2NO(g)+O2(g)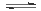 2NO2(g) ΔH2
2NO2(g) ΔH2
③CO2(g)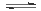 CO(g)+1/2O2(g) ΔH3 ④2CO(g)+2NO(g)
CO(g)+1/2O2(g) ΔH3 ④2CO(g)+2NO(g)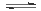 N2(g)+2CO2(g) ΔH4
N2(g)+2CO2(g) ΔH4
请完成以下问题:
(1)请根据反应①②③,确定反应④中ΔH4= 。
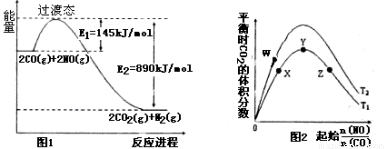
(2)根据图1,反应④的热化学方程式为: 。
该反应在 (填“高温”“低温”或“任意温度”)下有利于该反应正向自发。
(3)图2表示反应④的反应物NO、CO的起始物质的量比、温度对平衡时CO2的体积分数的影响。
①W、Y、Z三点的平衡常数的大小关系为: , X、Y、Z三点,CO的转化率由大到小的顺序是 。
②T1℃时,在1L密闭容器中,0.1molCO和0.1molNO,达到Y点时,测得NO的浓度为0.02mol/L,则此温度下平衡常数K= (算出数值)。若此温度下,某时刻测得CO、NO、N2、CO2的浓度分别为0.01 mol/L、a mol/L、0.01 mol/L、0.04 mol/L,要使反应向正方向进行,a的取值范围为 。
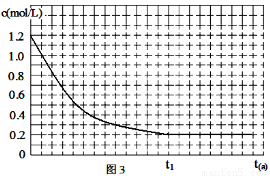
(4)恒温恒容时,反应④中NO、CO按一定比例投料,反应过程中CO浓度随时间的变化关系如图3所示,请在同一图中绘出N2浓度随时间的变化曲线。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com