
现有如下两个反应:
A. NaOH+HCl=NaCl+H2O B. 2FeCl3+Cu=2FeCl2+CuCl2
(1)根据两反应本质,判断能否设计成原电池:
A._________,B.__________(选择“能”或“不能”);
(2)如果可以,则写出正、负极材料及其电极反应式:
负极材料________,电极反应式_______________,
正极材料________,电极反应式_______________。
(8分)(1)(A)不能 (B)能;
(2)负极:铜,Cu-2e﹣=Cu2+;正极:碳棒,2Fe3++2e﹣=2Fe2+。
解析试题分析:(1)只有氧化还原反应才能设计成原电池,据此可知选项B可以,A是中和反应,不能设计成原电池。
(2)原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。所以根据反应的化学方程式可知,铜是负极,失去电子,电极反应式是,Cu-2e﹣=Cu2+;正极可以是碳棒,溶液中的铁离子在正极得到电子,电极反应式是2Fe3++2e﹣=2Fe2+。
考点:考查原电池构成以及原电池组成的有关判断
点评:该题主要是考查学生对原电池原理的熟悉了解程度,意在检验学生灵活运用基础知识解决实际问题的能力。该题的关键是明确原电池的工作原理和构成条件,并能结合题意灵活运用即可。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
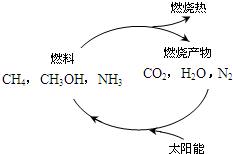 能源是当今社会发展的三大支柱之一.
能源是当今社会发展的三大支柱之一.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com