
分析 (1)灼烧时使用的仪器为坩埚;
(2)“搅拌、煮沸”可加快离子的溶解;
(3)H2O2溶液具有氧化性,二氧化锰也有氧化性,将碘离子氧化为碘单质,本身被还原为二甲锰离子;
(4)滴加溶液甲,溶液显蓝色,结合碘遇淀粉变蓝来解答.
解答 解:(1)灼烧时使用的仪器为坩埚,则选b来灼烧,故答案为:b;
(2)“搅拌、煮沸”可加快离子的溶解,使使I-充分溶解,故答案为:使I-充分溶解;
(3)H2O2溶液具有氧化性,能将I-氧化成I2,二氧化锰也有氧化性,将碘离子氧化为碘单质,本身被还原为二甲锰离子,反应为MnO2+2I-+4H+=Mn2++I2+2H2O,
故答案为:将I-氧化成I2;MnO2+2I-+4H+=Mn2++I2+2H2O;
(4)滴加溶液甲,溶液显蓝色,由碘遇淀粉变蓝,则甲为淀粉,故答案为:淀粉.
点评 本题以海水提碘考查混合物的分离、提纯,明确实验步骤中需要的仪器及发生的反应即可解答,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 饱和(NH4)2SO4、CuSO4溶液都能使蛋白质溶液发生盐析 | |
| B. | 肥皂能去污的原理,是其在水溶液中能电离出钠离子(亲水基团)和硬脂酸根离子(亲油基团),在它们的共同作用下,通过搓洗,将衣服上的油污“拖下水” | |
| C. | 糖类、油脂和蛋白质都是天然高分子化合物 | |
| D. | 福尔马林、葡萄糖都能发生银镜反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 混合溶液 | A | B | C | D | E | F |
| 4mol•L-1 H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | W | Z | 反应体系能量变化 | |
| 甲 | 2mol | 1mol | 放出akJ/mol | ||
| 乙 | 1mol | 1mol | 放出bkJ/mol | ||
| 丙 | 2mol | 2mol | 放出ckJ/mol | ||
| 丁 | 3mol | 2mol | 吸收dkJ/mol |
| A. | c+d<Q | |
| B. | 平衡时,甲、丁容器中X、W的转化率之和大于1 | |
| C. | 平衡时丙容器中Z的物质的量浓度最大 | |
| D. | X的转化率为:甲<乙<丙 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
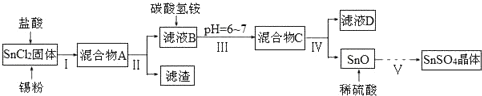
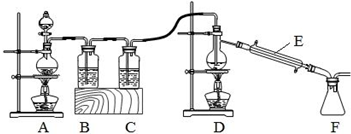
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
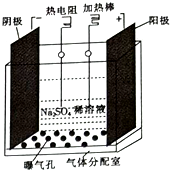 过氧化氢是实验室常用的试剂,在医疗、军事及工业上用途也非常广泛.回答下列问题:
过氧化氢是实验室常用的试剂,在医疗、军事及工业上用途也非常广泛.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com