
 A��B��C��D ����ѧ��ѧ���������ֵ��ʣ��ס��ҡ���Ϊ���ֻ�������ڳ�����Ϊ��ɫ��ζ��Һ�壬�������ʼ�ת����ϵ��ͼ����Ӧ��������ȥ��������գ�
A��B��C��D ����ѧ��ѧ���������ֵ��ʣ��ס��ҡ���Ϊ���ֻ�������ڳ�����Ϊ��ɫ��ζ��Һ�壬�������ʼ�ת����ϵ��ͼ����Ӧ��������ȥ��������գ� ���ʴ�Ϊ���ģ�
���ʴ�Ϊ���ģ� ��
��
| ||
| ||
| ||
| ||


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��84gNaHCO3�������NA��CO32- |
| B��1 mol Fe��������Fe2+ʧȥ������Ϊ2NA |
| C����״���£�11.2L���ȼ�������������Ϊ0.5NA |
| D��������ȼ�ϵ����ÿ����1molˮת�Ƶĵ�����ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
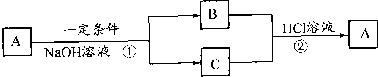
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��ѧʽ | ���볣�� |
| HClO | Ki=3��10-8 |
| H2CO3 | Ki1=4.3��10-7 |
| Ki2=5.6��10-11 |
| A��c��Na+����c��HCO3-��+c��ClO-��+2c��CO32-�� |
| B��c��ClO-����c��HCO3-����c��H+�� |
| C��c��HClO��+c��ClO-��=c��HCO3-��+c��CO32-��+c��H2CO3�� |
| D��c��Na+��+c��H+��=c��HCO3-��+c��ClO-��+c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��AgNO3��Һ�мӹ����İ�ˮ��Ag++NH3?H2O�TAgOH��+NH4+ |
| B����AgCl����Һ�еμ�������Һ����ɫ������ɺ�ɫ��2AgCl+S2-�TAg2S+2Cl- |
| C��FeS��������ϡHNO3��FeS+2H+�TFe2++H2S�� |
| D����NaHSO4��Һ�еμ�Ba��OH��2�����ԣ�H++SO4-+Ba2++OH-�TBaSO4��+H2O |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com