
 碳是形成物种最多的元素之一,许多含碳物质对人类极其重要.
碳是形成物种最多的元素之一,许多含碳物质对人类极其重要.| 时间/min | 0 | 10 | 20 | 30 |
| n(C8H10)/mol | 0.40 | 0.30 | 0.26 | n2 |
分析 (1)一个碳原子参与三个碳的形成,所以形成一个六元环,需要碳原子的个数为:6×$\frac{1}{3}$=2,由此分析解答;
(2)①可以从加快化学反应速率和平衡移动的角度分析解答;
②根据盖斯定律分析求解;
(3)①平衡时的量比20min的量小,但变化量小于10min-20min,所以0.22<n<0.26;
②根据三行式求变化量;
(4)葡萄糖到葡萄糖酸[CH2OH(CHOH)4COOH]发生氧化反应,所以在阳极产生,电极反应式为:CH2OH(CHOH)4CHO+H2O-2e-═CH2OH(CHOH)4COOH+2H+.
解答 解:(1)一个碳原子参与三个碳的形成,所以形成一个六元环,需要碳原子的个数为:6×$\frac{1}{3}$=2,所以12g石墨烯物质的量为1mol,所以形成6元环的物质的量为:$\frac{1}{2}$mol,即0.5NA个6元环,故答案为:0.5NA;
(2)①CH4+$\frac{1}{2}$O2(g)?CH3OH(g)△H=-128.5kJ/mol,正反应是气体体积减少的反应,所以可以通增大压强、选用合适的催化剂,
故答案为:增大压强、选用合适的催化剂;
②由CH4+$\frac{1}{2}$O2(g)?CH3OH(g)△H=-128.5kJ/mol…Ⅰ,CH4(g)+O2(g)→HCHO(g)+H2O(g)△H=c kJ/mol…Ⅱ,目标反应CH3OH(g)+$\frac{1}{2}$O2(g)→HCHO(g)+H2O(g),得Ⅱ-Ⅰ得:CH3OH(g)+$\frac{1}{2}$O2(g)→HCHO(g)+H2O(g)△H=(c+128.5)KJ•L-1,
故答案为:CH3OH(g)+$\frac{1}{2}$O2(g)→HCHO(g)+H2O(g)△H=(c+128.5)KJ•L-1;
(3)①平衡时的量比20min的量小,但变化量小于10min-20min,所以0.22<n<0.26,故答案为:0.22<n<0.26;
②C8H10(g)?C8H8(g)+H2(g)
开始 0.40mol 0 0
变化 x x x
平衡0.40mol-x x x
所以:$\frac{0.4+x}{0.4}$=1.4,解之得:x=0.16,所以苯乙烷的转化率为$\frac{0.16}{0.4}×100%$=40%,故答案为:40%;
(4)葡萄糖到葡萄糖酸[CH2OH(CHOH)4COOH]发生氧化反应,所以在阳极产生,电极反应式为:CH2OH(CHOH)4CHO+H2O-2e-═CH2OH(CHOH)4COOH+2H+;
故答案为:阳;CH2OH(CHOH)4CHO+H2O-2e-═CH2OH(CHOH)4COOH+2H+.
点评 本题考查外界条件对化学平衡的影响、盖斯定律、三行式的应用和电极反应式的书写,综合性强,有一定的难度.


 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将纯水加热到950C时,Kw变大,pH不变,水仍呈中性 | |
| B. | 向纯水中加入稀氨水,平衡逆向移动,c(OH-)增大,Kw变小 | |
| C. | 向水中加入少量固体硫酸氢钠,c(H+)增大,平衡逆向移动,KW不变 | |
| D. | 向水中通入HCl气体,平衡逆向移动,溶液导电能力减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,NaA溶液的pH=8,则c(Na+)-c(A-)=9.9×10-7 | |
| B. | pH=5.6的CH3COOH与CH3COONa混合溶液中,c(Na+)>(CH3COO-) | |
| C. | 0.1mol•L-1的NaHSO3的溶液中C(Na+)>C(HSO3-)>C(H+)>C(SO32-)>C(OH-) | |
| D. | 浓度均为0.1mol/L的 CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)] |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式C2H4 | B. | 丁烷的结构简式CH3(CH2)2CH3 | ||
| C. | 四氯化碳的电子式 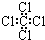 | D. | 环己烷的键线式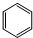 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18.6g | B. | 20g | C. | 19.4g | D. | 24g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “冰十六”的密度比液态水小 | B. | “冰十六”与干冰由不同分子构成 | ||
| C. | “冰十六”可以包合气体分子 | D. | 液态水转变成“冰十六”是化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
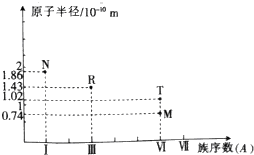
| A. | 常压下,单质R的熔点高于单质M的熔点 | |
| B. | R、T的简单离子都会破坏水的电离平衡 | |
| C. | N2M2与R2M3中所含化学键的类型完全相同 | |
| D. | N、R、T的最高价氧化物对应的水化物之间能相互反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com