
| A. | 氧化剂与还原剂的物质的量之比为1:8 | |
| B. | 还原产物为NH4+ | |
| C. | 若有1molNO3-参加还原反应,转移8mol e- | |
| D. | 该反应中H2O是反应物之一 |
分析 Fe2+具有还原性,NO3-在酸性条件下具有强氧化性,由题意可以确定,铁元素的化合价升高,N元素的化合价降低,则发生反应8Fe2++NO3-+10H+=8Fe3++NH4++3H2O.
A、该反应中氧化剂是NO3-,还原剂是Fe2+,结合方程式判断氧化剂与还原剂的物质的量之比;
B、氧化剂通过还原反应生成的产物为还原产物.反应中N元素的化合价由NO3-中+5价降低为NH4+中-3价;
C、反应中N元素的化合价由NO3-中+5价降低为NH4+中-3价,据此计算有lmolNO3- 发生还原反应转移电子数;
D、根据以上分析,H2O是生成物之一.
解答 解:Fe2+具有还原性,NO3-在酸性条件下具有强氧化性,由题意可以确定,铁元素的化合价升高,N元素的化合价降低,则发生反应8Fe2++NO3-+10H+=8Fe3++NH4++3H2O.
A、由方程式可知该反应中氧化剂(NO3-)与还原剂(Fe2+)物质的量之比为1:8,故A正确;
B、反应中N元素的化合价由NO3-中+5价降低为NH4+中-3价,NH4+是还原产物,故B正确;
C、反应中N元素的化合价由NO3-中+5价降低为NH4+中-3价,所以有lmolNO3- 发生还原反应,转移电子数为1mol×[5-(-3)]=8mol,故C正确;
D、根据以上分析,H2O是生成物之一,故D错误,
故选:D.
点评 本题考查氧化还原反应,难度中等,根据反应物和生成物结合物质的性质书写该反应的离子方程式是解答关键.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 原子数 | B. | 密度 | C. | 质子数 | D. | 质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 往新配制的可溶性淀粉溶液中滴加碘水,溶液显蓝色,用CCl4不能从中萃取出碘 | |
| B. | 硝酸钾饱和溶液冷却未出现结晶时,可以用玻棒充分磨擦器皿壁促使晶体析出 | |
| C. | 制备硫酸亚铁铵晶体时,最后在蒸发皿中蒸发浓缩溶液时,只需小火加热至溶液表面出现晶膜为止,不能将溶液全部蒸干 | |
| D. | 重结晶时,溶液冷却速度越慢得到的晶体颗粒越小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑥ | B. | ②③⑥ | C. | ①②④ | D. | ②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2+、H+、Na+、NO3- | B. | SiO32-、K+、Br-、H+ | ||
| C. | NH4+、Cl-、Mg2+、SO42- | D. | Na+、OH-、NH4+、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 中和热(△H)的测定中,若使用简易装置时在大小烧杯之间没有垫碎泡沫塑料(或纸条) | |
| B. | 用标准盐酸滴定氢氧化钠溶液,酸式滴定管洗净后,没有用标准盐酸润洗,所测出的碱液的浓度值 | |
| C. | 食醋总酸含量测定实验中,用移液管移取食醋体积时视线俯视标准线移液 | |
| D. | 在镀锌铁皮的锌镀层厚度的测定中,锌在酸中溶解后没有及时取出 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L SO3的分子数为1NA | |
| B. | 3.9g Na2O2固体中阴离子的数目为0.1NA | |
| C. | 1mol Cl2与1mol Fe反应,转移的电子数为2NA | |
| D. | 0.1molN2和C18O含有的中子数均为1.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
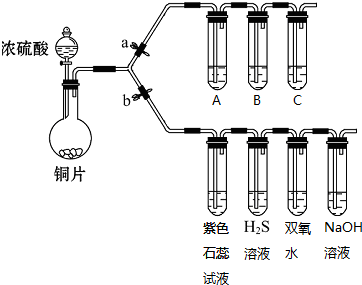
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com