
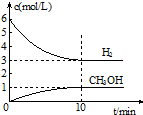
 T℃时,在1L的密闭容器中充入2mol CO2和6mol H2,发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1.测得H2和CH3OH(g)的浓度随时间变化情况如图所示:下列说法不正确的是( )
T℃时,在1L的密闭容器中充入2mol CO2和6mol H2,发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1.测得H2和CH3OH(g)的浓度随时间变化情况如图所示:下列说法不正确的是( )| A. | 0~10min内v(H2)=0.3 mol•L-1•min-1 | |
| B. | T℃时,平衡常数K=$\frac{1}{27}$,CO2与H2的转化率相等 | |
| C. | T℃时,当有32 g CH3OH生成时,放出49.0 kJ的热量 | |
| D. | 达到平衡后,升高温度或再充入CO2气体,都可以提高H2的转化率 |
分析 结合图可知浓度的变化,则
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
开始 2 6 0 0
转化 1 3 1 1
平衡 1 3 1 1
A.结合v=$\frac{△c}{△t}$计算;
B.K为生成物浓度幂之积与反应物浓度幂之积的比,起始量之比等于化学计量数之比;
C.n(CH3OH)=$\frac{32g}{32g/mol}$=1mol,物质的量与反应中热量变化成正比;
D.该反应为放热反应,升高温度平衡逆向移动;充入CO2气体平衡正向移动.
解答 解:结合图可知浓度的变化,则
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
开始 2 6 0 0
转化 1 3 1 1
平衡 1 3 1 1
A.0~10min内v(H2)=$\frac{3mol/L}{10min}$=0.3 mol•L-1•min-1,故A正确;
B.T℃时,平衡常数K=$\frac{1×1}{1×{3}^{3}}$=$\frac{1}{27}$,起始量之比等于化学计量数之比,则CO2与H2的转化率相等,故B正确;
C.n(CH3OH)=$\frac{32g}{32g/mol}$=1mol,物质的量与反应中热量变化成正比,则当有32 g CH3OH生成时,放出49.0 kJ的热量,故C正确;
D.该反应为放热反应,升高温度平衡逆向移动,H2的转化率减小;充入CO2气体平衡正向移动,H2的转化率增大,故D错误;
故选D.
点评 本题考查化学平衡的计算及平衡移动,为高频考点,把握图中浓度变化、平衡移动的影响因素为解答的关键,侧重分析与应用能力的考查,注意K的计算及平衡移动的应用,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 用托盘天平称取NaCl固体2.9 g | |
| B. | 胶头滴管加水定容时,有少量水滴到容量瓶外 | |
| C. | 定容时俯视读数 | |
| D. | 称量固体时,天平的两个托盘上放两张质量相等的纸片,其他操作均正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com