
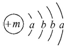 ,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.
,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.| 元素 | Al | B | Be | C | Cl | F | Li | Mg | N | Na | O | P | S | Si |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 2.8 | 4.0 | 1.0 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 |
分析 X原子的结构示意图为 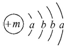 ,由于K最多容纳2个电子,L层最多容纳8个电子,可知a=2,b=8,故X为Ca元素;由化学XY2可知Y的化合价为-1价,而X的阳离子与Y的阴离子的电子层结构相同,离子核外电子数均为18,则Y原子核外电子数为17,故Y为Cl;元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,符合条件的元素有He、C、S,由于Z与Y相邻且Z、W能形成一种WZ2型分子,则Z为S元素,W为C元素,二者形成的分子为CS2,据此解答.
,由于K最多容纳2个电子,L层最多容纳8个电子,可知a=2,b=8,故X为Ca元素;由化学XY2可知Y的化合价为-1价,而X的阳离子与Y的阴离子的电子层结构相同,离子核外电子数均为18,则Y原子核外电子数为17,故Y为Cl;元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,符合条件的元素有He、C、S,由于Z与Y相邻且Z、W能形成一种WZ2型分子,则Z为S元素,W为C元素,二者形成的分子为CS2,据此解答.
解答 解:X原子的结构示意图为 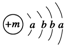 ,由于K最多容纳2个电子,L层最多容纳8个电子,可知a=2,b=8,故X为Ca元素;由化学XY2可知Y的化合价为-1价,而X的阳离子与Y的阴离子的电子层结构相同,离子核外电子数均为18,则Y原子核外电子数为17,故Y为Cl,则该融雪剂为CaCl2;元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,符合条件的元素有He、C、S,由于Z与Y相邻且Z、W能形成一种WZ2型分子,则Z为S元素,W为C元素,二者形成的分子为CS2.
,由于K最多容纳2个电子,L层最多容纳8个电子,可知a=2,b=8,故X为Ca元素;由化学XY2可知Y的化合价为-1价,而X的阳离子与Y的阴离子的电子层结构相同,离子核外电子数均为18,则Y原子核外电子数为17,故Y为Cl,则该融雪剂为CaCl2;元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,符合条件的元素有He、C、S,由于Z与Y相邻且Z、W能形成一种WZ2型分子,则Z为S元素,W为C元素,二者形成的分子为CS2.
(1)由上述分析可知,m=2+8+8+2=20,该融雪剂的化学式为CaCl2,故答案为:20;CaCl2;
(2)由上述分析可知,Z为硫元素、W为碳元素,故答案为:硫;碳;
(3)A.CaCl2属于离子化合物,而CS2是共价化合物,故A错误;
B.CaCl2中仅含离子键,CS2中只含共价键,且是极性共价键,故B正确;
C.因氯的非金属性强于硫,所以稳定性HCl>H2S,故C错误;
D.核外电子排布相同的离子,核电荷数越大,离子的半径越小,所以半径Ca2+<Cl-,故D错误,
故选:B;
(4)由表中数据可知,第二周期元素从Li~F,随着原子序数的递增,元素的电负性逐渐增大,第三周期元素从Na~Cl,随着原子序数的递增,元素的电负性也逐渐增大,并呈周期性变化,
故答案为:在同一周期中,随着原子序数的递增,元素的电负性逐渐增大,并呈周期性变化.
点评 本题考查的知识点较多,涉及核外电子排布、化学键、元素周期律、微粒半径比较等,难度不大,根据核外电子排布和原子结构推导出元素是解题的关键,(4)侧重学生对数据的分析处理、归纳总结能力的考查.


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
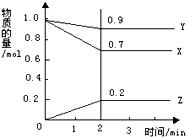 某温度下,在2L的密闭容器中,X、Y、Z三种物质随时间变化的曲线如图所示.由图中数据分析:该反应的化学方程式为:X+3Y?2Z.反应开始至2min,Z的平均反应速率为0.05mol/(L.min).
某温度下,在2L的密闭容器中,X、Y、Z三种物质随时间变化的曲线如图所示.由图中数据分析:该反应的化学方程式为:X+3Y?2Z.反应开始至2min,Z的平均反应速率为0.05mol/(L.min).查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 福尔马林具有防腐性,可用于制备酚醛树脂 | |
| B. | 甘油具有吸水性,可用作抗冻剂 | |
| C. | 乙酸乙酯能水解,可用于制备肥皂 | |
| D. | 淀粉水解能生成葡萄糖,可用于制备乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com