
【题目】查看下列酒类饮品的商品标签,其中酒精含量最高的是()
A. 啤酒 B. 白酒 C. 葡萄酒 D. 黄酒
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:高中化学 来源: 题型:
【题目】下列说法中,可以证明反应 N2+3H2![]() 2NH3 已达平衡状态的是( )
2NH3 已达平衡状态的是( )
A. 一个N≡N键断裂的同时,有三个H-H键形成
B. 一个N≡N键断裂的同时,有三个H-H键断裂
C. 一个N≡N键断裂的同时,有两个N-H键断裂
D. 一个N≡N键断裂的同时,有六个N-H键形成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为镁--次氯酸盐燃料电池的工作原理图,下列有关说法不正确的是

A. 该燃料电池中镁为负极,发生还原反应
B. 电池的总反应式为Mg+ClO-+H2O===Mg(OH)2↓+Cl-
C. 放电过程中OH-移向负极
D. 酸性电解质的镁--过氧化氢燃料电池正极反应为:H2O2+2H++2e-===2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种以30%KOH溶液为电解质的氢氧燃料电池的公共汽车已在北京街头出现。下列有关该氢氧燃料电池的说法中,正确的是( )
A. H2在正极发生氧化反应
B. 供电时的总反应为:2H2+O2![]() 2H2O
2H2O
C. 氢氧燃料电池不仅能量转化率高,而且产物是水,属于环境友好电池
D. 氢氧燃料电池中H2和O2燃烧放出的热量转变为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01 mol·L–1 r溶液的H+的浓度也是0.01 mol·L–1,s通常是难溶于水的有机混合物。上述物质的转化关系如图所示。下列说法正确的是( )
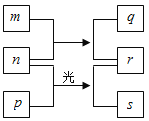
A. 原子半径的大小W<X<YB. 元素的非金属性Z>X>Y
C. Z的氧化物的水化物为强酸D. Y的氢化物常温常压下为液态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是实验室制取气体装置,其中发生装置相同(省去了铁架台和锥形瓶中的药品),干燥和收集装置有二套,分别用图一和图二。下列选项中不正确的是( )
A | 锌和稀盐酸 | 选用图1 |
B | 碳化钙和饱和食盐水 | 选用图1 |
C | 铜和浓硫酸 | 选用图2 |
D | 过氧化钠和水 | 选用图2 |

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E都是短周期元素,原子序数依次增大,A、D同主族,B、C、D、E同周期,B、A可按原子个数比2:l和1:1分别形成两种离子化合物甲和乙,C是地壳中含量最高的金属元素。短周期中,B原子半径最大,E的最高价氧化物对应水化物酸性最强。
(1)E的最高价氧化物对应的水化物的分子式为________________;
(2)D与E可形成分子式为D2E2的物质,该物质为浅黄色油状液体,有特殊气味,是一种重要的工业添加剂。则D2E2的结构式为______________;
(3)B、C、D、E、A简单离子半径由大到小的顺序为_______________(用离子符号表示)
(4)用电子式表示化合物甲的形成过程________;
(5)C元素的单质能与B元素的最高价氧化物的水化物发生反应,写出该反应离子方程式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了检验某溶液中是否含有常见的四种无机离子,某化学小组的同学进行了如下所示的实验操作。其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验能得出的正确结论是( )

A.原溶液中一定含有SO42- B.原溶液中一定含有NH4+
C.原溶液中一定含有Cl- D.原溶液中一定含有Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化镁是优良的阻燃剂,同时在医药、建筑等行业的应用也十分广泛。用硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量SiO2、FeCO3等)为原料制备高纯氧化镁的实验流程如下:

已知在水溶液中生成氢氧化物沉淀的pH:
Mg(OH)2 | Fe(OH)2 | Fe(OH)3 | |
开始沉淀时 | 9.4 | 7.6 | 1.5 |
完全沉淀时 | 10.4 | 9.7 | 2.8 |
(1)菱镁矿酸溶前需要粉碎,目的是_______________。
(2)加入H2O2氧化时,发生反应的离子方程式为______________________。
(3)加氨水调节溶液的pH范围为________ ,滤渣2 的主要成分是____________(填化学式)。
(4)流程图中在获得滤渣2的“过滤”与“煅烧”之间要经过的操作步骤为_______、过滤等操作,得到MgSO4·xH2O晶体。
(5)已知煅烧12.3gMgSO4·xH2O晶体得到2gMgO,则x值为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com