
| ���� | ���X-H��Y | ����kJ•mol-1 |
| ��HF��n | D-H��F | 28.1 |
| �� | O-H��O | 18.8 |
| ��NH3��n | N-H��N | 5.4 |
���� ��1��ͬһ����Ԫ���У�Ԫ�صĵ�һ����������ԭ����������������������ƣ�����IIA�塢��VA��Ԫ�ص�һ�����ܴ���ͬ��������Ԫ�صģ�
��2��ijԪ��λ�ڵ������ڢ��壬���̬ԭ�ӵ�δ�ɶԵ��������̬̼ԭ�ӵ�δ�ɶԵ�������ͬ��̼ԭ�ӵĵ����Ų�Ϊ1s22s22p2��δ�ɶԵ�����Ϊ2�����Ԫ��ΪNi��
��3����ϩͪ������̼ԭ�Ӿ�û�й¶Ե��ӣ�CH2��Cԭ���γ�3���Ҽ�����C=O��̼ԭ���γ�2���Ҽ����ӻ������Ŀ�ֱ�Ϊ3��2����C2H5O��3P=O���Ӻ���25���Ҽ���
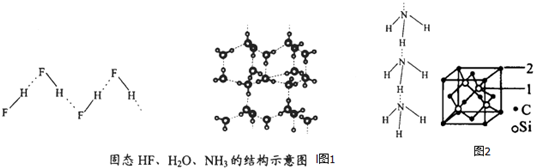
��4��ƽ��ÿ�����Ӻ������������2������HF��n�ͣ�NH3��nֻ��1�����������Ҫ�˷���������ܼ��ܣ�
��5�����ݾ�̯�����㾧����Si��Cԭ����Ŀ��ÿ��Siԭ����Χ��4��̼ԭ�ӣ�ԭ����λ����ԭ����Ŀ�ɷ��ȣ����Լ���̼ԭ����Χ�����������Ĺ�ԭ����Ŀ��
�Զ���Cԭ���о�����֮���������Cԭ��λ�������ϣ�ÿ������ԭ��Ϊ8���������ã�ÿ����Ϊ2���������ã�
����1��Siԭ�ӵ���Խ��ߡ�2��̼ԭ�ӵ���Խ��ߣ��ཻ��O�㣬�붥��̼ԭ���γ���ͼ��ʾ��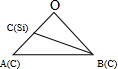 ������BΪ2��̼ԭ�ӣ�CΪ1��Siԭ�ӣ�1��Siԭ������Χ��4��Cԭ���γ��������壬1��Siԭ���붥��̼ԭ�����ߴ��ھ�����Խ����ϣ��Ҿ���Ϊ��Խ��߳��ȵ�$\frac{1}{4}$����Խ��߳���Ϊ$\sqrt{3}$a pm����OA=OB=$\frac{\sqrt{3}}{2}$a pm����OC=$\frac{\sqrt{3}}{4}$a pm���������Ҷ�������cos��AOB��ֵ�����������Ҷ�������BC�ij��ȣ�������ͼ2��1�Ź�ԭ�Ӻ�2��̼ԭ��֮��ľ��룻
������BΪ2��̼ԭ�ӣ�CΪ1��Siԭ�ӣ�1��Siԭ������Χ��4��Cԭ���γ��������壬1��Siԭ���붥��̼ԭ�����ߴ��ھ�����Խ����ϣ��Ҿ���Ϊ��Խ��߳��ȵ�$\frac{1}{4}$����Խ��߳���Ϊ$\sqrt{3}$a pm����OA=OB=$\frac{\sqrt{3}}{2}$a pm����OC=$\frac{\sqrt{3}}{4}$a pm���������Ҷ�������cos��AOB��ֵ�����������Ҷ�������BC�ij��ȣ�������ͼ2��1�Ź�ԭ�Ӻ�2��̼ԭ��֮��ľ��룻
��Ͼ�����ԭ����Ŀ����ʾ�������������ٸ��ݦ�=$\frac{m}{V}$���㾧���ܶȣ�
��� �⣺��1��ͬһ����Ԫ���У�Ԫ�صĵ�һ����������ԭ����������������������ƣ��������Nԭ�Ӻ�ȫ������Beԭ�ӵ�һ������Ҫ��ͬ��������Ԫ�صĸߣ��ʵ�һ�����ܽ���B��N֮��ĵڶ�����Ԫ����Be��C��O����Ԫ�أ�
�ʴ�Ϊ��3��
��2��ijԪ��λ�ڵ������ڢ��壬���̬ԭ�ӵ�δ�ɶԵ��������̬̼ԭ�ӵ�δ�ɶԵ�������ͬ��Cԭ�ӵĵ����Ų�Ϊ1s22s22p2��δ�ɶԵ�����Ϊ2�����Ԫ��ΪNi�����̬ԭ�ӵļ۲�����Ų�ʽΪ3d84s2��
�ʴ�Ϊ��3d84s2��
��3����ϩͪ������̼ԭ�Ӿ�û�й¶Ե��ӣ�CH2��Cԭ���γ�3���Ҽ�����C=O��̼ԭ���γ�2���Ҽ����ӻ������Ŀ�ֱ�Ϊ3��2������̼ԭ�ӵ��ӻ����������sp2��sp����C2H5O��3P=O���Ӻ���25���Ҽ���1mol��C2H5O��3P=O�����к��еĦҼ�����ĿΪ25NA��
�ʴ�Ϊ��sp2��sp��25NA��
��4����������ļ����ǣ�HF��n��������NH3��n����ƽ��ÿ�����Ӻ������������2������HF��n�ͣ�NH3��nֻ��1��������Ҫ�˷���������ܼ����DZ�����HF��n����NH3��n����H2O��HF��NH3�е����ν��ͣ�
�ʴ�Ϊ����������ļ����ǣ�HF��n��������NH3��n����ƽ��ÿ�����Ӻ������������2������HF��n�ͣ�NH3��nֻ��1��������Ҫ�˷���������ܼ����DZ�����HF��n����NH3��n��
��5��������Siԭ����ĿΪ4��Cԭ����ĿΪ8��$\frac{1}{8}$+6��$\frac{1}{2}$=4��ÿ��Siԭ����Χ��4��̼ԭ�ӣ�ԭ����λ����ԭ����Ŀ�ɷ��ȣ���̼ԭ����λ��Ҳ��4����̼ԭ����Χ�����������Ĺ�ԭ����ĿΪ4��
�Զ���Cԭ���о�����֮���������Cԭ��λ�������ϣ�ÿ������ԭ��Ϊ8���������ã�ÿ����Ϊ2���������ã���̼ԭ�ӵȾ��������̼ԭ����$\frac{8��3}{2}$=12����
����1��Siԭ�ӵ���Խ��ߡ�2��̼ԭ�ӵ���Խ��ߣ��ཻ��O�㣬�붥��̼ԭ���γ���ͼ��ʾ�� ������BΪ2��̼ԭ�ӣ�CΪ1��Siԭ�ӣ�1��Siԭ������Χ��4��Cԭ���γ��������壬1��Siԭ���붥��̼ԭ�����ߴ��ھ�����Խ����ϣ��Ҿ���Ϊ��Խ��߳��ȵ�$\frac{1}{4}$����Խ��߳���Ϊ$\sqrt{3}$a pm����OA=OB=$\frac{\sqrt{3}}{2}$a pm����OC=$\frac{\sqrt{3}}{4}$a pm����
������BΪ2��̼ԭ�ӣ�CΪ1��Siԭ�ӣ�1��Siԭ������Χ��4��Cԭ���γ��������壬1��Siԭ���붥��̼ԭ�����ߴ��ھ�����Խ����ϣ��Ҿ���Ϊ��Խ��߳��ȵ�$\frac{1}{4}$����Խ��߳���Ϊ$\sqrt{3}$a pm����OA=OB=$\frac{\sqrt{3}}{2}$a pm����OC=$\frac{\sqrt{3}}{4}$a pm����
��$\frac{\sqrt{3}}{2}$a��2+��$\frac{\sqrt{3}}{2}$a��2-2��$\frac{\sqrt{3}}{2}$a��$\frac{\sqrt{3}}{2}$a��cos��AOB=a2��
���cos��AOB=$\frac{1}{3}$
�ʣ�$\frac{\sqrt{3}}{4}$a��2+��$\frac{\sqrt{3}}{2}$a��2-2��$\frac{\sqrt{3}}{4}$a��$\frac{\sqrt{3}}{2}$a��$\frac{1}{3}$=BC2��
���BC=$\frac{\sqrt{11}a}{4}$
��������Ϊ4��$\frac{28+12}{{N}_{A}}$g�������ܶ�Ϊ4��$\frac{28+12}{{N}_{A}}$g�£�a��10-10 cm��3=$\frac{1.6��1{0}^{32}}{{a}^{3}��{N}_{A}}$g/cm3��
�ʴ�Ϊ��4��12��$\frac{\sqrt{11}a}{4}$��$\frac{1.6��1{0}^{32}}{{a}^{3}��{N}_{A}}$��
���� �����Ƕ����ʽṹ�����ʵĿ��飬�漰��������Ų��������ܡ��ӻ��������ѧ�����������������ȣ���4����5��Ϊ�״��㡢�ѵ㣬���ؿ���ѧ�����������������ѶȽϴ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ƿ������Ʊ�ľ�ķ���� | B�� | �赥�ʹ㷺���ڹ���ͨѶ | ||
| C�� | ������ɶ���������ˮ��Ӧ�Ƶ� | D�� | ˮ�������ǹ�������Ʒ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
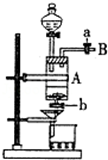 ���Ȼ�������ѧ��ѧʵ�����г��õĻ�ѧ�Լ���ͬѧ�����÷���м��������ͭ���ʣ���̽���Ʊ�FeCl3•6H2O�ķ�����ͬѧ����Ƶ�ʵ��װ����ͼ��ʾ����ʵ�鲽�����£�A�з��з���м���ձ���ʢ��������ϡ���ᣬʵ��ʱ�ȴ�a���ر�b���÷�Һ©����A�м�������������ַ�Ӧ����ʱ��Һ��dz��ɫ���ٴ�b���й��ˣ����˽�����ȡ�ձ�����Һ������������ȣ�����������ˮ��ʹʣ��HNO3�ֽ⣬�ٽ��½ᾧ��FeCl3•6H2O���壮
���Ȼ�������ѧ��ѧʵ�����г��õĻ�ѧ�Լ���ͬѧ�����÷���м��������ͭ���ʣ���̽���Ʊ�FeCl3•6H2O�ķ�����ͬѧ����Ƶ�ʵ��װ����ͼ��ʾ����ʵ�鲽�����£�A�з��з���м���ձ���ʢ��������ϡ���ᣬʵ��ʱ�ȴ�a���ر�b���÷�Һ©����A�м�������������ַ�Ӧ����ʱ��Һ��dz��ɫ���ٴ�b���й��ˣ����˽�����ȡ�ձ�����Һ������������ȣ�����������ˮ��ʹʣ��HNO3�ֽ⣬�ٽ��½ᾧ��FeCl3•6H2O���壮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ca��OH��2����ˮ������Ca��OH��2��������� | |
| B�� | ǿ�������Һ�ĵ����������ܱ����������Һ���������� | |
| C�� | Cu��NaCl��Һ���ǵ���ʣ������Ƿǵ���� | |
| D�� | SO3����ˮ�磬����SO3�ǵ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
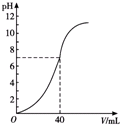 ��1mol•L-1NaOH��Һ�к�ijŨ�ȵ�������Һʱ����pH������NaOH��Һ�������ϵ��ͼ��ʾ��ԭ������Һ�����ʵ���Ũ�Ⱥͷ�Ӧ����Һ�������������仯���Բ��ƣ��ֱ��ǣ�������
��1mol•L-1NaOH��Һ�к�ijŨ�ȵ�������Һʱ����pH������NaOH��Һ�������ϵ��ͼ��ʾ��ԭ������Һ�����ʵ���Ũ�Ⱥͷ�Ӧ����Һ�������������仯���Բ��ƣ��ֱ��ǣ�������| A�� | 0.5 mol•L-1 100 mL | B�� | 0.5 mol•L-180 mL | ||
| C�� | 1 mol•L-160 mL | D�� | 1 mol•L-180 mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��H2SO40.2mol��Ũ������������Cu��Ӧ�ɲ���SO2������Ϊ0.1NA | |
| B�� | ����Fe��1 mol������Ӧ��ת�Ƶĵ�����Ϊ3NA | |
| C�� | ��״���£�22.4LSO3���з��ӵ���ĿΪNA�� | |
| D�� | 1molNa2O2������������Ϊ3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
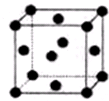 X��Y��Z��W��R����Ϊǰ������Ԫ����ԭ��������������X�Ļ�̬ԭ�Ӻ�����7�ֲ�ͬ�˶�״̬�ĵ��ӣ�Yԭ���������2�ԳɶԵ��ӣ�Z��ԭ������ΪY��ԭ��������2����W3+�Ļ�̬����3d���Ϊ�����״̬��R��������������Һ�����ڼ��������ǵĴ��ڣ�
X��Y��Z��W��R����Ϊǰ������Ԫ����ԭ��������������X�Ļ�̬ԭ�Ӻ�����7�ֲ�ͬ�˶�״̬�ĵ��ӣ�Yԭ���������2�ԳɶԵ��ӣ�Z��ԭ������ΪY��ԭ��������2����W3+�Ļ�̬����3d���Ϊ�����״̬��R��������������Һ�����ڼ��������ǵĴ��ڣ��鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com