
| A.单质Be与酸或碱反应都能放出氢气 | B.Be(OH)2为两性氢氧化物 |
| C.Be的氧化物的化学式为Be2O3 | D.BeCl2晶体属于分子晶体 |
科目:高中化学 来源:不详 题型:单选题
| A.除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数 |
| B.电离能最小的电子能量最高 |
| C.同是s能级,在不同的电子层中所能容纳的最多电子数是不相同的 |
| D.核外电子排布完全相同的两种微粒,其化学性质一定相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na+ < Mg2+ < Al3+ < F- | B.S2-< Cl-< Na+ < Al3+ |
| C.Na > Mg > Al > S | D.Cs < Rb < K < Na |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.三者原子半径大小顺序为X>Y>Z |
| B.分子组成为Y5Z12的物质一定为纯净物 |
| C.1.5molX2与2molY恰好完全反应时,可得到相同物质的量的两种氧化物 |
| D.实验室用Z2X2为原料可以制备X2,每转移2mol电子,得到22.4LX2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
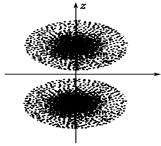
| A.2pz轨道上的电子在空间出现的概率分布是z轴对称 |
| B.点密集的地方表明电子出现的机会多 |
| C.电子先沿z轴正半轴运动,然后在负半轴运动 |
| D.2pz轨道形状为两个椭圆球 |
|
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
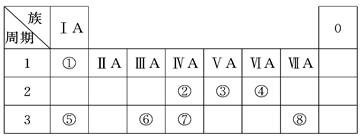
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | | | | | ① | | ② | |
| 三 | ③ | ④ | ⑤ | ⑥ | | | ⑦ | ⑧ |
| 四 | ⑨ | | | | | | ⑩ | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 代号 | 物质 | 结构简式 | 水中溶解度/g (25℃) | 熔点/℃ | 沸点/℃ |
| A | 邻—硝基苯酚 | 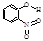 | 0.2 | 45 | 100 |
| B | 对—硝基苯酚 | 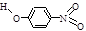 | 1.7 | 114 | 295 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 编号 | 性质 | 化学方程式 |
| 示例 | 氧化性 | H2WO3+3H3PO3===3H3PO4+H2W↑ |
| 1 | | |
| 2 | | |

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X。
物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X。 。(填序号)
。(填序号)| A.氧化性:KBrO3>H3AsO4 | B.氧化性:H3AsO4> KBrO3 KBrO3 |
| C.还原性:AsH3>X | D.还原性:X>AsH3 |

 物能分解为它的另一种氢化物,此分解反应的化学方程式是 。
物能分解为它的另一种氢化物,此分解反应的化学方程式是 。
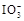 +5I-+6H+=3I2+3H2O,据此反应,可用试纸和一些生活中常见的物质设计实验,证明食盐中存在
+5I-+6H+=3I2+3H2O,据此反应,可用试纸和一些生活中常见的物质设计实验,证明食盐中存在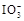 。可供选用的物质有:①自来水;②蓝色石蕊试纸;③碘化钾淀粉试纸;④淀粉;⑤食醋;⑥白酒;⑦食糖。你认为进行上述实验时必须使用的物质是 (填序号)。
。可供选用的物质有:①自来水;②蓝色石蕊试纸;③碘化钾淀粉试纸;④淀粉;⑤食醋;⑥白酒;⑦食糖。你认为进行上述实验时必须使用的物质是 (填序号)。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com