
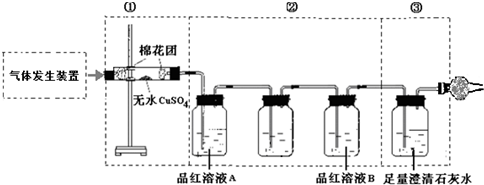
分析 浓硫酸具有强的氧化性,能够在加热条件下氧化碳生成二氧化碳、二氧化硫和水,依据反应为状态和反应条件选择发生装置,要检验水应选择无水硫酸铜,无水硫酸铜遇水显蓝色,检验二氧化硫用品红溶液,二氧化硫具有漂白性,能够使品红溶液褪色,检验二氧化碳需要用澄清石灰水,能够使澄清石灰水变浑浊,二氧化硫也能使澄清石灰水变浑浊,所以检验二氧化碳之前应用酸性高锰酸钾除去二氧化硫,排除二氧化硫对二氧化碳检验造成的干扰,据此解答.
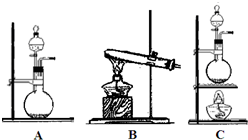
解答 解:(1)浓硫酸具有强的氧化性,能够在加热条件下氧化碳生成二氧化碳、二氧化硫和水,方程式:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2S02↑+C02↑+2H2O,反应物为固体与液体加热,所以应选择C发生装置;
故答案为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2S02↑+C02↑+2H2O;C;
(2)一般检验含有水汽的混合气体,水通常是第一个检验的;实验利用白色硫酸铜遇到水变为蓝色证明含有水蒸气,①中无水硫酸铜的作用是检验反应生成的水蒸气;
故答案为:检验反应生成的水蒸气;
(3)因S02和C02都能使石灰水变浑浊,因此要想检验出C02,就要先把S02检验了,并除掉S02,这样石灰水变浑浊才能说明有C02,即②一定要在③的前面.根据检验SO2和CO2时,就要先把SO2检验了,并除掉SO2,这样石灰水变浑浊才能说明有CO2,所以高锰酸钾溶液是吸收二氧化硫的作用,
故答案为:酸性高锰酸钾,除去混合气体中的SO2;
(4)根据检验SO2和CO2时,就要先把SO2检验了,并除掉SO2,这样石灰水变浑浊才能说明有CO2,所以②中两次用到品红溶液,它们的作用分别是检验生成的SO2气体;检验SO2是否除尽;
故答案为:检验生成的SO2气体;检验SO2是否除尽;
(5)装置是验证二氧化硫气体除净后,检验二氧化碳气体存在的实验装置,反应现象是二氧化碳和氢氧化钙反应生成白色沉淀;
故答案为:出现白色沉淀.
点评 本题考查了反应产物的检验,明确浓硫酸与碳发生反应的实质,熟悉二氧化碳、二氧化硫的性质是解题关键,注意产物检验试验涉及的严密性,题目难度不大.


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 电子在1s轨道上运动像地球围绕太阳旋转 | |
| B. | 2s的电子云半径比1s电子云半径大,说明2s能级的电子比1s的多 | |
| C. | 1s轨道的电子云形状为圆形的面 | |
| D. | nf能级中最多可容纳14个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
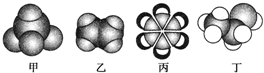
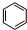 ,丁CH3CH2OH
,丁CH3CH2OH +HO-NO2$→_{△}^{浓硫酸}$
+HO-NO2$→_{△}^{浓硫酸}$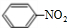 +H2O
+H2O查看答案和解析>>
科目:高中化学 来源: 题型:选择题
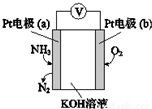
| A. | 该传感器在工作过程中KOH的物质的量不变 | |
| B. | a极的电极反应式为2NH3+3O2--6e-═N2+3H2O | |
| C. | 反应消耗的NH3与O2的物质的量之比为4:5 | |
| D. | b极为负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,4.48L3717Cl2含有0.72NA个中子 | |
| B. | 3717Cl、3517Cl互为同位素,3717Cl2、3517Cl2互为同素异形体 | |
| C. | 通常情况下,氯气做氧化剂,但氯气也具有还原性 | |
| D. | 3717Cl2的摩尔质量是74 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A组 | B组 |
| Ⅰ.H-I键的键能大于H-Cl键的键能 Ⅱ.H-I键的键能小于H-Cl键的键能 Ⅲ.H-I键的键能小于H-Cl键的键能 Ⅳ.HI分子间作用力小于HCl分子间作用力 | ①HI比HCl稳定 ②HCl比HI稳定 ③HI沸点比HCl低 ④HI沸点比HCl低 |
| A. | Ⅰ① | B. | Ⅱ② | C. | Ⅲ③ | D. | Ⅳ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
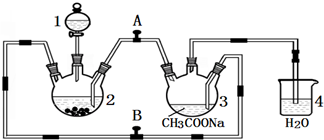
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com