
【题目】根据图1、图2、图3及题中信息,回答下列问题
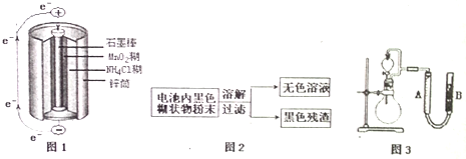
![]() 图1是锌锰干电池基本构造图,该电池的负极材料是 ______ ;工作时
图1是锌锰干电池基本构造图,该电池的负极材料是 ______ ;工作时![]() 离子在正极放电产生两种气体,其中一种气体分子是含
离子在正极放电产生两种气体,其中一种气体分子是含![]() 的微粒,正极的电极反应式是 ______ ;当电路中每通过
的微粒,正极的电极反应式是 ______ ;当电路中每通过![]() ,负极质量减少 ______ ;
,负极质量减少 ______ ;
![]() 图2是利用废旧锌锰干电池内的黑色糊状物分离得到黑色残渣
图2是利用废旧锌锰干电池内的黑色糊状物分离得到黑色残渣![]() 的流程图.该流程中溶解和过滤操作均要使用到的玻璃仪器有 ______ ;
的流程图.该流程中溶解和过滤操作均要使用到的玻璃仪器有 ______ ;
![]() 图3是探究
图3是探究![]() 在制
在制![]() 过程中的作用的实验装置图,利用该装置完成下表中实验一和实验二,实验过程中有关实验现象和所得数据如下表
过程中的作用的实验装置图,利用该装置完成下表中实验一和实验二,实验过程中有关实验现象和所得数据如下表![]() 已知:两次实验气体的体积在相同条件下测定:
已知:两次实验气体的体积在相同条件下测定:![]() 由分液漏斗滴入到圆底烧瓶
由分液漏斗滴入到圆底烧瓶![]() 。
。
序号 | 烧瓶中的物质 | 实验记录 | 实验结论 |
实验一 | 足量 |
|
|
实验二 | 足量 |
|
|
![]() 在测量气体体积时,除要注意待气体温度恢复至室温、平视度数外,还需要注意 ______ ;
在测量气体体积时,除要注意待气体温度恢复至室温、平视度数外,还需要注意 ______ ;
![]() 实验一、二中参加反应的
实验一、二中参加反应的![]() 的物质的量之比为 ______ 。
的物质的量之比为 ______ 。
【答案】Zn ![]()
![]() 烧杯和玻璃棒 催化剂 氧化剂 上下移动B管,使A、B两管中液面相平 2:1
烧杯和玻璃棒 催化剂 氧化剂 上下移动B管,使A、B两管中液面相平 2:1
【解析】
![]() 锌锰干电池的负极上Zn失去电子;
锌锰干电池的负极上Zn失去电子; ![]() 离子在正极得电子生成氨气和氢气;根据
离子在正极得电子生成氨气和氢气;根据![]() 计算消耗Zn的质量;
计算消耗Zn的质量;
(2)根据基本操作溶解和过滤操作分析;
(3)实验一涉及反应为![]() ,实验二中的反应为
,实验二中的反应为![]() 。
。
![]() 锌锰干电池的负极上Zn失去电子,负极反应为
锌锰干电池的负极上Zn失去电子,负极反应为![]() ,该电池的负极材料是Zn;由
,该电池的负极材料是Zn;由![]() 离子在正极放电产生2种气体,其中一种气体分子是含
离子在正极放电产生2种气体,其中一种气体分子是含![]() 的微粒为氨气,另一种为氢气,正极反应为
的微粒为氨气,另一种为氢气,正极反应为![]() ,当电路中每通过
,当电路中每通过![]() ,根据负极反应
,根据负极反应![]() ,可知消耗
,可知消耗![]() ,质量为
,质量为![]() ;
;
![]() 溶解需要玻璃棒、烧杯等仪器,过滤需要玻璃棒、烧杯以及漏斗等仪器,则均使用的玻璃仪器为烧杯和玻璃棒;
溶解需要玻璃棒、烧杯等仪器,过滤需要玻璃棒、烧杯以及漏斗等仪器,则均使用的玻璃仪器为烧杯和玻璃棒;
![]() ①充分反应后未见黑色固体物质减少,二氧化锰起到催化剂的作用,过氧化氢在二氧化锰催化作用下生成氧气;
①充分反应后未见黑色固体物质减少,二氧化锰起到催化剂的作用,过氧化氢在二氧化锰催化作用下生成氧气;
②充分反应后黑色粉末部分溶解,生成锰离子,Mn元素化合价降低,反应中二氧化锰起到氧化剂的作用;
③测量气体体积时,除要注意待气体温度恢复至室温、平视读数外,要注意上下移动B管,使A、B两管中液面相平;
④实验一涉及反应为![]() 、实验二中反应生成锰离子、水、氧气,离子反应为
、实验二中反应生成锰离子、水、氧气,离子反应为![]() ,由氧气的体积1:1可知,参加反应的
,由氧气的体积1:1可知,参加反应的![]() 的物质的量之比为2:1。
的物质的量之比为2:1。


科目:高中化学 来源: 题型:
【题目】成熟的苹果中含有淀粉、葡萄糖和无机盐等,某课外兴趣小组设计了一组实验证明某些成份的存在,请你参与并协助他们完成相关实验。
(1)用小试管取少量的苹果汁,加入_________,溶液变蓝,则苹果中含有淀粉。
(2)用小试管取少量的苹果汁,加入新制Cu(OH)2悬浊液,并加热,产生砖红色的沉淀,则苹果中含有____________(写分子式)。
(3)葡萄糖在一定条件下可以得到化学式为C2H6O的化合物A。
A + CH3COOH→有香味的产物
① 含A的体积分数为75%的水溶液可以用做_____________。
②写出化合物A与CH3COOH反应的化学方程式为______________________,该反应的类型为_____。
(4)苹果中含有苹果酸,测得其相对分子质量为134。取0.02mol苹果酸,使其完全燃烧,将燃烧后的产物先后通过足量的无水CaCl2和碱石灰,两者分别增重1.08g 和 3.52g。则分子中C、H原子的个数比_______。苹果酸的分子式是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温常压下,取下列四种有机物各1mol,分别在足量的氧气中燃烧,消耗氧气最多的是
A. C2H5OH B. CH4 C. C2H4O D. C3H8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究铜跟浓硫酸的反应,用如图所示装置进行有关实验。请回答:

(1)装置A中发生反应的化学方程式:_________。
(2)装置D中试管口放置浸有NaOH溶液的棉花,其作用是______。
(3)装置B中应放置的液体是______。
(4)反应完毕,发现烧瓶中有铜片剩余,下列药品中能用来证明反应结束后的烧瓶中确有余酸的是______(填字母)。
a.铁粉 b.BaCl2溶液 c.银粉 d.NaHCO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2L密闭容器中X、Y、Z三种气态物质的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据
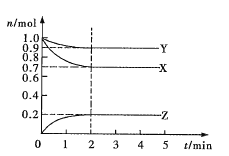
(1)该反应的化学方程式为______________。
(2)反应开始至2min,用Z表示的平均反应速率为_________。
(3)下列叙述能说明上述反应达到化学平衡状态的是________(填序号)
A.混合气体的总物质的量不随时间的变化而变化
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗![]() X,同时生成
X,同时生成![]() Z
Z
D.混合气体的总质量不随时间的变化而变化
E.混合气体的密度不再发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于取代反应的是
A.CH4+2O2![]() CO2+2H2O
CO2+2H2O
B.CH2=CH2+H2![]() CH3CH3
CH3CH3
C.2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
D.![]() +HO-NO2
+HO-NO2![]()
 +H2O
+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质常温下发生水解,对应的离子方程式正确的是
A.Na2CO3:CO32-+2H2O![]() H2O+CO2↑+2OH-
H2O+CO2↑+2OH-
B.NH4Cl:NH4++H2O![]() NH3·H2O+OH-
NH3·H2O+OH-
C.CuSO4:Cu2++2H2O![]() Cu(OH)2+2H+
Cu(OH)2+2H+
D.NaF:F-+H2O=HF+OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把0.4molX气体和0.6molY气体混合于2L密闭容器中,使它们发生如下反应:4X(g)+5Y(g) ![]() nZ(g)+6W(g)。2min末已生成0.3molW,若测知以Z的浓度变化表示的反应速率为0.05mol/(L·min),试计算
nZ(g)+6W(g)。2min末已生成0.3molW,若测知以Z的浓度变化表示的反应速率为0.05mol/(L·min),试计算
(1)前2min内用W的浓度变化表示的平均反应速率为_______________。
(2)2min末时Y的浓度为_____________________________。
(3)化学反应方程式中n=_____________________________。
(4)2min末,恢复到反应前温度,体系内压强是反应前压强的__________倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种制备高效漂白剂NaC1O2的实验流程如图所示,反应I的化学方程式为: 3NaC1O3+4SO2+3H2O=2C1O2+Na2SO4+3H2SO4+NaCl,下列说法正确的是
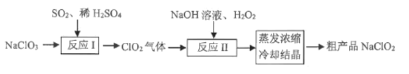
A.NaClO2的漂白原理与SO2相同
B.反应I中氧化产物和还原产物物质的量比为4:3
C.反应II中H2O2做氧化剂
D.实验室进行蒸发操作通常在坩埚中进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com