
| A. | 等质量的H2O与CH2D2含有的质子数相同 | |
| B. | 1L 0.1mol•L-1 NH4Cl溶液中Cl-的数目为0.1NA | |
| C. | 标准状况下,6.72L NO2与水充分反应转移的电子数为0.2NA | |
| D. | 1mol CH3COOC2H5在足量H2SO4溶液中水解得到的乙醇分子数为NA |
分析 A.1个H2O含有10个质子,1个CH2D2含有10个质子,二者摩尔质量相等;
B.依据n=CV计算氯化铵的物质量,1mol氯化铵电离产生1mol氯离子;
C.求出二氧化氮的物质的量,然后根据3mol二氧化氮与水反应时转移2mol电子来分析;
D.酯的水解反应为可逆反应,可逆反应不能进行到底.
解答 解:A.H2O与CH2D2摩尔质量相等,含有质子数相等,依据n=$\frac{m}{M}$可知,质量相等的H2O与CH2D2物质的量相等,含有质子数相同,故A正确;
B.1L 0.1mol•L-1 NH4Cl溶液中含有氯化铵的物质的量为0.1mol/L×1L=0.1mol,含有氯离子物质的量为1mol,Cl-的数目为0.1NA,故B正确;
C.标况下6.72L二氧化氮的物质的量为0.3mol,而3mol二氧化氮与水反应时转移2mol电子,故0.3mol二氧化氮转移0.2mol电子即0.2NA个,故C正确;
D.酯的水解反应为可逆反应,可逆反应不能进行到底,1mol CH3COOC2H5在足量H2SO4溶液中水解得到的乙醇分子数小于NA,故D错误;
故选:D.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,注意可逆反应不能进行到底的特点.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 现象或事实 | 解释 |
| A | 用热的纯碱溶液洗去油污 | Na2CO3可直接与油污反应 |
| B | 漂白粉在空气中久置变质 | 漂白粉中的CaCl2与空气中的CO2反应生成CaCO3 |
| C | 向Mg(OH)2悬浊液中滴加CuSO4溶液,生成蓝色沉淀 | Cu(OH)2的溶度积比Mg(OH)2的小,Mg(OH)2转化为Cu(OH)2 |
| D | 施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用 | K2CO3与NH4Cl反应会损失钾肥 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | L电子层的电子数为奇数的所有元素都是非金属元素 | |
| B. | 短周期元素X、Y的原子序数相差2,则X、Y不可能处于同一主族 | |
| C. | 从左至右第8、9、10三列元素中没有非金属元素 | |
| D. | 若M+和R2+的核外电子层结构相同,则可推出原子序数:R>M |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
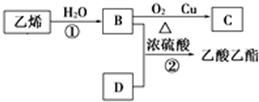
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com