
【题目】某化学兴趣小组的同学利用下图所示实验装置进行实验(图中a、b、c表示止水夹) 。

(1)A、C、E相连后的装置可用于制取Cl2并进行相关的性质实验。①若在丙中加入适量水,即可制得氯水。将所得氯水进行实验,实验操作、现象、结论如下:
实验操作 | 现 象 | 结 论 |
氯水中加入碳酸氢钠粉末 | 有无色气泡产生 | 氯气和水反应的产物具有酸性 |
实验的结论是否合理__________,(选填合理或不合理)请说明理由______________________。请利用上述装置设计一个简单的实验验证Cl-和S2-的还原性强弱,则甲、乙、丙中盛放的试剂是甲__________________ 乙__________________ 丙__________________
(2)B、D、E装置相连后,在B中盛装浓硝酸和铜片(放在有孔塑料板上),可制得并进行NO2有关实验。欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹________,再打开止水夹________,使烧杯中的水进入试管丁的操作是:___________________________________使试管中的气体逸出,NO2与水接触后即可引发烧杯中的水进入试管丁。
【答案】不合理 制取的氯气中含有氯化氢,溶于水遇碳酸氢钠粉末有气泡 浓盐酸 MnO2 硫化钠溶液 ab c 双手紧握(或微热)试管丁
【解析】
(1)用二氧化锰和浓盐酸加热制备的氯气中混有氯化氢气体,据此分析解答;可根据反应Cl2+S2- =2Cl- +S↓设计实验验证Cl-和S2-的还原性强弱;
(2)浓硝酸具有强氧化性,与铜反应生成二氧化氮气体收集在丁中,NO2能够与水反应,使得气体压强减小,结合装置D的特征分析解答。
(1)根据图示,A装置制备的氯气中含有HCl气体,HCl气体溶于水就是盐酸,盐酸能够与碳酸氢钠粉末反应生成二氧化碳气体,在实验中没有进行除杂,不能说明氯气和水反应的产物具有酸性;要验证Cl-和S2-的还原性强弱,可根据反应Cl2+S2- =2Cl- +S↓设计实验,在A装置中,生成的气体通入到装有硫化钠溶液的中,在C中盛放硫化钠溶液,如试管中溶液由无色变为淡黄色浑浊,即可证明氯气的氧化性强于硫,则S2-的还原性强于Cl-,故答案为:不合理;制取的氯气中含有HCl气体,HCl溶于水后能与碳酸氢钠粉末反应产生气泡;浓盐酸;MnO2;硫化钠溶液;
(2)浓硝酸具有强氧化性,与铜反应生成二氧化氮气体,反应的化学方程式为Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O;浓硝酸与铜反应生成的二氧化氮收集于试管丁中,要验证NO2与水的反应,要先关闭a、b,打开止水夹c,然后用微热法使试管中气体逸出,NO2与水接触后即可引发烧杯中的水倒流入试管丁中,故答案为:ab;c;双手紧握(或微热)试管丁。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】(1)氢氧燃料电池是一种高效无污染的清洁电池它分碱性(用KOH做电解质)和酸性(用硫酸做电解质)燃料电池。如果是酸性燃料电池,则正极反应方程式是___。
(2)科研人员设想用如图原电池装置生产硫酸,则负极的电极反应式为___。

(3)二氯化二硫(S2Cl2)是一种琥珀色液体,是合成硫化染料的重要原料。
a.S2Cl2分子中所有原子都满足8电子稳定结构,写出它的电子式__;
b.指出它分子内的键型__。
(4)分子式为C5H12O的有机物,能与金属钠反应产生氢气的有__种,其中能够发生催化氧化生成醛的有___种。
(5)乙烷中混有丙烯杂质,写出除杂的化学反应方程式__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某化合物的晶体是由以下最小单元密置堆积而成的,关于该化合物的以下叙述中错误的是
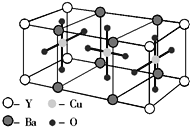
A.1 mol该化合物中有1 mol Y
B.1 mol该化合物中有3 mol Cu
C.1 mol该化合物中有2 mol Ba
D.该化合物的化学式是YBa2Cu3O6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将有机物完全燃烧,生成CO2和H2O。将6g该有机物的完全燃烧产物先通过浓硫酸,浓硫酸增重3.6g,再通过碱石灰,碱石灰增重8.8g。则该有机物的分子式为( )
A.C4H10B.C2H6OC.C3H8OD.C2H4O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨及其相关工业中,部分物质间的转化关系如下:
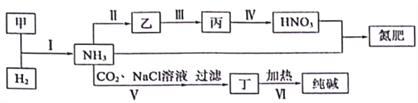
下列说法不正确的是( )
A. 反应Ⅰ、Ⅱ、Ⅲ、Ⅳ均属于氧化还原反应
B. 上述转化中包含了氨气、硝酸、硝铵、小苏打、纯碱的工业生产方法
C. 反应Ⅳ和Ⅵ中的部分产物可在上述流程中循环利用
D. 反应V是先向饱和氯化钠溶液中通CO2至饱和再通NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学通过实验研究FeCl3溶液与Cu粉发生的氧化还原反应。实验记录如下:
序号 | I | II | III |
实验步骤 |
充分振荡,加入2mL蒸馏水 |
充分振荡,加入2mL蒸馏水 |
充分振荡,加入2mL蒸馏水 |
实验现象 | 铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象 | 铜粉有剩余,溶液黄色褪去,加入蒸馏水后生成白色沉淀 | 铜粉有剩余,溶液黄色褪去,变成蓝色,加入蒸馏水后无白色沉淀 |
下列说法不正确的是
A. 实验I、II、III中均涉及Fe3+被还原
B. 对比实验I、II说明白色沉淀的产生与铜粉的量有关
C. 实验II、III中加入蒸馏水后c(Cu2+)相同
D. 向实验III反应后的溶液中加入饱和NaCl溶液可能出现白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酒精灯给试管里的物质加热时,发现试管破裂可能的原因有:①用酒精灯的外焰加热;②加热时试管外壁的水没有擦干;③加热时试管底部接触灯芯;④被加热的液体超过试管容积的![]() ;⑤加热液体时没有不时的上下移动试管;⑥没有进行预热,直接集中加热试管里的物质;⑦加热固体时试管口向上倾斜。其中与之相关的是( )
;⑤加热液体时没有不时的上下移动试管;⑥没有进行预热,直接集中加热试管里的物质;⑦加热固体时试管口向上倾斜。其中与之相关的是( )
A.②③⑤⑦B.②④⑤⑥C.②③⑥⑦D.①③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对于过氧化钠的叙述中,正确的是( )
A. 将少量Na2O2投入紫色石蕊试液中,溶液最终呈蓝色
B. 1 mol Na2O2与H2O完全反应,转移2 mol电子
C. 充分加热等物质的量的Na2O2和NaHCO3的混合物,剩余物质为Na2CO3
D. a g CO和H2的混合气体充分燃烧的产物与足量的Na2O2充分反应后,固体质量增加a g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组用含A、B两种金属单质的粉末状混合物进行如下实验,其转化关系如下图所示(部分反应物和生成物未列出),其中E为白色胶状沉淀,I为红褐色沉淀。(此转化关系中所用的试剂都是足量的)
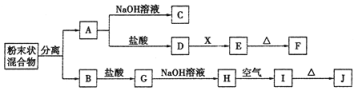
(1)写出下列物质的化学式:F____________,G________________。
(2)将混合物中两种金属分离开的最简单的方法是___________。
(3)D→E的转化中,加入过量的X可能是_____________________。
A.饱和NaCl溶液 B.NaOH溶液 C.氨水 D.Ba(OH)2溶液
(4)写出下列转化的化学方程式:
A→C:______________________________________________;
H→I:_______________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com